Будуємо графік залежності «молярна частка - температура» для двох речовин (g) та (a), тому що параалкілфеноли зіллються в одну лінію, те ж саме станеться і з ортоалкілфеноламі.
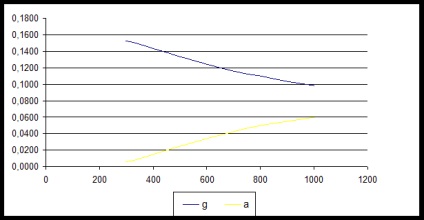
З графіка видно, що при збільшенні температури молярна частка параалкілфенолов зменшується. Тому процес слід вести при невисоких температурах.
Як правило, параалкілфеноли використовується як проміжний продукт для синтезу неіоногенних поверхнево-активних речовин шляхом їх оксіетилювання:
Щоб отримати продукти з кращого біохімічної Здатність до розпаду необхідний алкіл з менш розгалуженим ланцюгом.
2. Адіабатичний перепад температур в реакторі
(Є помилка в розрахунках ентальпії АЛКІЛФЕНОЛИ, реакція екзотермічна)
Розрахуємо тепловий ефект реакції і температуру суміші в кінці реакції в адіабатичному реакторі. Припустимо, що при алкилировании фенолу тетрадеценом-1 утворюється 7- (4'-гідроксифеніл) тетрадекан.
Кількості тепла входить в реактор складається з тепла внесеного з фенолом і олефіном. Витрата фенолу 1,1 моль / год, витрата олефина 1 моль / год.
Необхідно знайти температуру вихідної суміші з реактора, для цього потрібно знати температуру вхідної суміші. Після змішування фенолу і олефина їх середня температура буде дорівнює tвх, пор. Таким чином Qвх одно:
Використовуючи програму Microsoft Excel і функцію «підбір параметрів», а так само певні раніше залежності теплоємності від температури і кількість тепла що входить в реактор знайдемо tвх, пор.
Tвх, ср = 315,13 К, при цьому = 110,45 (Дж / моль), = 328,84 (Дж / моль).
Ентальпія реакції з слідства закону Гесса дорівнює:
= - =
= - (+)
= -229297 + (98386,5 + 227532) = 96621,5 (Дж / моль)
Реакція ендотермічна, протікає зі зменшенням кількості тепла у всій системі.
Припустимо що ступінь конверсії олефина 100%.
Кількість тепла, що виходить з сумішшю з предконтактной зони одно:
Qвих = Qвх - Qреакціі
Qвих = 141911,6 - 96621,5 = 45290,1 (Дж / год)
Так само кількості тепла виходить з сумішшю можна розрахувати через Tвих, пор.
Таким чином Tвих, ср = 171,26 К.
3. Кінетика процесу
1. Відбувається протонирование олефина з утворенням карбкатиона:
2. Утворюється-комплекс:
3. Утворюється-комплекс. Дана стадія є лімітуючої.
4. Відрив протона від ароматичного ядра:
Отделившийся протон може взаємодіяти з олефіном, і процес піде заново або з каталізатором, тоді реакція припинитися.
В якості каталізаторів - протонних кислот - в промисловості найчастіше застосовують сірчану кислоту. Вона є найбільш активною серед інших доступних і дешевих кислот, але в той же час каталізує і побічні реакції, приводячи додатково до сульфуванням фенолу і сульфуванням олефина і утворюючи фенолсульфокіслоти HOC6H4SO2OH і моноалкілсульфати ROSO2OH, які також беруть участь в каталізі процесу. З сірчаною кислотою алкілування н-оліфінамі відбувається при 100-120ºС. Іншим каталізатором, що не викликає побічних реакцій сульфування і більш м'яким за своєю дією, є п-толуолсульфокіслоти CH3C6H4SO2OH. Однак вона має меншу активність і велику вартість, ніж H2SO4.
З цими каталізаторами алкілування фенолу протікає як гомогенна реакція по наступному рівнянню:
=
З рівняння видно, що при збільшенні концентрації однієї з речовин швидкість реакції лінійно зросте. У виробництві працюють при порівняно невеликому надлишку фенолу по відношенню до олефину і навіть при їх еквімольном кількості. Якщо в якості каталізатора беруть H2SO4, то вона застосовується в кількості 3-10% (мас.). Збільшення температури позитивно позначиться на швидкості реакції, тому що процес ендотермічний.
4. Технологія процесу
Для алкілування фенолів застосовують періодичний процес. Реакцію проводять в апараті з мішалкою і сорочкою для обігріву парою або охолодження водою. У нього завантажують фенол і каталізатор, нагрівають їх до 90 ºС, після чого при перемішуванні і охолодженні подають рідкий тетрадецен-1 при температурі 25 ºС (температура плавлення -12,7 ºС). Роблять саме так тому що, якщо завантажити спочатку каталізатор з олефіном, то там можуть піти реакції олиго- і полімеризації. У другій половині реакції, навпаки, необхідно підігрівати реакційну масу. Загальна тривалість операції становить 2-4 години. Після цього реакційну масу нейтралізують в змішувачі 5% -ної лугом, взятої в еквівалентній кількості до кислоті-каталізатору, нагріваючи суміш гострою парою. Нейтралізований органічний шар сирих алкилфенолов відокремлюють від водяного розчину солей і направляють на вакуум перегонку, коли відганяється вода, залишки олефина і не перетворений фенол.
При окислювальному аммоноліз пропілену отримана реакційна маса такого складу (% мас.): - пропілен - 18,94, нітрил акрилової кислоти - 54,85, ацетонітрил - 13,00, ацетальдегід - 1,15, пропіоновий альдегід - 5,07, синильна кислота - 4,99, формальдегід - 0,80, СО2 - 1,20. Обчислити ступінь конверсії реагентів, селективність процесу по кожному з продуктів реакції в розрахунку на кожен реагент і вихід на пропущене сировину кожного з продуктів реакції в розрахунку на один реагент.
Рішення: найбільш ймовірна схема перетворень при окислювальному аммоноліз:
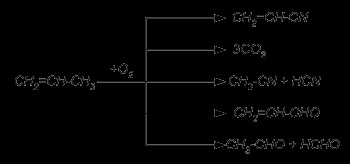
Складемо таблицю розподілу мовляв. часткою вих. речовини: