Стронцій розташований в п'ятому періоді II групи головною (А) підгрупі Періодичної таблиці.
Відноситься до елементів s -сімейство. Метал. Позначення - Sr. Порядковий номер - 38. Відносна атомна маса - 87,62 а.е.м.
Електронна будова атома стронцію
Атом стронцію складається з позитивно зарядженого ядра (+38), всередині якого є 38 протонів і 50 нейтронів, а навколо, по п'яти орбітах рухаються 38 електронів.
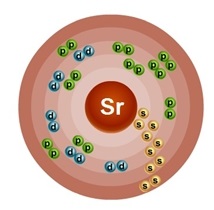
Рис.1. Схематична будова атома стронцію.
Розподіл електронів по орбіталях виглядає наступним чином:
Зовнішній енергетичний рівень атома стронцію містить 2 електрона, які є валентними. Енергетична діаграма основного стану приймає наступний вигляд:
Валентні електрони атома стронцію можна охарактеризувати набором з чотирьох квантових чисел: n (головне квантове), l (орбітальне), ml (магнітне) і s (спіновий):
Вкажіть яку атомну орбіталь і чому вибере черговий електрон згідно з принципом найменшої енергії: 3d або 4p, 5s або 4d, 4s або 3p, 4d або 5p.
Заповнення орбіталей електронами відбувається відповідно до принципу Паулі, правилами Клечковского і хунди. Спочатку заповнюються електрони з найменшим значенням суми (n + l), де n-головне квантове число, а l- орбітальне квантове число. Якщо ця сума для декількох підрівнів однакова, першої заповнюється орбіталь з найменшим значенням n.
Тоді, з двох орбіталей (в дужках вказана сума n + l) 3d (5) і 4p (5) першої буде заповнюватися 4p-орбіталь; з 5s (5) і 4d (6) - 5s-підрівень; з 4s (4) і 3p (4) - 3р-підрівень; з 4d (6) і 5p (6) - 4d -подуровень.