Схема атома кисню
Однак Прістлі спочатку не зрозумів, що відкрив нове проста речовина. він вважав, що виділив одну із складових частин повітря (і назвав цей газ «дефлогістрованим повітрям»). Про своє відкриття Прістлі повідомив видатному французькому хіміку Антуану Лавуазьє. У 1775 А. Лавуазьє встановив, що кисень є складовою частиною повітря, кислот і міститься в багатьох речовинах.
Таким чином, заслугу відкриття кисню фактично ділять між собою Прістлі, Шеєле і Лавуазьє.
походження назви
Слово кисень (іменувався на початку XIX століття ще «кіслотвором») своєю появою в російській мові зобов'язане М. В. Ломоносову - це калька терміна «оксиген» (фр. L'oxygène), запропонованого А. Лавуазьє (грецьке όξύγενναω від ὀξύς - « кислий »і γενναω -« народжую »), який перекладається як« породжує кислоту », що пов'язано з первісним значенням його -« кислота », раніше який передбачав оксиди, іменовані по сучасній міжнародній номенклатурі оксидами.
Знаходження в природі
В даний час в промисловості кисень одержують з повітря. У лабораторіях користуються киснем промислового виробництва, що поставляються в сталевих балонах під тиском близько 15 МПа. Найважливішим лабораторним способом його отримання є електроліз водних розчинів лугів. Невеликі кількості кисню можна також отримувати взаємодією розчину перманганату калію з підкисленим розчином пероксиду водню. Також добре відомі і успішно застосовуються в промисловості кисневі установки. що працюють на основі мембранної і азотної технологій.Прі нагріванні перманганат калію KMnO4 розкладається до манганата калію K2 MnO4 і діоксиду марганцю MnO2 з одночасним виділенням газоподібного кисню O2:
У лабораторних умовах отримують також каталітичним розкладанням пероксиду водню Н2 О2:
Каталізатором є діоксид марганцю (MnO2) або шматочок сирих овочів (в них містяться ферменти. Прискорюють розкладання пероксиду водню).
Кисень можна також отримати каталітичним розкладанням хлорату калію (бертолетової солі) KClO3:
Каталізатором також виступає MnO2.
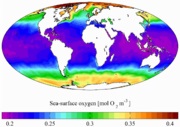
Холодна вода містить більше розчиненого O2
Фізичні властивості
При нормальних умовах кисень це газ без кольору, смаку і запаху. 1л його важить 1,429 м Трохи важче повітря. Слабо розчиняється у воді (4,9 мл / 100г при 0 ° C, 2,09 мл / 100г при 50 ° C) і спирті (2,78 мл / 100г при 25 ° C). Добре розчиняється в розплавленому сріблі (22 обсягу O2 в 1 обсязі Ag при 961 ° C). Є парамагнетиком.
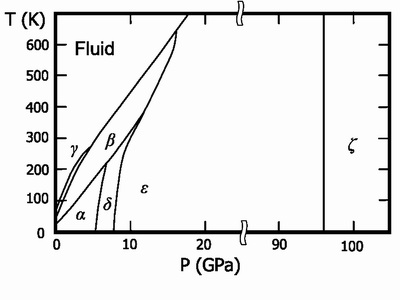
Твердий кисень (темп. Плавлення -218,79 ° C) - сині кристали. Відомі 6 кристалічних фаз. з яких 3 існують при тиску в 1 атм.
- α-О2 температура нижче -249,35 ° C, яскраво-сині кристали, ромбічна сингонія. параметри осередку a = 5,50Å, b = 3,82Å, c = 3,44Å;
- β-О2 температура від -249,35 до -229,35 ° C, блідо-сині кристали, при підвищенні тиску колір переходить в рожевий, ромбоедрична сингония, a = 6,19Å, α = 99 ° 6;
- γ-О2 температура від -229.35 до -218,79 ° C, блідо-сині кристали, кубічна сингонія, a = 6,83Å;
Ще три фази утворюються при високому тиску:
- δ-О2 інтервал температур до 300 К і тиск 6-10 GPa. помаранчеві кристали;
- ε-О2 тиск від 10 і до 96 GPa, колір кристалів від темно червоного до чорного, МОНОКЛІННА СИНГОНІЯ;
- ζ-О2 тиск більше 96 GPa, металевий стан з характерним металевим блиском, при низьких температурах переходить в надпровідний стан.
Хімічні властивості
- Сильний окислювач, взаємодіє, практично, з усіма елементами, утворюючи оксиди. Ступінь окислювання -2. Як правило, реакція окислення протікає з виділенням тепла і прискорюється при підвищенні температури. Приклад реакцій, що протікають при кімнатній температурі:
- окисляє сполуки, які містять елементи з не максимальним ступенем окислення:
- окисляє більшість органічних сполук:
- за певних умов можна провести «ніжне» окислення органічної сполуки:
- Кисень не окисляє Au і Pt. галогени та інертні гази.
- Кисень утворює пероксиди зі ступенем окислення -1.
- наприклад, пероксиди виходять при згорянні лужних металів в кисні:
-
- по теорії горіння, розробленої А. Н. Бахом і Енглер, окислення відбувається в дві стадії з утворенням проміжного пероксидного з'єднання. Це проміжне з'єднання можна виділити, наприклад, при охолодженні полум'я палаючого водню льодом, поряд з водою, утворюється перекис водню:
- Надпероксида мають ступінь окислення -1/2, тобто один електрон на два атома кисню (іон O2 -). Отримують взаємодією пероксидов з киснем при підвищених тисків і температури:
- Озоніди містять іон O3 - зі ступенем окислення -1/3. Отримують дією озону на гідроксиди лужних металів:
- Іон діоксігеніл O2 + має ступінь окислення +1/2. Отримують по реакції:
- фториди кисню
- Дифторид кисню. OF2 ступінь окислення +2, отримують пропусканням фтору через розчин лугу:
-
- Монофторид кисню (Діоксідіфторід), O2 F2. нестабільний, ступінь окислення +1. Отримують з суміші фтору з киснем в тліючому розряді при температурі -196 ° С.
- Пропускаючи тліючий розряд через суміш фтору з киснем за певних тиску і температурі виходять суміші вищих фторидів кисню O3 F2. О4 F2. ПРО5 F2 і ПРО6 F2.
- підтримує процеси дихання, горіння, гниття
- існує в двох аллотропних модифікаціях: O2 і O3 (Озон)
застосування
Широке промислове застосування кисню почалося в середині ХХ століття, після винаходу турбодетандеров - пристроїв для скраплення і поділу рідкого повітря.
У металургії
Конвертерний спосіб виробництва сталі пов'язаний із застосуванням кисню.
Зварювання та різання металів
Кисень в балонах широко використовується для газополум'яної різання і зварювання металів.
Як окислювач для ракетного палива застосовується рідкий кисень. перекис водню. азотна кислота і інші багаті киснем з'єднання. Суміш рідкого кисню і рідкого озону - один з найпотужніших окислювачів ракетного палива (питомий імпульс суміші водень - озон перевищує питомий імпульс для пари водень -фтор і водень -фторід кисню).
В медицині
Кисень використовується для збагачення дихальних газових сумішей (аеронетікі) при порушенні дихання. для лікування астми. у вигляді кисневих коктейлів, кисневих подушок і т. д.
У харчовій промисловості
У харчовій промисловості кисень зареєстрований в якості харчової добавки E948 [1]. як пропеллент і пакувальний газ.
Біологічна роль кисню
Живі істоти дихають киснем повітря. Широко використовується кисень в медицині. При серцево-судинних захворюваннях, для поліпшення обмінних процесів, в шлунок вводять кисневу піну ( «кисневий коктейль»). Підшкірне введення кисню використовують при трофічних виразках, слоновості, гангрени та інших серйозних захворюваннях. Для знезараження і дезодорації повітря і очищення питної води застосовують штучне збагачення озоном. Радіоактивний ізотоп кисню 15 O застосовується для досліджень швидкості кровотоку, легеневої вентиляції.
Токсичні похідні кисню
Деякі похідні кисню (т. Н. Реактивні форми кисню), такі як синглетний кисень. перекис водню. супероксид. озон і гідроксильний радикал. є високотоксичними продуктами. Вони утворюються в процесі активування або часткового відновлення кисню. Супероксид (супероксидний радикал), перекис водню і гідроксильний радикал можуть утворюватися в клітинах і тканинах організму людини і тварин і викликають оксидативний стрес.
Є радіоактивні ізотопи 11 О, 13 О, 14 О (період напіврозпаду 74 сек), 15 О (Т1 / 2 = 2,1 хв), 19 О (Т1 / 2 = 29,4 сек), 20 О (суперечливі дані по періоду напіврозпаду від 10 хв до 150 років).
Цікаві факти
- Молекули кисню при кімнатній температурі рухаються з надзвуковою середньою швидкістю, що становить 480 метрів в секунду. [2]
Дивитися що таке "Кисень (газ)" в інших словниках:
КИСЕНЬ - газ, у воді знаходиться у вигляді розчинених молекул. Присутність його є обов'язковою умовою для існування більшості організмів, що живуть у воді. Влітку кількість К. в воді безперервно поповнюється з атмосфери і за рахунок виділення його ... ... Ставкове рибництво
Кисень - Цей термін має також інші значення див. Кисень (значення). 8 Азот ← Кисень → Фтор ... Вікіпедія
кисень - а; м. Хімічний елемент (O), газ без кольору і запаху, що входить до складу повітря, необхідний для дихання і горіння і утворює в поєднанні з воднем воду. ◊ Перекрити кисень кому л. Створити нестерпні умови життя, роботи. ◁ Кисневий, ... ... Енциклопедичний словник
КИСЕНЬ - (латинське Oxygenrum) хімічний елемент; символ О; атомний номер 8, відносна атомна маса 15,999. При нормальних умовах кисень газ без кольору і запаху. У звичайних умовах молекула кисню двухатомная (О2); в тихому електричному ... ... Металургійний словник
КИСЕНЬ - КИСЛОРОД, найлегший елемент VI групи періодичної системи Менделєєва, симв. О, порядковий номер 8. К. газ без кольору, запаху і смаку. Ізотопів не має. Ат. в. 16,000, мовляв. в. 32,000. Уд. в. К. по відношенню до повітря 1,10535; при 0 ° і 760 ... Велика медична енциклопедія
КИСЕНЬ - (Охуgenum). Безбарвний газ без запаху і смаку. Мало розчинний у воді (приблизно 1:43). Інгаляціями кисню широко користуються при різних захворюваннях, що супроводжуються гіпоксією: при захворюваннях органів дихання (пневмонія, набряк легенів ... Словник медичних препаратів
КИСЕНЬ - (Oxygenium), О, хімічний елемент VI групи періодичної системи, атомний номер 8, атомна маса 15,9994; газ, температуру кипіння 182,962шC. Кисень найбільш поширений елемент, в атмосфері 23,10% по масі вільного кисню, в гідросфері і ... ... Сучасна енциклопедія
КИСЕНЬ - (лат. Oxygenium) О, хімічний елемент VI групи періодичної системи, атомний номер 8, атомна маса 15,9994. У вільному вигляді зустрічається у вигляді двох модифікацій О2 (звичайний кисень) і О3 (озон). О2 газ без кольору і запаху, щільність 1,42897 ... ... Великий Енциклопедичний словник
Кисень - найпоширеніший елемент земної кори. Содер. його становить 49,13 за вагою і 91,8% за обсягом. У літосфері содер. 47% К. за вагою, в гідросфері 85,89% і в атмосфері 23,01%. Переважна частина атомів К. (близько 99,99%) має високу хім. ... ... Геологічна енциклопедія
Кисень (Oxygen) - газ без кольору і запаху, що становить одну п'яту частину всього атмосферного повітря. Кисень необхідний для життя більшості живих організмів, так як в ході його сполуки з глюкозою (або іноді з іншими видами палива джерелами енергії) в ... ... Медичні терміни
- Кисень. Jesse Russell. Ця книга буде виготовлена в відповідності з Вашим замовленням за технологією Print-on-Demand. Увага! Книга являє собою набір матеріалів з Вікіпедії і / або інших online-джерел. ... Детальніше Купити за 998 руб
- Кисень в нашому житті. А. Ю. Аксельрод. Відомо, що кисень - це "газ" життя. Але навіщо клітинам організму кисень? Скільки кисню людині потрібно в хвилину? В годину? На рік? Що таке "кисневе голодування" і як з ним борються ... Детальніше Купити за 140 руб
- Захоплююча хімія. Дитяче видавництво Олена. Зустрічайте: «Захоплююча хімія»! В кінці цієї подорожі дядько кузя і Чевостік виконають на самій звичайній кухні кілька хімічних дослідів. Це - дуже захоплююче заняття і, хочу особливо ... Детальніше Купити за 126 руб аудіокнига