Сторінка 121 з 126
Діапазон лікувальних заходів, який можна робити за допомогою сучасних ендоскопів, широкий. Іригаційні електрорезектоскопи дозволяють видаляти новоутворення уретри в межах здорових тканин. Віддалені результати лікування хворих з папілярними утвореннями уретри показують відсутність рецидивів протягом 3 років, що свідчить про ефективність ендоуретральних хірургії подібних захворювань [Лопаткін Н. А. Симонов В. Я. 1981.]. Внутрішня уретротомія при коротких стриктурах уретри є ефективним методом лікування даного захворювання.
Апаратура та інструменти.
Для проведення оперативного втручання використовують спеціальні інструменти: електрорезектоскоп з голчастим електродом, оптичний уретротом з рухомим ножем.
Методи лікувальної ендоскопії. Ендоскопічна електрохірургія нижніх сечових шляхів є методом вибору оперативного втручання, дозволяє уникнути великих повітряних операцій, тривалого епіцістостоміческого дренування і сприяє профілактиці запальних захворювань сечових шляхів.
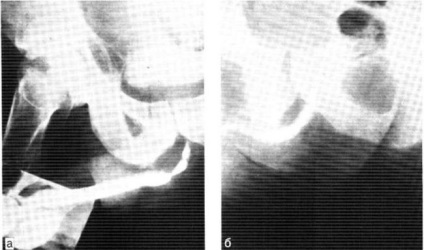
За допомогою трансуретральних втручань вдається ліквідувати стриктури уретри, що виникли після позаділобковой або трансвезікальной аденомектоміі (рис. 5.14). Склеротичні процеси в задній уретре- в повному обсязі віддалена тканину аденоми, залишки капсули аденоми передміхурової залози, що утворюють клапани і порушують пасаж сечі, можна легко ліквідувати під візуальним контролем.
Сучасні інструменти і методика трансуретральной електрорезекції дозволяють проводити видалення пухлин передміхурової залози і сечового міхура. Особливо ефективна трансуретральная електрорезекція шийки сечового міхура при хворобі Маріона - кільцеподібній звуженні, що локалізується в шийці сечового міхура. Розсічення цього кільця за допомогою голчастого електрода і економна резекція шийки сечового міхура дозволяють домогтися достатнього розкриття його шийки [Симонов В. Я. 1978].
5.14. Уретрографія хворого зі стриктурою уретри, a- до операції-б-через 1 міс після уретротомія, стриктура відсутня.
Вибір обсягу резекції передміхурової залози залежить від віку хворого, необхідності зберегти його репродуктивну функцію, а також кількості залишкової сечі і вторинних змін верхніх сечових шляхів. При циркулярної електрорезекції можливий ретроградний закид еякуляту в сечовий міхур. З метою запобігання порушенню еякуляції у хворих з невеликою кількістю залишкової сечі (до 300 мл) доцільно розсікати шийку сечового міхура на 5 і 7 годинах в напрямку від гирла сечоводів до насіннєвому горбку. Аденоми передміхурової залози невеликих розмірів (до 60 г) доцільно видаляти трансуретрально.
Електрорезекція починають з видалення середньої частки аденоми передміхурової залози, що дозволяє в разі виникнення будь-яких ускладнень перервати операцію, а сечовипускання буде проте вже відновлено. При відсутності ускладнень послідовно резецируют праву і ліву частки аденоми. При незначному артеріальній кровотечі не слід виробляти коагуляцію, так як це призводить до втрати часу. Витрати часу збільшуються при зміні петлевидних електрода на коагуляційний кульку. Після резекції кожної частки хірург проводить ретельний гемостаз, коагулює артеріальні і венозні судини. Після закінчення операції через тубус інструменту евакуюють резецированной тканину, а по уретрі проводять триходовий катетер Фолі № 12` 22 за шкалою Шарьера. Балон катетера Фолі наповнюють 20 мл рідини і встановлюють в ложі аденоми. Притисненням судин запобігають можливе кровотеча в післяопераційному періоді. Залежно від кількості вилученої тканини, інтенсивності гематурії, супутніх захворювань у хворого уретральний катетер видаляють через 24-48 ч. Повна епітелізація ложа аденоми передміхурової залози настає через 7-8 тижнів [Лопаткін Н.А. та ін. 1982].
При раку передміхурової залози, що викликає порушення акту сечовипускання і наростання кількості залишкової сечі в сечовому міхурі, для того щоб уникнути надлобкового дренування сечового міхура при відсутності різкого підвищення рівня сечовини і креатиніну в сироватці крові показана трансурстральная електрорезекція передміхурової залози. Техніка резекції відрізняється від такої при аденомі передміхурової залози. Якщо при аденомі хірург прагне до трансуретральной енуклеація аденоматозних вузлів, то при раку втручання зводиться до створення конусовидного тунелю від шийки сечового міхура до зовнішнього сфінктера. Труднощі оперативного втручання полягає в складності візуального визначення меж резекції через можливість проростання пухлиною шийки сечового міхура і задньої уретри. У зв'язку з цим електрорезекція при раку передміхурової залози слід проводити під контролем пальця хірурга, введеного в пряму кишку, або при фарадіческій роздратуванні зовнішнього сфінктера сечового міхура. Загальноприйнята думка щодо мінімального обсягу резекції передміхурової залози, ураженої пухлиною, ми вважаємо недостатньо обґрунтованим.
Слід зазначити, що чим менше залишається нерезецірованной пухлини, тим менше буде потрібно гормональних препаратів для інволюції передміхурової залози. Таким чином, інтервал між електрорезекція залози у хворого на рак, які виробляють з метою відновлення акту сечовипускання, може бути збільшений.
Останнім часом трансуретальную резекцію застосовують в комплексному лікуванні хронічного і гострого простатиту з метою розкриття і дренування гнійних вогнищ передміхурової залози, поліпшення акта сечовипускання, а також видалення каменів з залози.
Одним з методів лікування хворих на рак сечового міхура може бути його трансуретральная електрорезекція. Показанням до її застосування є пухлини в стадії Т1-2. Трансуретральна резекція сечового міхура може бути виконана і з паліативної метою. Це оперативне втручання можна проводити у хворих на рак сечового міхура з вираженими супутніми захворювань і. коли радикальне трансвезікальной втручання не може бути вироблено, а триваюче кровотеча загрожує життю хворого.
Видалення пухлини сечового міхура роблять петлею електрорезектоскопа від верхівки освіти до його основи. На певному етапі настає стадія «уявної сліпоти», промивна рідина стає малопрозорий через домішки крові, що надходить з множинних артерій пухлини.
5.15. Цистоскопія. Трансуретральная електрорезекція аденоми передміхурової залози. Видно насіннєвий горбок.
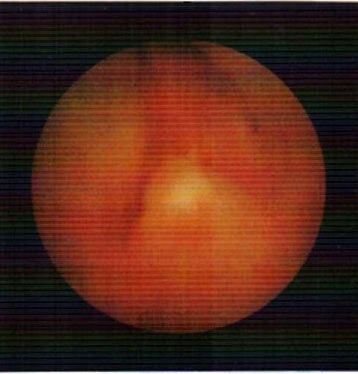
У цей період хірург не повинен втрачати самовладання, продовжувати електрорезекція, сконцентрувавши увагу на об'єкті операції. У міру наближення до основи пухлини кількість судин зменшується і кровотеча стає менш дифузним. Проводять коагуляцію судин. Підстава пухлини резецируют разом з м'язовим шаром сечового міхура і відправляють на гістологічне дослідження для підтвердження радикальності операції. Краї рани і кратероподібне поглиблення в стінці сечового міхура піддають глибокої діатермокоагуляції або ендовезікальной впливу потужного випромінювання ІАГ-лазера з наступними параметрами: довжина хвилі 1060 нм, потужність 30-40 Вт, тривалість імпульсу 1,5-2 с. Січовий що служить показником до цістолітотріпсіі, яку краще проводити в прозорому середовищі.
Цістолітотріпсію виробляють механічним, електрогідравлічним і ультразвуковим способами. Важливим моментом в механічної цістолітотріпсіі є захоплення конкременту і його дроблення на вазі для профілактики поранення стінки сечового міхура. По завершенні цістолітотріпсіі потрібно усунути причину инфравезикальной обструкції, що викликала каменеутворення.
Створення апаратури здатної забезпечувати наднизьку температуру робочого елемента ендоскопа, призвело до утворення нового напрямку в лікуванні захворювань сечового міхура і передміхурової залози - кріохірургії.
5.16. Трансуретральне і трансвезікальной кріодеструктор.
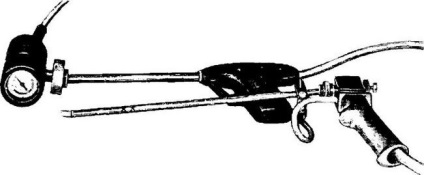
Кріодепузирь дренируют по уретрі катетером на термін від 2 до 8-10 діб. Тривалість дренування залежить від обсягу операції і глибини резекції стінки сечового міхура.
Надалі проводять Цістоскопіческій контроль кожні 3 міс. На місці електрорезекції при відсутності рецидиву визначається білястий безсудинного ділянку з ніжним рубцем.
Порушення пасажу сечі по нижнім сечовим шляхах сприяє каменеутворення в сечовому міхурі, обструкцію проводять в газовому середовищі пацієнтам, яким не можна виконати радикальне оперативне лікування. Кріодеструктор представлені на рис. 5.16.
Трансуретральная хірургія дозволяє лікувати хворих з аномаліями розвитку сечоводів, наприклад уретероцелє. Під час цистоскопії знаходять точкове гирлі уретероцелє і виробляють його розсічення. При виявленні конкрементів їх витягають, піддають дробленню і евакуації. Віддалені результати дозволяють позитивно оцінити цей метод лікування.
Сучасні урологічні ендоскопічні інструменти дають можливість отримувати катетери, дренажні трубки, проведені по сечоводу в сечовий міхур під час операції, і інші сторонні предмети сечового міхура і сечовипускального каналу.
Ендоскопічні методи лікування застосовні при каменях сечоводу і вторинному пієлонефриті. Катетеризація сечоводу вище конкременту відновлює відтік сечі з нирки, сприяє стихання запального процесу в пий. Камені сечоводу можна піддати літотрипсії з використанням ультразвукової енергії і електрогідравлічного розряду (апарат «Байкал»).
При локалізації конкрементів в нижній третині сечоводу можливе його зведення в сечовий міхур за допомогою екстрактора Дорма. У тому випадку, коли конкремент ущемляється в гирлі сечоводу, виробляють розсічення гирла сечоводу протягом 5-8 мм струмами високої частоти за допомогою інструменту, проведеного по другому каналу катетеризаційна цистоскопа.
Можливості застосування цистоскопа і резектоскопа не обмежуються проведенням його по уретрі. Виникають такі ситуації, коли необхідно оглянути сечовий міхур, провівши інструмент по епіцістостоміческому ходу, Епіцістоскопію виробляють при стриктурах уретри і для того щоб виконати циркулярну електрорезекція довго не загоюються надлобкового норицевого ходу.
Ускладнення. Кількість ускладнень трансуретральної хірургії значно менше, ніж при відкритих оперативних втручаннях. Однак ускладнення можливі, про них слід пам'ятати і постійно здійснювати їх профілактику.
Вторинного кровотечі, тампонади сечового міхура і його розриву після операції можна уникнути при ретельній евакуації резецированной тканини фрагментів конкрементів з сечового міхура за допомогою евакуатора Елліка або шприца Жане. Іригація сечового міхура протягом першої доби запобігає утворенню згустків крові і забезпечує хорошу функцію катетера.
Можуть бути різні види травм сечового міхура. Одним з методів лікування цього ускладнення є тривале дренування міхура, що запобігає утворенню сечових затекло і флегмон клітковини малого таза.
Грозним ускладненням трансуретральной хірургії є розвиток гемолізу при тривалих і великих операціях. Він виникає при попаданні в кровоносне русло великої кількості промивної рідини. Гемоліз супроводжується зниженням артеріального тиску, а іноді виникненням ниркової недостатності.
Надійними способами профілактики цього ускладнення є використання негемолизирующих розчинів для іригації (5% розчин глюкози, 0,9% розчин сечовини тощо), підтримка низкою внутріпузирного тиску шляхом періодичного спорожнення сечового міхура. Обсяг промивної рідини не повинен перевищувати фізіологічну ємність сечового міхура. Доцільно застосування припливно аспирационного резектоскопа, а також надлобкового дренування сечового міхура під час операції.
При застосуванні екстракторів типу Дорміа може спричинити серйозне ускладнення. При недотриманні показань до їх застосування (камінь великих розмірів, камінь у верхній третині сечоводу) можуть спостерігатися перфорації або відрив сечоводу, обмеження конкремента з екстрактором в сечоводі з розвитком гострого пієлонефриту. При цих ускладненнях потрібне проведення екстреного оперативного втручання.
Облік показань і протипоказань до екстракції конкременту, використання справного інструментарію і щадне маніпулювання є запорукою успішного застосування ендоскопічних методик для лікування хворих з каменями сечоводу.
Незважаючи на те що ендоскопія розвивається вже понад 100 років, сучасна технологія виробництва ендоскопічної апаратури та інструментів дозволила зробити якісно новий крок в розвитку ендоскопічної хірургії. Останнє п'ятиліття ознаменувало собою такі нові і перспективні методи ендоскопічної хірургії, як уретеропіелоскопія і черезшкірна піелокалікоскопія. Уретероскопія дозволяє зробити діагностичне дослідження сечоводу на всій його довжині і ультразвукову літотрипсії.
Уретероскопія і ультразвукова літотрипсія найбільш легко здійсненна у жінок в зв'язку з анатомічними особливостями будови уретри. Дане оперативне втручання зазвичай виконується під наркозом.
Черезшкірна піелоскопія виконується також під наркозом. Попередньо під контролем електроннооптичного преобразвателя (ЕОП) проводиться (на тлі екскреторної урографії для візуалізації чашечнолоханочной системи) черезшкірна пункція балії з подальшою дилатацією нефростоміческого ходу до розміру, необхідного для проведення нефроскопа. Потім, звичайно через добу, проводиться піелоскопія і ультразвукова літотрипсія конкрементів, що знаходяться в балії і чашечках нирки. За допомогою спеціальних щипців можна витягувати конкременти, що залишилися після піелонефролітотоміі. Є можливість використовувати нефропіелоскоп для електрокоагуляції невеликих пухлинних утворень і зупинки кровотеч.
В даний час ведуться дослідження з використання гнучких лазерних систем для лазерної аплікації пухлин балії і чашок нирок.
Таким чином, прогрес ендоскопії в урології, досягнутий за останнє сторіччя, поява нових інструментів, методів діагностики і лікування дозволили створити новий напрямок у клінічній урології, яке може бути названо трансуретральной хірургією і ендоскопічної урології. Подальше вдосконалення ендоскопічної апаратури та інструментів дозволить якісно поліпшити діагностику і лікування багатьох урологічних захворювань.