Основний метод лікування гострого лейкозу - це хіміотерапія. Вибір схеми хіміотерапії залежить від підтипу лейкозу.
Методи лікування гострих лейкозів у дорослих
Гострий лейкоз у дорослих - це не одне захворювання, а кілька, і хворі з різними підтипами лейкозу неоднаково відповідають на лікування.
Вибір терапії грунтується як на конкретному підтип лейкозу, так і на певних характеристиках хвороби, які називаються прогностичними ознаками. Ці ознаки включають: вік хворого, кількість лейкоцитів, відповідь на хіміотерапію і відомостей про те, чи лікувався раніше цей хворий з приводу іншої пухлини.
Під хіміотерапією мається на увазі застосування препаратів, що знищують пухлинні клітини. Зазвичай протипухлинні препарати призначаються внутрішньовенно або всередину (через рот). Як тільки препарат надходить в кровотік, він розноситься по всьому організму. Хіміотерапія - основний метод лікування гострих лейкозів.
Хіміотерапії гострого лімфобластного лейкозу (ГЛЛ)

Консолідація. Завданням на цьому етапі лікування є знищення тих пухлинних клітин, які залишилися після проведення першого етіпа - індукції.
Підтримуюча терапія. Після проведення перших двох етапів хіміотерапії в організмі ще можуть залишатися лейкозні клітини. На даному етапі лікування призначаються низькі дози хіміопрепаратів протягом двох років.
Лікування ураження центральної нервової системи (ЦНС). У зв'язку з тим, що гострий лімфобластний лейкоз часто поширюється в оболонки головного і спинного мозку, хворим вводяться хіміопрепарати в спинномозковий канал або призначається променева терапія на головний мозок.
Хіміотерапія гострого мієлоїдного лейкозу (ГМЛ)
Лікування ГМЛ складається з двох фаз: індукції ремісії і терапії після досягнення ремісії.
У період першої фази знищується більшість нормальних і лейкозних клітин кісткового мозку. Тривалість цієї фази - зазвичай один тиждень. У цей період і протягом кількох наступних тижнів кількість лейкоцитів буде дуже низьким і тому будуть потрібні заходи проти можливих ускладнень. Якщо в результаті тижневої хіміотерапії ремісія не буде досягнута, то призначаються повторні курси лікування.
Мета другої фази - знищення залишилися лейкозних клітин. Лікування протягом тижня потім супроводжується періодом відновлення кісткового мозку (2-3 тижні), потім курси хіміотерапію тривають ще кілька разів.
Деяким хворим призначають хіміотерапію дуже високими дозами препаратів для знищення всіх клітин кісткового мозку, після чого проводиться трансплантація стовбурових клітин.
Побічні ефекти хіміотерапії
В процесі знищення лейкозних клітин пошкоджуються і нормальні клітини, які поряд з пухлинними клітинами також володіють швидким зростанням ..
Клітини кісткового мозку, слизової оболонки порожнини рота і кишечника, а також волосяних фолікулів відрізняються швидким ростом і тому піддаються впливу хіміопрепаратів. Тому хворі, які отримують хіміотерапію, мають підвищений ризик розвитку інфекції (через низьку кількість лейкоцитів), кровотеч (низька кількість тромбоцитів) і підвищену стомлюваність (низька кількість еритроцитів). До інших побічних ефектів хіміотерапії відносяться: тимчасове облисіння, нудота, блювота і втрата апетиту.
Ці побічні явища зазвичай проходять незабаром після припинення хіміотерапії. Як правило, існують методи боротьби з побічними ефектами. Наприклад, для запобігання нудоти і блювоти разом з хіміотерапією призначаються протиблювотні препарати. Для підвищення кількості лейкоцитів і профілактики інфекції застосовуються фактори росту клітин.
Можна знизити ризик інфекційних ускладнень за рахунок обмеження контакту з мікробами шляхом ретельної обробки рук, вживання в їжу спеціально приготованих фруктів і овочів. Хворі, які лікуються, повинні уникати скупчень людей і хворих з інфекцією.
Під час хіміотерапії хворим можуть призначатися сильні антибіотики для додаткової профілактики інфекції. Антибіотики можуть бути застосовані при перших ознаках інфекції або навіть раніше з метою запобігання інфекції. При зниженні кількості тромбоцитів можливо їх переливання, як і переливання еритроцитів при зниженні і виникненні задишки або підвищеної стомлюваності.
Синдром лізису пухлини - побічний ефект, викликаний швидким розпадом лейкозних клітин. При загибелі пухлинних клітин вони вивільняють в кровотік речовини, що ушкоджують нирки, серце і центральну нервову систему. Призначення хворому великої кількості рідини і спеціальних препаратів допоможе запобігти розвитку важких ускладнень.
У деяких хворих з ГЛЛ після закінчення лікування пізніше можуть виникнути інші види злоякісних пухлин: ГМЛ, неходжкінська лімфома (лімфосаркома) або ін.
Трансплантація стовбурових клітин (ТСК)
Хіміотерапія пошкоджує як пухлинні, так і нормальні клітини. Трансплантація стовбурових клітин дозволяє лікарям використовувати високі дози протипухлинних препаратів з метою підвищення ефективності лікування. І хоча протипухлинні препарати руйнують кістковий мозок хворого, пересаджені стовбурові клітини допомагають відновити клітини кісткового мозку, які продукують клітини крові.
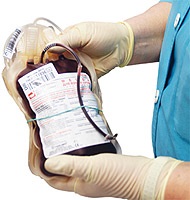
Хворому призначається хіміотерапія дуже високими дозами препаратів для знищення пухлинних клітин. У доповненні до цього проводиться променева терапія для знищення залишилися лейкозних клітин. Після такого лікування збережені стовбурові клітини вводяться хворому у вигляді переливання крові. Поступово пересаджені стовбурові клітини приживляються в кістковому мозку хворого і починають виробляти клітини крові.
Хворим, яким пересаджували донорські клітини, призначаються препарати, що запобігають відторгнення цих клітин, а також інші препарати для профілактики інфекцій. Через 2-3 тижні після трансплантації стовбурових клітин вони починають виробляти лейкоцити, потім тромбоцити, і врешті-решт - еритроцити.
Хворі, яким проведена ТСК, повинні оберігатися від інфекції (перебувати в ізоляції) до необхідного збільшення кількості лейкоцитів. Такі хворі перебувають в лікарні до досягнення кількості лейкоцитів близько 1000 в куб. мм крові. Потім майже кожен день такі хворі спостерігаються в поліклініці протягом декількох тижнів.
Трансплантація стовбурових клітин все ще залишається новим і складним методом лікування. Тому така процедура повинна здійснюватися в спеціалізованих відділеннях зі спеціально навченим персоналом.
Побічні ефекти при трансплантації стовбурових клітин
Побічні ефекти ТСК підрозділяються на ранні та пізні. Ранні побічні ефекти мало відрізняються від ускладнень у хворих, які отримують хіміотерапію високими дозами протипухлинних препаратів. Вони викликані пошкодженням кісткового мозку та інших швидкозростаючих тканин організму.
Побічні явища можуть існувати протягом тривалого часу, інколи роками після перенесеної трансплантації. З пізніх побічних ефектів слід зазначити наступні:
- Променеве ушкодження легенів, що приводить до задишки;
- Реакція "Трансплантат проти господаря" (РТПХ), яка зустрічається тільки при пересадці клітин від донора. Це серйозне ускладнення спостерігається тоді, коли клітини імунної системи донора атакують шкіру, печінку, слизову оболонку порожнини рота і інші органи хворого. При цьому спостерігаються: слабкість, підвищена стомлюваність, сухість у роті, висип, інфекція і м'язові болі;
- Пошкодження яєчників, що приводить до безпліддя і порушення менструального циклу;
- Пошкодження щитовидної залози, що викликає порушення обміну речовин;
- Катаракта (пошкодження кришталика ока);
- Пошкодження кісток; при важких змінах може знадобитися заміщення частини кістки або суглоба.
Променева терапія (використання рентгенівських променів високих енергій) грає обмежену роль при лікуванні хворих на лейкоз.
У дорослих хворих з гострим лейкозом опромінення може бути застосоване при ураженні центральної нервової системи або яєчок. У рідкісних екстрених випадках променева терапія призначається для зняття здавлення трахеї пухлиннимпроцесом. Але навіть і в цьому випадку нерідко замість променевої терапії застосовується хіміотерапія.
При лікуванні хворих на лейкоз, на відміну від інших видів злоякісних пухлин, операція, як правило, не використовується. Лейкоз - хвороба крові і кісткового мозку і її не можна вилікувати хірургічним шляхом.
В процесі лікування хворому на лейкоз за допомогою невеликого оперативного втручання може бути введений катетер у велику вену для введення протипухлинних та інших препаратів, взяття крові для досліджень.
Що відбувається після лікування гострих лейкозів
Після завершення лікування з приводу гострого лейкозу необхідно динамічне спостереження в поліклініці. Таке спостереження дуже важливо, тому що дозволяє лікарю спостерігати за можливим рецидивом (поверненням) хвороби, а також за побічними ефектами терапії. Важливо негайно повідомити лікаря про з'явилися симптоми.
Зазвичай рецидив гострого лейкозу, якщо він буває, виникає під час лікування або незабаром після його закінчення. Рецидив розвивається дуже рідко після ремісії, тривалість якої перевищує п'ять років.