
Даний урок проводиться в 7 класі за підручником Г.Є. Рудзитис 8 клас із застосуванням ІКТ. В методичній розробці представлений план-конспект уроку поглиблення і коригування знань, закріплення практичних умінь і навичок і презентація до нього. Мета: узагальнити і систематизувати знання про хімічні формули, якісний та кількісний склад речовин; розвивати навички вирішення завдань з використанням масової частки елемента в речовині; ознайомитися зі способами знаходження формул речовин за даними про масові частках елемента.
П л а н - к о н с п е к т у р о к а п про
х і м і і в 7 до л а с с е п о т е м е:
«МАСОВА Д О Л Я Е Л Е М Е Н Т А
Тема урока. Масова частка елемента в складній речовині. рішення
Мета уроку: узагальнити і систематизувати знання про хімічні формули,
якісному і кількісному складі речовин; розвивати навички
вирішення завдань з використанням масової частки елемента в речовині; ознайомитися зі способами знаходження формул речовин за даними про масові частках елементів.
Обладнання: періодична система хімічних елементів Д. І. Менделєєва, картки із завданням для фронтальної роботи, алгоритми.
Базові поняття і терміни: відносна формульна і відносна молекулярна маси, масова частка елемента, прості і складні речовини,
Тип уроку: поглиблення і коригування знань, закріплення практичних умінь і навичок.
Методи і прийоми: пояснювально-ілюстративні; практичні. вирішення задач; репродуктивні; частково-пошукові.
І. Організаційний етап
II. Перевірка домашнього завдання
III. Актуалізація опорних знань учнів
IV. Узагальнення і систематизація знань учнів
V. Домашнє завдання
VI. Підведення підсумків уроку
«Уміння вирішувати завдання - це мистецтво, що купується практикою»
1. Організаційний етап
II. Перевірка домашнього завдання.
Для успішного сходження на вершину знань, необхідно мати хорошу підготовку, мати необхідні знання і навички, які потрібні для освоєння матеріалу. Давайте перевіримо, наскільки ми готові до сходження на вершину, до сприйняття нових знань. Якими знаннями ми вже володіємо, і чим нам необхідно опанувати.
Проводиться перевірка виконання письмових домашніх завдань.
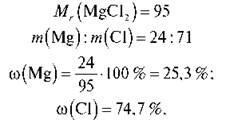
m (Cr). m (O) = 52: 48 = 26:24 = 13: 12
III. Актуалізація опорних знань учнів
Ми поступово починаємо підніматися на вершину знань. Але для такого важкого шляху нам необхідно мати знаряддя, тобто згадати деякі відомості, які знадобляться при вивченні теми.
- Дайте визначення поняття «відносна молекулярна маса». Як її обчислюють?
- Дайте визначення поняття «масова частка елемента в речовині». Як її обчислюють?
- Запишіть формули для обчислення масової частки елемента і маси елемента.
- Які величини необхідно знати для обчислення масової частки елемента за хімічною формулою?
- Як знайти відносну атомну масу?
- За якими даними записують хімічні формули?
IV. Узагальнення і систематизація знань учнів
Перед нами вершина знань. На минулому уроці ми вже освоїли основні прийоми вирішення завдань по формулі речовини, і кожен з вас досяг деяких висот на цій вершині. Дехто знаходиться біля підніжжя гори (середній рівень), хто досяг самого піку - вершини знань. І сьогодні ми повинні піднятися якомога вище, навчитися знаходити масові частки елементів в речовинах, обчислювати маси елементів по їх масовим часткам, знаходити формули речовин за даними про масові частках елементів.
Подивіться на альпініста біля підніжжя гори. Як ви думаєте, йому потрібні зусилля, щоб піднятися на гору? А якщо без зусиль рухатися по горі, то куди можна потрапити? Тому сьогодні на уроці, для того, щоб не скотитися вниз, нам потрібно буде докласти багато зусиль для розв'язання вправ, бути уважними і наполегливими в роботі.
1.Рішення завдань з використанням поняття «масова частка елемента»
1.Запісать скорочена умову задачі. 2. Визначити відносну молекулярну або формульну масу речовини. 3. Визначити масову частку шуканого елемента речовини за формулою. 4.Запісать відповідь.
Для визначення масової частки елемента в з'єднанні користуються формулою:
Де ω% (Е) - масова частка елемента в з'єднанні;
n - кількість атомів елемента в з'єднанні;
Ar (Е) - відносна атомна маса цього елемента;
Mr (речовини) - відносна молекулярна маса даного з'єднання.
Завдання 1. а) .Малахіт - крихкий мінерал зеленого кольору, має формулу СіСО3 (OH) 2. Його вважають російським каменем, слава його почалася з 1635р. - після відкриття уральських малахітових рудників, які зараз повністю вичерпані. Визначте масову частку всіх елементів в цьому з'єднанні.
б) Магнезит має формулу МgСО3. Обчислити масові частки елементів в мінералі.
в) Смарагд - камінь зеленого кольору, формула Be 3 Al2 (SiO3) 6. В смарагдову чашу, за біблійною легендою, зібрали кров Христа. Римський імператор Нерон через смарагдовий монокль спостерігав як горить Рим. Визначте масову частку всіх елементів в цьому з'єднанні.
Завдання 2. а) Бірюза має блакитний колір завдяки наявності в цьому з'єднанні іонів міді. Вона хімічно нестійка: поглинає вологу, вбирає жири, «боїться» сонця, взаємодіє з вуглекислим газом, набуваючи зелений колір. Камінчик масою 208г містить 16г атомів міді. Обчисліть масову частку міді в бірюзі.
б) Рубін, який в Стародавній Індії називали царем дорогоцінних каменів - різновид мінералу корунду (Al 2 O3). Його червоний колір обумовлюють домішки атомів Хрому. Кристал рубіни масою 167г містить 15г атомів Хрому. Обчисліть масову частку Хрому в цьому кристалі.
2. Обчислення відносини мас елементів у складній речовині за його формулою
1.Запісать скорочена умову задачі.
2.Запісать формулу для обчислення масових співвідношень елементів, вказуючи в дужках їхні символи:
m (А). m (В). m (С) = Хм (А). розум (В). Zм (С)
3.Рассчітать масові співвідношення, підставивши відповідні значення в формулу.
Задача1. Знайти масове співвідношення елементів в сульфате алюмінію Al2 (SO4) 3.
Завдання 2. Знайти масове співвідношення елементів в глюкозі З 12 Н 22 О11
3. Обчислення маси елемента за відомою масовою часткою.
1. Записати скорочена умову задачі
2. Визначити відносну молекулярну масу даної речовини
3. Визначити масу елемента за формулою
4. Записати відповідь
Завдання 1. Гематит - напівдорогоцінне каміння від чорного до червоного кольору, відомий ще в Давньому Єгипті. Масова частка Заліза в ньому 0,7. Обчисліть масу Заліза в камінчику масою 50г.
Завдання 2. А) Мінерал сильвин, що має хімічну формулу KCl, використовують як калійне добриво. Обчисліть масу атомів Калію, яка міститься в 50г Сільвіна.
Б) Гірський кришталь - це кристалічний. прозорий, безбарвний кварц з хімічною формулою SiO2. У стародавній Греції вважали, що це скам'яніла кришталева вода, яка зовсім втратила тепло. Яка маса кремнію міститься в кристалі гірського кришталю масою 200г?
4. Обчислення маси речовини за відомою масовою часткою елемента.
Алгоритм 1. Записати скорочена умову задачі
2. Визначити відносну молекулярну або формульну масу речовини
3.Зная масову частку елемента і його масу в речовині, за допомогою пропорції знаходимо масу сполуки.
Завдання 1. Сапфіри синього кольору здавна були «королівськими камінням» - символами мудрості, влади, перемоги. Це різновид корунду з масовою часткою Алюмінію 52,9% і домішками Титана і Заліза. Обчисліть масу кристала сапфіра, в якому міститься 5,4 г атомів Алюмінію.
Завдання 2. Мармур. вапняк, кальцит і крейда є різновидами з'єднання з хімічною формулою СаСО3. Визначити, в якій масі цього з'єднання міститься 120г атомів Карбону.
5.Нахожденіе формул речовин за даними про масові частках елементів.
1.Запісиваем коротко умову задачі.
2.Определяем відносну молекулярну або формульну масу
3. За формулою n = W • Mr / Ar • 100% можна визначити кількість атомів кожного елемента у формулі.
4. Записати відповідь.
Задача1. Мінерал пірит -руда, з якої отримують залізо. Вона містить 47% заліза і 53% сірки. Відносна формульна маса піриту дорівнює 120. Визначте формулу піриту.
Завдання 2.Визначте формулу гематиту - з'єднання заліза з киснем, в якому масова частка заліза 70%.
6. Знаходження формули речовини за масовою співвідношенням елементів.
Записуємо короткий умову задачі.
Записати формулу для обчислення масових співвідношень елементів, вказуючи в дужках їхні символи:
m (А). m (В). m (С) = Х: У. Z,
Перейти до масових співвідношенням, в яких містилося б ціле кількість атомів кожного виду.
Записати формулу речовини.
Завдання 1. Встановити найпростішу формулу речовини, до складу якої входять водень, вуглець, кисень і азот в масових співвідношеннях 1: 3: 4: 7.
Задача2. Масові співвідношення міді, сірки і кисню рівні 2: 1: 2. Вивести формулу речовини.
1.Вичісліть масову частку міді в з'єднанні CuSO4
А) 20; Б) 40; В) 60; Г) 80
2. Масова частка натрію в соді становить 27%. розрахувати масу
атомів натрію в соді масою 20г.
А) 6,8; Б) 8,2; В) 5,4; Г) 3,6
3.Рассчітать масу гірського кришталю, в якому міститься 80г кисню, якщо масова частка кисню в ньому становить 53%.
А) 249; Б) 124,5; В) 150,9; Г) 265,8
4. Вивести формулу пиролюзита, якщо відомо, що в його склад входить марганець і кисень з масовими частками 63% і 37%, а відносна формульна маса дорівнює 87.
1.Рассчітать масову частку алюмінію в поєднанні AlPO4
А) 22, Б) 33, В) 44, Г) 66
2.Массовая частка заліза в Сидерит становить 48%. Розрахувати масу атомів заліза в мінералі масою 200г.
А) 60; Б) 40; В) 96; Г) 20
3.Рассчітать масу кристала мінералу, в якому міститься 30г магнію, якщо масова частка магнію в ньому становить 48%.
А) 67,5; Б) 56,8; В) 62,5; Г) 34,8
4. Встановити формулу кіноварі. якщо відомо, що в його склад входить ртуть і сірка з масовими частками 86% і 14%, а відносна формульна маса дорівнює 233.
Учитель. Кожна речовина має свою, тільки характерну для нього хімічну формулу, яка показує якісний і кількісний склад. За формулою можна дати назву речовини. Крім цього, за формулою знаходять її відносну формульну масу і масову частку елементів у з'єднанні. Для опису речовини за формулою можна використовувати такий план.
Якісний склад речовини (елементи, які його утворюють).
Складне речовина або просте.
Кількісний склад (кількість атомів кожного елемента в формульної одиниці).
Співвідношення атомів різних елементів в речовині.
Відносна формульна маса.
Масова частка елементів у з'єднанні.
Ось ми і на вершині знань. Сьогодні, кожен з вас завоював свою маленьку перемогу. Давайте поставимо свої прапорці на ту висоту знань, якої ми досягли на уроці.
Навчання це робота, яка починається в школі. а закінчується будинку.
Виконати завдання за картками
Знайти і підготувати цікаву інформацію для презентації про коштовні камені (легенди, історичні факти, вплив на здоров'я, долю, талісмани)