Переохолодженням називається явище освіти метастабильного стану рідини, охолодженої нижче температури плавлення відповідної твердої фази. Температура затвердіння може збігатися з температурою плавлення тільки при повільному охолодженні в присутності твердої фази.
Переохолоджена рідина може існувати необмежений час без будь-яких змін, якщо в ній не з'являється «зародок» твердої фази. Необхідною умовою зародження кристала і його зростання з розплаву є переохолодження розплаву. Однак слід відрізняти переохолодження рідини, необхідне для того, щоб кристал ріс, від переохолодження, необхідного для зародження кристалічного центру. Якщо температуру кристалізації ми визначаємо як температуру, при якій починається ріст кристала, що знаходиться в охолоджувальної рідини, то температура, при якій кристалізація, розпочавшись, триватиме, практично не буде відрізнятися від температури кристалізації, важливо лише те, щоб ця температура мала тенденцію до зниження , так як без цієї умови, т. е. точно при температурі кристалізації, кристал буде перебувати в рівновазі з розплавом. Інша працювати з початком кристалізації, т. Е. У відсутності готового зародка або затравки.
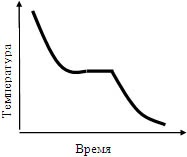
Мал. 1.2. Хід температури при охолодженні розплаву без переохолодження
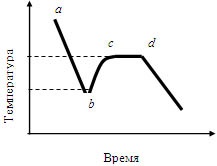
Мал. 1.3. Хід температури при охолодженні розплаву з переохолодженням
З сучасної точки зору рідина при температурі затвердіння ближче підходить до структури кристала, ніж до будови пара. Коли рідина переохолоджена, то вона значною мірою підготовлена до переходу в твердий стан. У ній знаходиться значне число скупчень з орієнтованим розташуванням молекул на зразок кристалічної решітки. Однак ці скупчення знаходяться в нестійкому стані.
Численні дослідження показують, що на граничних твердих поверхнях молекули рідини адсорбуються і утворюють тонкі поверхневі шари з орієнтованими певним чином молекулами рідини. Ці прикордонні шари є не тільки найбільш сприятливими місцями для зародження центрів кристалізації, але є і єдино можливими. Отже, звідси випливає, що для виникнення зародків необхідною умовою є наявність твердої фази і наявність анизотропного шару молекул рідини на цьому кордоні.
Якщо тверда фаза належить тому ж речовини, як і розплав, то кристалізація йде по всій поверхні розділу. Якщо тверда фаза належить до іншої речовини, то кристалізація відбувається тільки в окремих точках. Якщо всередині переохолодженої рідини немає твердої кристалічної фази у вигляді стінок або зважених часток і немає анізотропних шарів, що нагадують за своєю будовою кристали, то рідина взагалі може втратити здатність до переохолодження.
Освіта центрів кристалізації полегшується сторонніми твердими частинками зваженими в розчині або в розплаві. Досліди показують, що затравки, які є центрами кристалізації, можуть служити 1) частки речовини, що кристалізується; 2) частки інших речовин і, ізоморфних з речовини, що кристалізується і утворюють з ним тверді розчини; 3) частки речовин, що дають з речовини, що кристалізується закономірні зростки; 4) частки речовин, які на своїй поверхні адсорбують молекули речовини, що кристалізується.
Так як поверхні твердих тіл ніколи не бувають однорідні, то окремі ділянки мають різну активністю по відношенню до утворення нової фази. Ця активність визначається як фізико-хімічної природою ділянки, так і геометричній його формою і величиною. Слід розрізняти два випадки активує дії поверхні кристала. Поверхні мінералів і інших кристалічних речовин можуть викликати утворення центрів кристалізації, що орієнтує, власної кристалічної решітки. В цьому випадку знову зародився кристал завжди орієнтований певним чином щодо решітки того кристала, на якому він виник. Існує ряд досліджень, які доводять, що в цьому випадку має існувати певне співвідношення між формою і величиною елементарних осередків кристалів.
Нерозчинні домішки відіграють дуже велику роль при кристалізації з розплаву і з розчину. Вони є центрами, навколо яких ростуть кристали. Від кількості цих сторонніх домішок залежить структура злитка, що виходить при затвердінні розплаву. Чим більше домішок, тим більше може бути центрів кристалізації, тим дрібніше структура злитка, т. Е. Тим дрібніше зерна або кристалітів. Механічні властивості чистих металів і сплавів залежать від їх структури. Чим дрібніше структура, тим вище механічні якості металу.
Чи не всякі нерозчинні домішки є центрами кристалізації. Ті домішки, які мають таку ж кристалічну решітку, яку має розплавлене або розчинена речовина, служать надійними центрами кристалізації. Ізоморфні домішки є, перш за все, зародками. Однак кристалізація близько твердої стінки відбувається легше навіть в тому випадку, якщо вона не ізоморфна з розплавленим речовиною. Тому можна очікувати, що більшість домішок впливає на зародження кристалів.