Важливим завданням у створенні будь-якого біотехнологічного процесу є розробка і оптимізація науково-обгрунтованої технології та апаратури для нього.
При організації біотехнологічних виробництв частково був запозичений досвід розвиненою на той час хімічної технології. Однак біотехнологічні процеси мають істотні відмінності від хімічних, оскільки в біотехнології використовують складнішу організацію матерії - біологічну. Кожен біологічний об'єкт (клітка, фермент і т. Д.) - це автономна саморегулююча система. Природа біологічних процесів складна і далеко не з'ясована остаточно. Для мікробних популяцій, наприклад, характерна істотна гетерогенність по ряду ознак - віком, фізіологічної активності, стійкості до впливу несприятливих факторів середовища.
Вони також схильні до випадкових мутацій, частота яких становить 10-4-10-8. Гетерогенність також може бути обумовлена наявністю поверхонь розділу фаз і неоднорідністю середовища.
В основу підрозділу біотехнологічних процесів можуть бути покладені різні принципи, наприклад, оцінка приналежності об'єктів до надцарству живих істот, функціональної активності біооб'єкту, можливості виокремлення окремих етапів з біотехнологічних схем виробництва у вигляді самостійних процесів: виділення, очищення і упаковка готового продукту і т.д. (Табл. 2.1).
Таблиця 2.1. Систематизація біотехнологічних процесів
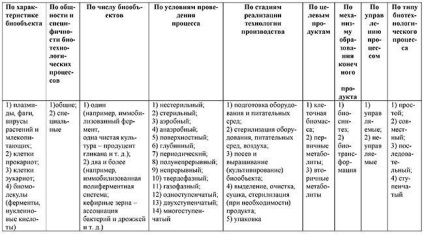
Класифікаційні схеми подібного роду виправдані і ними можна користуватися як рівноправними.
Біотехнологічні процеси умовно можна поділити на біологічні, біохімічні та біоаналогічние. До перших відносять ті з них, які грунтуються на використанні акаріот, прокаріотів і еукаріотів, другі - на використанні ферментів і треті - на хімічному синтезі або напівсинтезу речовин, функціонально близьких або еквівалентних первинним (отримання амінокислот і ін.) Або другорядні метаболіти живих організмів ( отримання похідних пеніциліну і цефалоспорина, тетрацикліну, нуклеїнових підстав і ін.).
У загальному вигляді будь-біотехнологічний процес включає 3 основні стадії: предферментаціонную, ферментаційне і постферментаціонную. Принципова схема реалізації біотехнологічних процесів в загальному вигляді може бути представлена схемою, в якій зроблено спробу відбити всі варіанти ферментативних процесів (рис. 2.1).
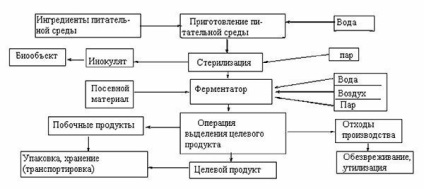
Мал. 2.1. Узагальнена схема процесів в біотехнології
Предферментаціонная стадія
На цій стадії здійснюється зберігання і підготовка культури продуцента (інокулята), підготовка і отримання поживних субстратів і середовищ, ферментаційної апаратури, технологічних і реціркуліруемих води і повітря.
Компоненти поживних середовищ підбирають на підставі розрахунку матеріального балансу, пов'язаного з трансформацією того чи іншого джерела живлення в клітинну біомасу і / або метаболіт при обліку витрачається (виділяється) енергії. Зазвичай якісний і кількісний склад поживних середовищ зазначений в регламентної документації.
Підтримка і підготовка чистої культури є дуже важливим моментом предферментаціонной стадії для отримання цільових продуктів: найчастіше це біомаса мікроорганізмів - продуцентів. Такими є бактерії і нижчі гриби, проте іноді в якості продуцентів можуть виступати клітини вищих еукаріот (комах, ссавців, рослин).
Продуцент, його фізіологобіохіміческіе характеристики і властивості визначають ефективність всього біотехнологічного процесу. У відділенні чистої культури здійснюють зберігання виробничих штамів і забезпечують їх реактивацію і напрацювання продуцента в кількостях, необхідних для початку процесу.
Промисловий штам в ідеалі повинен відповідати таким основним вимогам:
1) стабільності структурно-морфологічних ознак і фізіологічної активності і експлуатації у виробництві;
2) підвищеній швидкості росту і біосинтезу цільового (-их) продукту (ів);
3) досить широкому діапазону стійкості до впливу несприятливих зовнішніх чинників (коливання температури, рН, перемішування, в'язкості середовища);
4) помірної вимогливості до обмеженого числа джерел живлення; ніж ширший набір джерел вуглецю, азоту та інших елементів може використовувати виробничий штам, тим легше його культивувати, і з більшою вигодою.
При вирощуванні посівних доз інокулята застосовують принцип масштабування, т. Е. Проводять послідовне нарощування біомаси продуцента в колбах, бутлях, далі в серії послідовних ферментаторів. Кожен наступний етап даного процесу відрізняється за обсягом від попереднього зазвичай на порядок. Отриманий продуцент по стерильною посівної лінії направляється далі в апарат, в якому реалізується ферментаційна стадія.
Приготування поживних середовищ здійснюється в спеціальних реакторах, обладнаних мішалками. Залежно від розчинності і сумісності компонентів середовищ можуть бути застосовані окремі реактори. Технологія приготування середовищ значно ускладнюється, якщо в їх склад входять нерозчинні компоненти. У різних біотехнологічних процесах застосовуються різні за походженням і кількостей субстрати, тому процес їх приготування варіюють.
Дозування поживних компонентів підбирається і здійснюється індивідуально на кожному виробництві відповідно до технологічного регламенту конкретного процесу. Як дозуючого обладнання при цьому застосовуються вагові і об'ємні пристрої, що використовуються в харчовій і хімічній промисловості. Транспорт речовин здійснюється насосами, стрічковими і шнековими транспортерами. Сипучі компоненти подають в ферментатори за допомогою вакуумних насосів.
Часто застосовують принцип попередніх сумішей, тобто солі попередньо розчиняють і потім транспортують по трубопроводах, дозуючи їх подачу за обсягом.
В силу виняткового різноманітності біотехнологічних процесів і застосовуваних для їх реалізації середовищ, методів і апаратури, розгляд даних елементів далі буде пов'язано з конкретними біотехнологічними виробництвами.
ферментація
Стадія ферментації є основною стадією в біотехнологічному процесі, так як в її ході відбувається взаємодія продуцента з субстратом і утворення цільових продуктів. Ця стадія здійснюється в біохімічному реакторі (ферментаторі) і може бути організована різними способами в залежності від особливостей використовуваного продуцента і вимог до типу і якості кінцевого продукту.
Ферментація може відбуватися в строго асептичних умовах або без дотримання правил стерильності (так звана «незахищена» ферментація); на рідких і твердих середовищах, анаеробно і аеробно. Аеробна ферментація може протікати, в свою чергу, поверхнево або глибинно (у всій товщі живильного середовища). Культивування біологічних об'єктів може здійснюватися в періодичному і проточному режимах, напівбезперервна з підживленням субстратом.
В ході періодичної ферментації вирощується культура проходить ряд послідовних стадій: лаг-фазу, експонентну, уповільнення росту, стаціонарну і відмирання (рис. 2.2). При цьому відбуваються істотні зміни фізіологічного стану біооб'єкту, а також ряду параметрів середовища.
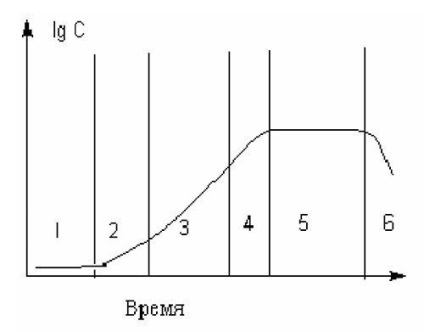
Мал. 2.2. Крива зростання мікроорганізмів в ході періодичної ферментації: 1 - лаг-фаза; 2 - фаза експоненціального зростання; 3 - фаза лінійного зростання; 4 - фаза уповільнення зростання; 5 - стаціонарна фаза; 6 - фаза відмирання
Цільові продукти утворюються в експоненційної (первинні метаболіти - ферменти, амінокислоти, вітаміни, т. Е. Речовини, які потрібні для росту культури клітин) і стаціонарної (вторинні метаболіти - антибіотики, алкалоїди, гормони, токсини - низькомолекулярні речовини, не є необхідною умовою для зростання культури , але необхідні для функціонування зрілої популяції, часто виконують захисну функцію) фазах, тому в залежності від цілей біотехнологічного процесу в сучасних промислових процесах застосовують принцип диференціювання режимів культивування. В результаті цього створюються умови для максимального виробництва того чи іншого цільового продукту.
Безперервна ферментація біооб'єктів здійснюється в умовах сталого режиму, коли мікробна популяція і її продукти найбільш однорідні, т. Е. В стаціонарній фазі. Застосування безперервних процесів ферментації створює умови для ефективного регулювання та управління процесами біосинтезу. Системи безперервної ферментації можуть бути організовані за принципом повного витіснення або повного змішання.
Перший приклад - так звана тубулярная культура: процес ферментації здійснюється в довгій трубі, в яку з одного кінця безперервно надходять живильне середовище і інокулят, а з іншого - з тією ж швидкістю витікає культуральна рідина і цільові продукти. Дана система проточної ферментації є гетерогенною і реалізується, як правило, без перемішування.
При безперервної ферментації в ферментаторах повного змішання (гомогенно-проточний спосіб) у всій масі ферментаційного апарату створюються однакові умови. Застосування таких систем ферментації дозволяє ефективно управляти окремими стадіями, а також всім біотехнологічним процесом і стабілізувати продуцент в практично будь-якому необхідному експериментатору або біотехнології стані.
Забезпечення процесу ферментації з точки зору інженерної реалізації зводиться до дозованому надходженню в ферментатор потоків (інокулята, повітря або газових сумішей, поживних біогенних елементів, піногасники) і відведення з нього тепла, відпрацьованого повітря, культуральної рідини, а також до вимірювання та стабілізації основних параметрів процесу на рівні, необхідному для оптимального розвитку продуцента і освіти цільового продукту.
В ході ферментації утворюються складні суміші, що містять клітини, позаклітинні метаболіти, залишкові концентрації вихідного субстрату. При цьому цільові продукти, як правило, знаходяться в цій суміші в невеликих концентраціях, а багато хто з них легко руйнуються. Все це накладає обмеження на методи виділення та висушування біологічних препаратів.
Л.В. Тимощенко, М.В. Чубик