Хімія і хімічна технологія
Методом низькотемпературного фракціонування суміш розділяють на етан, етилен, пропан, пропілен і паливний газ. Етан і пропан піддають подальшому крекінгу в трубчастих печах в присутності водяної пари для отримання етилену і пропилену. Після компресії і охолодження гази знову направляють на установку для поділу газів. Ацетилен видаляється шляхом каталітичного гідрування або із загальної кількості нефтезаводского газу. або тільки з етиленової фракції. Поділ пропану і пропілену здійснюється дистиляцією або, якщо це доцільно, проведенням з сумішшю ряду реакцій. Вартість установки для виробництва 90 ТОВ т етилену і 43 ТОВ т пропілену з нефтезаводского газів становить 9,9 млн. Доларів, ціна 1 фунта етилену і пропилену 0,0241 долара. [C.9]
Збільшення обсягів при п протоці газоподібних парафінових вуглеводнів. Якщо пропан в процесі піролізу па 100% перетворюється в метан і етилен або в пропен і водень, то обсяг газу при цьому збільшується вдвічі. З 100 л пропану утворюється 200 л продуктів реакції. Звідси випливає, що незалежно від того, яке питоме значення реакцій крекінгу і дегідрування, завжди утворюється подвійний обсяг продуктів реакції порівняно з вихідним. Отр 50% -ному перетворенні пропану з 100 л пропану утворюється 150 л продуктів реакції. [C.51]
Такі повні дані до сих пір вдалося отримати тільки для небагатьох вуглеводнів. До i їм належать ацетилен, метилацетилен, диметил- ацетилен, метан, етилен, аллен, пропав, циклопропан і бензол. [C.301]
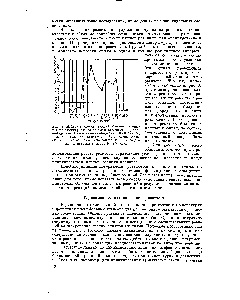
Давно відомий метод автотермічний дегідрірованія етану в етилен (рис. 12) вдосконалений в даний час для дегідрірованія природних газів [93]. У реакторі з керамічної футеровкой теплоносієм є порцелянові кульки. Газова суміш з етану і пропану вводиться в реактор разом з чистим киснем і спалюється не до кінця при 850-900 ° С. Тиск 0,6 кгс / см2, час контакту 1с. При цьому виходять такі продукти етилен. пропілен, метан, окис і двоокис вуглецю. [C.35]
Високотемпературне (450-700 ° С) хлорування низькомолекулярних аліфатичних вуглеводнів. головним чином метану, етану, пропану, бутану, ізобутану, етилену і пропилену, а також їх хлорпроізводіих, проходить вже не як чиста реакція заміщення, а здебільшого як розщеплює і будує крекінг. У разі метану переважає з'єднання уламків j з утворенням іерхлоретілена, в разі пропаном і пропілену - розщеплення з утворенням чотирихлористого вуглецю та іерхлоретілена, в разі етапів і етилену в залежності від умов реакції можуть виходити різні продукти [183-186]. [C.201]
Питомий значення протікають одночасно реакцій крекінгу а дегідрірованія залежить в першу чергу від числа атомів С в вихідному матеріалі. У той час як етан при високому нагріванні перетворюється практик но тільки в етилен і водень і, отже, тут в основному йде реакція термічного дегідрірованія, при нагріванні пропану вже більше значення має реакція крекінгу з утворенням етилену і метану. При нагріванні бутану до високої температури утворюється зовсім небагато бутена. Бутан розщеплюється головним чином на етилен і етан або, відповідно на Проню і метан. Ізобутан, навпаки, приблизно на 50% перетворюється в ізобутіл. [C.47]
Велику роль відіграє дегидрирование. етану і бутану в етилен і бутнлен. Дегидрирование пропану в промисловому масштабі здійснюється незначно, так як пропілен, що утворюється спільно з іншими вуглеводнями прн інших процесах. зокрема при піролізі, повністю покриває потребу в даному продукті в більшості промислових країн. Тому термічне і каталітичне дегідрування пропану описується коротко. Правда, пропилен, одержуваний шляхом каталітичного дегідрування пропану, дешевше утворюється при піролізі. [C.10]
Пента-1 (а-амилен. Або пропив-етилен). СНз- Hj-СНа-СН = СНД -165,2 -1-30,0 1,3715 0,6405 [c.366]
Умови проведення піролізу визначаються двома факторами. По-перше, при піролізі пропану етилен виходить по реакції розщеплення (відщеплення метану), а при піролізі етану -по реакції дегідрування. протікає з великими труднощами. При дегидрировании для досягнення тієї ж ступеня превраш, ення потрібна вища температура, тобто при даній температурі швидкість піролізу пропану буде у багато разів перевищувати швидкість піролізу етану. Як видно з даних, наведених в табл. 26, в одному з дослідів (див. Стовпець 4), вихідний газ складався з 75% пропану і 25% етану, а надходила в піч піролізу робоча суміш. включала рециркулюючий газ, містила приблизно рівні обсяги етану і пропану. Здається, піроліз проводили в умовах, при яких етан розкладався, але не відбувалося його накопичення в робочій суміші, що надходить в змійовики. [C.104]
СНЗ-СНД-СНД-СН = = СНД а-Амі- льон Пентен-) я-Пропил-етилен -138,0 29,9 0,6405 [c.245]
Було показано, що ацетилен при піролізі пропану виходить в результаті розщеплення первинного продукту реакції - етилену і, можливо, пропілену. Звісно ж імовірним, що перед освітою ацетилену пропілен також розкладається на етилен і метан. [C.87]
За старою номенклатурою тут, як і в граничному ряді. все більш складні вуглеводні розглядаються як похідні найпростішого - етилену, одержувані з нього заміщенням одного, двох або всіх чотирьох атомів водню різними радикалами. Так, пропилен по цій номенклатурі отримує назву метил етил, бутилен (I) - етил-етилену, бутилен (II) - диметил-етилену симметрического заміщення, бутилен (III), зазвичай носить нераціональне назву изобутилена, тут отримує назву несиметричного диметил-етилену . Для амиленом отримуємо назви пропив-етилен (I) i метил-етил-етилен симетричний (II), метил-етил-етилен несиметричні (Ш), трима-тил-етилен (IV) і ізопропіл-етилен (V). При більш складних вуглеводнях і тут, як в граничному ряді. назви виходять вже мало зручними, тому що доводиться відзначати складні радикали, які можуть в свою чергу існувати в кількості декількох ізо.черних форм. Тому і тут виходом зі скрути є женевська номенклатура. З цієї номенклатурі загальні назви, що характеризують тільки склад, виробляються від назв насичених вуглеводнів. змінюючи закінчення ан нема на Ілен, а на ен і, таким чином. маємо gH - етен, gHg- пропен, 4Hg - бутен, H q - Пента і т. д. Назва компанії залишається для всіх нормально побудованих ізомерів. Щоб визначити положення подвійного зв'язку. вуглецеві атоми перенумеровуються і вказують на цифру вуглецевого атома. у якого вона починається. Так, для бутен, QHg, маємо [c.44]
Детально досліджувався також радіаційне і термічне а лкілі-вання пропану етиленом в паровій фазі. так як в цій простій системі протікає термічна реакція. швидкість якої досить велика для можливості порівняння продуктів, що утворюються при термічному і радіаційному алкилировании. [C.129]
Для пояснення будь-яких реакцій, що протікають в паровій фазі. необхідно знати хоча б наближено, чи є реакція дійсно гомогенної або частково протікає і на поверхні. Тому в реакції алкілування пропану етиленом вивчали роль поверхонь. змінюючи відношення поверхню обсяг в дуже широких межах (від 5,40 до 36 ТОВ см). Досліди проводили в реакторі періодичної дії. застосовуючи в якості насадки тонку фольгу з нержавіючої сталі. Було встановлено, що продукти радіаційного алкилирования залишалися незмінними у всіх досліджуваних інтервалі відносини поверхню обсяг. хоча ступінь перетворення пропану кілька збільшувалася (табл. 5). Отже, при високих відносинах поверхню обсяг поверхню дійсно грає невелику, але все ж помітну роль в протіканні реакції. Однак з точки зору порівняння термічного та радіаційного алкилирования реакцію, здійснювану в безнасадоч-них реакторах, можна розглядати як гомогенну (табл. 5). [C.130]

S hneider і Froli h показали, що ступінь, до якої йдуть реакції деметанізаціі і дегидрогенизации при піролізі пропану (при 725 ° і атмосферному тиску в кварцових трубках) практично одна і та ж для будь-якого процентного розкладання пропану від "Про до 40%. При некаталітичні піролізі пропану. етилен завжди виходить у великих кількостях. чим пpoiпілeн, навіть при малому часу контактування, коли розкладається тільки невелика кількість пропану. [c.145]
Отримання 1,1,1-тринітро-3- (трінітрометілмеркур) пропану [159]. У водний розчин ртутної солі трінітрометана (10 г в 50 мл води), поміщений в циліндр, пропускають при кімнатній температурі струм етилену. Через 15-20 хв. після початку реакції випадає осад 1,1,1-тринітро-3- (трінітрометілмеркур) пропану. Етилен пропускають в цілому 6 год. відфільтровують осад через кожні 2 години. Потім реакційну суміш залишають стояти 12 год. протягом яких випадає ще кілька продукту. Кожну порцію відфільтрованого осаду промивають 2-3 рази водою і висушують на повітрі. Загальний вихід 9,8 г (93%). Т. пл. 167 ° С (з розкладанням) при повільній кристалізації з води. [C.132]
Відомі й інші варіанти перхлорірованія пропілену або пропану. Наприклад, при перхлорірованіі в киплячому шарі в якості розріджувачів пропонуються гексахлоретан, чотирихлористий вуглець і перхлоретілен [197], в якості гартівних засобів (охолоджувачів) придатні чотирихлористий вуглець і хлористий етилен. В останньому випадку виходить особливо високий вихід 55,8% чотирихлористого вуглецю. 44% перхлоретілена і всього 0,2% побічних продуктів [198]. [C.203]
У міру збільшення швидкості реакції від мінімального її значення частка вуглеводнів, перетвореного в кисневі сполуки. продовжує зменшуватися, а частка вуглеводнів, що перетворювався в олефіни, відповідно збільшуватися. Швидко зростає утворення етилену л, приблизно, при 500 ° С реакція стає в основному сенсибілізованим киснем крекингом пропану. Шульц [55] знайшов, що ставлення пропілену до етилену в даному інтервалі температур узгоджується з передбаченим теорією Райса-Косякова для крекінгу вуглеводнів. [C.331]
З причини того, що вільні радикали в протилежність іонів Карбонія здатні в умовах алкілування віднімати водень як від нормальних, так і від розгалужених парафінових вуглеводнів. термічного алкілування (але не каталитическому) можуть легко піддаватися пропан і інші н-алкани. Так, при алкилировании пропану з етиленом виходить суміш н-і ізопентанів, що утворюються в результаті приєднання радикалів до- та Ізопропілов до етилену [16]. [C.232]