Вода в природі рідко буває чистою і дистильованої, вона містить розчинені солі, поживні речовини і т. Д. Концентрація яких залежить від місцевих умов. Риби і рослини розвивалися протягом мільйонів років в конкретних умовах і можуть просто не вижити в воді, яка істотно відрізняється за хімічним складом від водойми їх звичного місця проживання.
Акваріумісти вважають за краще утримувати рибок, які можуть жити у звичайній водопровідній воді. Досвідчені і акваріумісти можуть змінювати характеристики води відповідно до потреб риб, хоча зробити це майже завжди важче, ніж здається на перший погляд. У будь-якому випадку, ви повинні знати досить про хімічний склад води, щоб вода в акваріумі відповідала потребам риб, яких ви тримаєте.
Вода має чотири вимірюваних властивості, які зазвичай використовуються, щоб характеризувати її хімічний склад. це:
- Міра кислотності води (рН).
- Карбонатна жорсткість (буферна ємність, kH)
- Загальна жорсткість (gH)
- Мінеральний склад води.
рН - Міра кислотності води
рН є мірою співвідношення вільних іонів водню (H +) і вільних іонів гідроксиду (OH) в воді. Вимірюється за шкалою від 0 до 14. p Н = 7 вважається нейтральною, рН нижче 7 - кислому і рН вище 7 - основний або лужної.
Для початківців хіміків рівняння виглядає наступним чином:
Подібно шкалою Ріхтера для вимірювання сили землетрусів, шкала рН є логарифмічною. Іншими словами, вода з рН = 6,0 в 10 разів більше кисла, ніж вода з рН = 7,0 і рН = 5,0 в 100 разів більше кисла, ніж рН = 7.0.
Для акваріумістів важливі два аспекти рН. По-перше, швидка зміна рН викликає стрес для риб, і його слід уникати. Зміна рН на більш ніж 0,3 пункту в день може викликати у риб стрес. Таким чином, рН вашого акваріума потрібно підтримувати постійним і стабільним протягом тривалого часу. По-друге, риби пристосувалися жити у воді певного (іноді вузького) значення рН. Значить, ви повинні бути впевнені, що рН в вашому акваріумі відповідає умови утримання тих риб, яких ви тримаєте.
Коли pH падає через збільшення концентрації кислот (наприклад підвищення концентрації нітритів [NO2] і нітратів [NO3]), карбонати і бікарбонати реагують з кислотами і «нейтралізують» їх. При цьому лужність води (kH) знижується. Якщо у воді все більше і більше кислоти (нітратів), то лужність все нижче і нижче, і врешті-решт більше не зможе буферізіровать (зберігати) pH. Коли лужність сильно впала, тобто вичерпався буфер kH, pH різко падає.
Так як кислота, якої є нітрат, - кінцевий продукт азотного циклу, це пояснює, чому в акваріумі з часом рівень нітратів підвищується, а рівень pH знижується.
Оптимальним рівнем pH в акваріумі з рослинами вважається 6,8-7,2.
У м'якій воді з низьким pH = 6,0 приблизно 80% двоокису вуглецю буде знаходиться в формі CO2 або у вигляді вугільної кислоти [H2CO3], і тільки 20% у вигляді гідрокарбонату. При pH = 7.0 переважає бікарбонат HCO3-. Відповідно, чим нижче pH, тим більше CO2 знаходиться в легко доступною для рослин формі.
При підвищенні pH з нормальних 7,0 до 8,0 менш токсичний амоній [NH4 +] переходить в форму високотоксичного аміаку [NH3] - його частка збільшується з 0,5% до 5% - в 6 разів.
Більшість риб може пристосуватися до рН, трохи відрізняється від оптимального діапазону. Якщо рН вашої води знаходиться в межах від 6,5 до 7,5, ви зможете утримувати більшість видів риб без будь-яких проблем. Якщо рН в межах цього діапазону, то немає необхідності його коригувати.
Таблиця кислотності води (рН)
kH - буферна ємність (карбонатна жорсткість, лужність)
Карбонатна жорсткість, виражена в градусах жорсткості (k H). вимірює кількість карбонатів і бікарбонатів в воді. Насправді k H вимірюється не жорсткість, а лужність води (буферна ємність - здатність нейтралізувати кислоти).
Буферна ємність відноситься до здатності води зберігати стабільний рН при додаванні кислоти або лугу. рН і буферна ємність тісто пов'язані один з одним. Якщо вода має достатній потенціал буферизації, буферна ємність може поглинути і нейтралізувати кислоти без істотної зміни рН. Концептуально буфер діє на зразок великої губки. «Потужність» губки, проте, обмежена - як тільки буферна ємність витрачається, рН при додаванні кислоти змінюється швидшими темпами.
Буферизація має як позитивні, так і негативні сторони. З одного боку, без буферизації рН в акваріумі буде падати з плином часу - це погано. З достатньою буферизацией рН залишається стабільним - це добре. З іншого боку, жорстка водопровідна вода майже завжди має велику буферну ємність. Якщо рН води занадто високий для риб, буферна ємність ускладнює зниження рН до більш відповідного значення.
Яка буферна ємність необхідна вашому акваріуму? Чим більше значення k H, тим вода більш стійка до змін рН. Рівень k H повинен бути досить високим, щоб запобігти різким коливанням рН в акваріумі з плином часу. Якщо k H нижче 4,5 d Н, ви повинні звернути особливу увагу на рН в акваріумі. Це особливо важливо, якщо ви не часто міняєте воду в акваріумі. В круговороті азоту існує тенденцію до зменшення значення рН з часом. Зміна рН залежить від кількості і швидкості виробництва нітратів, а також k H. Якщо рН падає більш ніж 0,5 пункту протягом місяця, ви повинні подумати про збільшення k H або проводити часткову заміну води частіше.
Примітка: не рекомендується використовувати в акваріумі дистильовану воду. За визначенням, дистильована вода практично не має буферної ємності. Це означає, що додавання навіть трохи кислоти значно змінить рН.
gH - загальна жорсткість
Загальна жорсткість (GH) - це загальна кількість іонів магнію (Mg +) і кальцію (Ca +) в воді. «Жорстка» вода часто надходить з водоносних горизонтів, що проходять у вапняку. Вапняк містить карбонат кальцію, який при розчиненні у воді збільшує значення як g H (від кальцію), так і k H (від карбонату). Збільшення значення k H також зазвичай збільшує рН.
Жорсткість води вимірюється в таких одиницях. Термін d Н позначає «градус жорсткості», а ppm означає «частина на мільйон», що приблизно еквівалентно мг / л у воді. 1 градус d Н дорівнює 17,8 ppm CaCO 3. Більшість тестів показують жорсткість в градусах CaCO3; і це означає, що жорсткість еквівалентна кількості CaCO3 в воді, але це не означає, що фактично така кількість CaCO3 міститься у воді. .
Таблиця загальної жорсткості води
Солоність води - загальна кількість розчинених у ній речовин. Солоність розраховувати як сума компонентів kH і gH. а також інших речовин, зокрема, натрій. Значення солоності води важливо для морських акваріумів. У прісноводних акваріумах досить знати значення рН, kH і gH.
Деякі прісноводні риби легко переносять (або навіть відчувають себе краще) невелика кількість солі у воді. Крім того, паразити (наприклад, іхтіофтіріус) не переносять сіль взагалі. Таким чином, додавання солі в концентрації до 1 столової ложки на 5 літрів може реально допомогти запобігти і вилікувати риб від іхтіофтіріусов та інших паразитарних інфекцій.
З іншого боку, деякі види риб не переносять сіль. Все бесчешуйчатих риби, а також деякі соми, наприклад, роду Corydoras, набагато більш чутливі до солі, ніж більшість прісноводних риб. Додавайте сіль, тільки якщо ви впевнені, що це не завдасть шкоди мешканцям акваріума.
Живильні речовини і мікроелементи
Водопровідна вода містить поживні речовини і мікроелементи в дуже низьких концентраціях. Наявність (або відсутність) мікроелементів може бути важливо в деяких ситуаціях.
Найбільш поширені мікроелементи:
Вуглекислий газ (CO2)
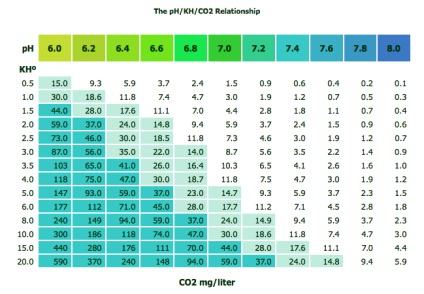
Вуглекислий газ не також є невід'ємною частиною хімічного складу води. CO2 присутній у воді в набагато більшій кількості, ніж кисень і азот разом узяті (70: 2: 1). Часто акваріумісти використовують установки CO2. щоб збільшити темпи росту рослин. Але вуглекислий газ безпосередньо пов'язаний з рівнем k Н і рН. Коли вуглекислий газ розчиняється в воді, в акваріумі збільшується кількість кислоти і знижується значення рН. Кількість присутніх в воді карбонатів (k H) буде визначати, наскільки падає рівень рН.
Співвідношення значень рН, k Н і CO2