ФГБУ Російський науковий центр хірургії ім. Б. В. Петровського
Історія питання та огляд існуючих методик
Ендоскопічні технології налічують більш ніж 200 річну історію. Творцем першого ендоскопа вважається P.Bozzini, який в 1806р. сконструював прилад "Lichtleiter" [1]. Вперше в клінічній практиці був використаний ендоскоп французького хірурга A.J.Desormeaux. Першу торакоскопію в 1910 році виконав професор Каролінського університету H.Jacobeus [2]. За допомогою урологічного цистоскопа, він справив візуальну ревізію плевральної порожнини у хворого на туберкульоз. Цю операцію прийнято вважати точкою відліку історії торакоскопічної хірургії. У 1925р. професор П.А. Герцен виконав першу в Радянському Союзі торакоскопію з приводу емпієми плеври.
Удосконалення інструментів і поява гнучких ендоскопів, а також талант і ентузіазм окремих хірургів дозволив відмовитися від мінідоступу і виконувати всі етапи операції, використовуючи тільки спеціальні ендоскопічні інструменти. При цьому візуальний контроль здійснюється тільки через монітор, а кількість робочих портів коливається від 3 до 5, при цьому максимальна довжина розрізу становить 25мм [10]. Видалити резецированной частина легкого або пухлина середостіння можна розширивши цей розріз до 3-3.5см і помістивши віддалену частку в спеціальний герметичний контейнер.
Прагнення максимально зменшити хірургічну травму призвело до зменшення кількості використовуваних портів до одного. З'явилася методика оперування через один порт або єдиний доступ, розміром до 5 см [34]. При таких операціях через єдиний порт вводяться спеціальні довгі вигнуті артикуляційні інструменти, що дозволяє використовувати до 3-4 інструментів одночасно [34-36]. Слід зазначити, що виконання лобектомія через один порт представляє значні складності, а по травматичності такі операції не суттєво відрізняються від повністю закритих, оскільки вся різниця полягає в відсутності кількох додаткових портів діаметром, від 3 до 5 мм. Осі робочих інструментів практично паралельні осі камери, що також ускладнює роботу.
Основні принципи виконання торакоскопічних анатомічних резекцій легенів з приводу раку
Одними з найбільш складних торакоскопічних втручань є анатомічні резекції легенів різного об'єму. Злоякісні пухлини легень характеризуються високим потенціалом лімфогенного метастазування. Тому операція повинна супроводжуватися не тільки видаленням ураженого органу або його частини, але і широким видаленням медиастинальной клітковини з лімфатичними вузлами - медиастинальной лімфодіссекціей. Термін "лімфодіссекція" видається більш точним, ніж термін "лімфаденектомія" оскільки відображає суть цього етапу, а саме видалення єдиним блоком клітковини, лімфатичних вузлів і судин, а в ряді випадків і нервових сплетінь. Слід підкреслити, що прагнення зменшити хірургічну травму не повинно превалювати над онкологічним радикалізмом. Іншими словами, обсяг торакоскопічної операції повинен бути повністю можна порівняти з традиційним втручанням, як за обсягом резекції легкого, так і за якістю виконуваної медиастинальной лімфодіссекціі.
Ми вважаємо за краще користуватися повністю ендоскопічної технікою при виконанні торакоскопічних втручань. Операція виконується в положенні хворого на боці за методикою 4-х портового доступу (3 порту по 5мм і один 25мм). Рис.1.
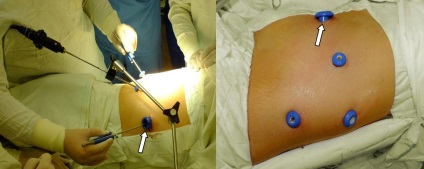
Рис.1 Розташування портів під час торакоскопічної верхньої лобектомія справа. Найбільший порт 25мм розташований в V міжребер'ї по среднеключичной лінії. (Вказано стрілкою)
Використовуємо камеру Olympus LTF 5мм, тримач для камери і набір торакоскопічних інструментів, розроблений профессорм D.Gossot (Delacroix-Chevalier, Paris, France). Мініторакотомія не виконує. Контроль за діями хірурга здійснюється через 2 монітори, які розташовані по обидва боки від операційного столу. Основні етапи видалення частки представлені на малюнку 2.
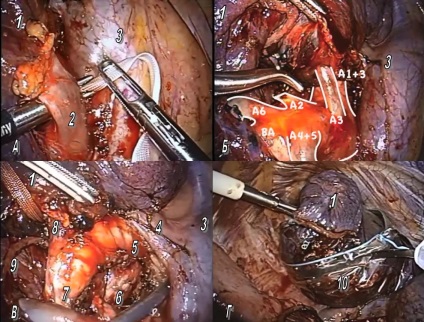
Рис.2 А - виділення верхнедолевой гілки верхньої легеневої вени; Б - лімфодіссекція в корені легені, виділені сегментарні гілки правої легеневої артерії; В - виділення правого верхнедолевого бронха в єдиному блоці з лімфовузлами кореня частки; Г - видалення резецированной частини легкого в контейнері. 1 - верхня частка правої легені, 2 - верхнедолевая вена, 3 - проекція верхньої порожнистої вени, 4 - дуга непарної вени, 5 - правий головний бронх, 6 - лівий головний бронх, 7 - проміжний бронх, 8 - верхнедолевой бронх з лімфатичними вузлами, 9 - нижня частка правої легені, 10 - контейнер.
Найбільш складні етапи медиастинальной лімфодіссекціі при виконанні операції справа представлені на малюнках 3 і 4.
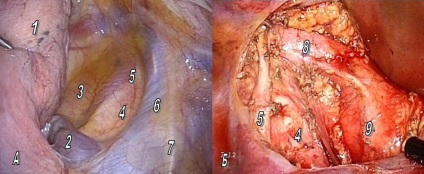
Рис.3 А - праве паратрахеальние простір з лімфатичними вузлами 2R і 4R групи: 1 - верхня частка правої легені; 2 - дуга непарної вени; 3 - стравохід; 4 - трахея; 5 - правий блукаючий нерв; 6 - верхня порожниста вена; 7 - правий діафрагмальний нерв; Б - вид операційного поля після виконання торакоскопічної паратрахеальние лімфодіссекціі: 8 - плечоголовний артеріальний стовбур; 9 - дуга аорти.
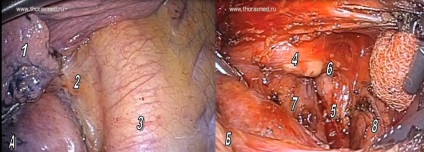
Рис.4 Лімфодіссекція в зоні біфуркації трахеї під час верхньої лобектомія справа
А - проекція біфуркації трахеї з лімфатичними вузлами 7 групи: 1 - непарна вена, 2 - стравохід, 3 - дуга непарної вени, 4 - праву легеню, 5 - медиастинальная плевра, що покриває задню поверхню кореня правої легені, 6 - міжреберна вена; Б - вид операційного поля після видалення клітковини і лімфатичних вузлів: 7 - лівий головний бронх, 8 - правий головний бронх, 9 - проміжний бронх, 10 - верхнедолевой бронх, 11 - задня стінка перикарда.
Медіастинальної лімфодіссекція при операції зліва представляє найбільші труднощі, особливо це стосується верхнедолевой локалізації пухлини. Це пов'язано з анатомічними особливостями: грудна аорта і стравохід прикривають зону біфуркації трахеї і ускладнюють доступ до біфуркаційним лімфовузлів, які розташовані у вузькому просторі між зазначеними структурами і задньою стінкою перикарду. З огляду на ці особливості, лімфодіссекцію зручніше виконувати до етапу видалення частки, за яку можна здійснювати тракцию догори і медіально. Рис.5. Виділення блоку клітковини проводиться за допомогою монополярной і біполярної коагуляції, а також гармонійного скальпеля. Слід пам'ятати про можливість механічної та електричної травми мембранозной частини головних бронхів і стінки стравоходу. У зв'язку з цим, необхідно уникати прямого контакту з активованою робочою частиною інструменту.
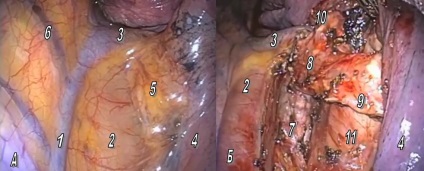
Мал. 5. Біфуркаційних лімфодіссекція зліва. А - задня поверхня кореня лівої легені; Б - вид біфуркації трахеї після лімфодіссекціі. 1 - нижня частка лівої легені, 2 - медиастинальная плевра, що покриває стравохід і зону біфуркації трахеї, 3 - грудна аорта, 4 - лівий головний бронх, 5 - правий головний бронх, 6 - біфуркація трахеї, задня стінка перикарда, 8 - стравохід.
Не менш важливою зоною лімфодіссекціі при лівосторонньої локалізації раку легкого є аортальне вікно. Тут розташовані лімфатичні вузли 5 і 6 груп. Видалення цього блоку клітковини має виконуватися дуже акуратно, максимально уникаючи травми лівого поворотного гортанного нерва. Мал. 6. Цей етап зручніше виконувати після перетину верхнедолевого бронха і видалення препарату.
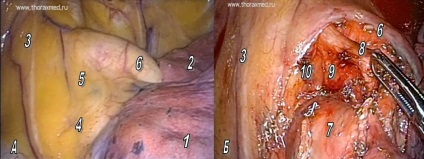
Рис.6 Зона аортального вікна з лімфатичними вузлами 5 і 6 груп. А - інтраопераційна ревізія; Б - вид операційного поля після завершення лімфодіссекціі. 1 - верхня частка лівої легені, 2 - нижня частка лівої легені, 3 - лівий діафрагмальнийнерв, 4 - передня поверхня кореня лівої легені, 5 - проекція аортального вікна, 6 - дуга аорти, 7 - стовбур лівої легеневої артерії з пересіченими сегментарними гілками, 8 - лівий блукаючий нерв, 9 - лівий поворотний гортанний нерв, 10 - проекція артеріальної зв'язки.
Операція закінчується промиванням і дренуванням плевральної порожнини. Для досягнення кращого гемостазу і зменшення кількості виділень по дренажу в післяопераційному періоді доцільно використання місцевих гемостатичних матеріалів, які укладаються в зони лімфодіссекціі. Місця установки портів пошарово вшиваються розсмоктується шовним матеріалом. Краї шкірних розрізів зводяться за допомогою спеціального клею, який забезпечує швидке загоєння і хороший косметичний ефект. рис.7
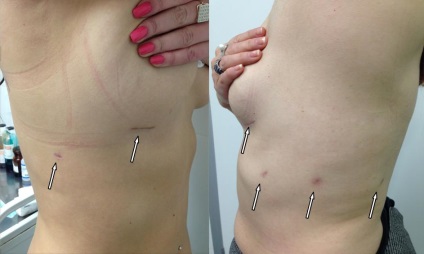
Рис.7. 3 місяці після торакоскопічної операції. А - верхня лобектомія справа; Б - нижня лобектомія зліва. Стрілками вказані місця установки портів.
Показання та протипоказання
В даний час абсолютними протипоказаннями до торакоскопічних операції можуть вважатися: непереносимість однолегочной вентиляції і розмір пухлини, який не дозволяє витягти її через невеликий розріз. При раку легені абсолютними протипоказаннями є: наявність метастазів в корені легені (рівень N1) і розмір пухлини в легкому більш 6см. Плевральні зрощення в даний час є відносним протипоказанням. На думку досвідчених хірургів, внутриплевральное спайковий процес, що вимагає конверсії зустрічається рідко, оскільки після створення невеликого простору для введення камери і несколькох інструментів ендоскопічний адгезіолізіс може проводитися швидко і безпечно. Також відносними протипоказаннями для торакоскопічної лобектомія є центральні пухлини (розташовані ближче 2см від гирла бронха) і лімфаденопатія в корені легені ускладнює виділення судин (хронічне запалення або каліцінати) [41. 42].
Частота конверсій різна і має стійку тенденцію до зменшення в міру накопичення досвіду. Ця ж закономірність стосується і часу операції. Якщо перші торакоскопічних лобектомія характеризуються значним збільшенням часу до 5-6 годин і більше, то з накопиченням досвіду і відпрацюванням основних прийомів, за умови достатнього технічного забезпечення, середній час операції скорочується в 1.5-2 рази і стає таким самим з традиційними операціями.
висновок
Безсумнівно, торакоскопічних операції повинні бути присутніми в арсеналі сучасної хірургічної клініки, що займається онкопульмонологіей. Однак, слід підкреслити, що для досягнення хороших результатів лікування раку легкого необхідний ретельний відбір пацієнтів із застосуванням сучасних методик передопераційного обстеження і клінічного стадіювання, використанням можливостей ПЕТ-КТ, трансбронхіальную і ЧЕРЕЗСТРАВОХІДНОЮ тонкоголкової біопсія лімфатічсекіх вузлів середостіння. При дотриманні методології навчання і ретельної селекції пацієнтів для виконання торакоскопічних операцій можна сподіватися на подальший розвиток методу і максимальну реалізацію основних принципів онкохірургії, до яких відносяться: онкологічна адекватність, функціональність і максимальна безпека.
Література.
1. Bozzini P. Lichtleiter, eine Erfindung zur Anschauung innerer Teile und Krankheiten, nebst der Abbildung. Journal der practischen Arzneykunde und Wundarzneykunst (Journal of Practical Medicine and Surgery), 1806. 24: p. 107-124.
2. Jacobaeus H.C. The Cauterization of Adhesions in Artificial Pneumothorax Treatment of Pulmonary Tuberculosis under Thoracoscopic Control. Proc R Soc Med, 1923. 16 (Electro Ther Sect): p. 45-62.
3. Semm K. [The endoscopic intra-abdominal suture (author's transl)]. Geburtshilfe Frauenheilkd, 1982. 42 (1): p. 56-7.