ПРОМИСЛОВЕ ОТРИМАННЯ АЛЮМІНІЮ
В даний час за обсягом виробництва алюміній займає перше місце серед кольорових металів, і виробництво його постійно розширюється.
Сьогодні вітчизняна алюмінієва промисловість для виробництва глинозему використовує апатито-нефелінові породи Хибинского масиву і нефелінові сиеніти ряду ме-сторожденій Сибіру і Уралу.
Глини та каоліни широко використовують у багатьох галузях промисловості при виробництві кераміки, вогнетривів і інших виробів. Глина, як извесно, є алюмосилікатом кальцію, а крім цього містить багато різних компонентів. Глина складається з дрібних кристалів. Ці кристали формують глиностворюючих мінерал класу силікатів - каолініт. Його склад: 47% оксиду кремнію IV (SiO2), 39% оксиду алюмінію (Аl2О3) і 14% води (Н20).
Глинозем - чистий оксид алюмінію (Аl2О3), основний, вихідний матеріал для виробництва алюмінію електролізом.
Вихід вчені та інженери знайшли в наступному. У електролізної ванні спочатку розплавляють кріоліт Na3 AlF6 (температура розплаву трохи нижче 1000 ° C). Криоліт можна отримати, наприклад, при переробці нефелінів Кольського півострова. Далі в цей розплав додають трохи Al2 О3 (до 10% по масі) і деякі інші речовини, улучает умови проведення наступного процесу. При електролізі цього розплаву відбувається розкладання оксиду алюмінію, кріоліт залишається в розплаві, а на катоді утворюється розплавлений алюміній:
Так як анодом при електролізі служить графіт, то виділяється на аноді кисень (O) реагує з графітом і утворюється вуглекислий газ СО2.
Електроліз кріолітогліноземних розплавів є основним способом отримання алюмінію, хоча деяку кількість алюмінієвих сплавів виходить електротермічним способом.
Перші промислові електролізери були на силу струму до 0,6 кА і за наступні 100 років вона зросла до 300 кА. Тим не менш, це не внесло істотних змін в основи виробничого процесу.
Загальна схема виробництва алюмінію представлена на малюнку нижче:
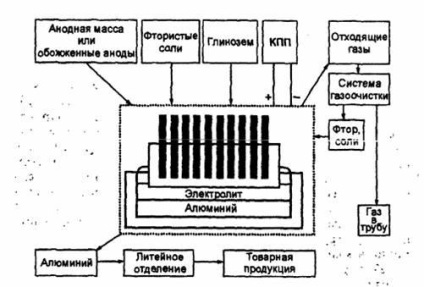
Основним агрегатом є електролізер. Електроліт є розплав кріоліту з невеликим надлишком фториду алюмінію, в якому розчинений глинозем. Процес ведуть при змінних концентраціях глинозему приблизно від 1 до 8% (мас.). Зверху в ванну опущений вугільний анод, частково занурений в електроліт. Існують два основних типи витрачаються анодів: самообжігающіеся і попередньо обпалені. Перші використовують тепло електролізу для випалу анодної маси, що складається з суміші коксу-наповнювача і зв'язуючого - пеку. Обпалені аноди є попередньо обпалену суміш коксу і пекового сполучного.
Розплавлений алюміній при температурі електролізу (950 - 960 ° С) важче електроліту і знаходиться на подине електролізера. Кріолітогліноземних розплави - дуже агресивні, протистояти яким можуть вуглецеві і деякі нові матеріали. З них і виконується внутрішня футеровка електролізера.
Процес, що протікає в електролізері, полягає в електролітичному розкладанні глинозему, розчиненого в електроліті. На рідкому алюмінієвому катоді виділяється алюміній, який періодично виливається за допомогою вакуум-ковша та направляється в ливарне відділення на розливання або міксер, де в залежності від подальшого призначення металу готуються сплави з кремнієм, магнієм, марганцем, міддю або проводиться рафінування. На аноді відбувається окислення виділяється киснем вуглецю. Відходить анодний газ являє собою суміш СО2 і СО.
Теоретично на процес електролізу витрачаються глинозем і вуглець анода, а також електроенергія, необхідна не тільки для здійснення електролітичного процесу - розкладання глинозему, але і для підтримки високої робочої температури. Практично витрачається і деяку кількість фтористих солей, які випаровуються і вбираються в футеровку. Для отримання 1 т алюмінію необхідно: