В.Я. Вартанов, М.М. Хутірська, І.Г. Труханова, Л.В. Кругова, С.А. Василькін, Ю.Г. Кутирева, М.М. Дорожкіна
ГБУЗ Самарської області «Тольяттинская міська клінічна лікарня № 5» (головний лікар - к.м.н. Н.А. Ренц), РФ
Кафедра анестезіології, реаніматології та швидкої медичної допомоги ІПО СамГМУ, РФ
V.Ia. Vartanov, N.N. Hutorskayia, I.G. Trukhanova, L.V. Krugova, S.A. Vasilkin, Yu.G. Kutireva, M.M. Dorozhkina
Ключові слова: аспіраційний синдром, повний шлунок, регургітація
Класики на те і класики, щоб кожне слово їх публікацій повторювалося, а часом і перебріхувалося нащадками.
Отже, нагадаємо ще раз читачеві, що аспіраційний гиперергический пневмоніт (АГП) або синдром Мендельсона розвивається при попаданні шлункового вмісту з рН нижче 2,5 і обсягом понад 25 мл в трахею і бронхи. Чим нижче рН і чим більший об'єм аспіріруемой рідини, тим важчий перебіг аспіраційного пневмоніту! Не зазнали значних метаморфоз і причини аспіраційного синдрому [3]:
- ПОВНИЙ ШЛУНОК (прийом їжі в межах 46 годин (при вагітності при будь-якому терміні прийому їжі), хірургічні захворювання органів черевної порожнини, гостра ниркова недостатність, цукровий діабет, черепно мозкова травма, коматозний стан, медикаментозний сон.
- ЗНИЖЕННЯ внутрішньогрудних тиск (ШВЛ з негативним тиском в кінці видиху, ручна ШВЛ).
- ЗНИЖЕННЯ ТОНУСУ кардіального гніту (під час вагітності, захворювання шлунково-кишкового тракту, медикаментозна депресія атропін, міорелаксанти, печія, стравохідний рефлюкс, запори).
- ПІДВИЩЕННЯ ВНУРІБРЮШНОГО ТИСКУ (вагітність, ожиріння, закид повітря в шлунок, фібриляція м'язів, парез кишечника).
Під час анестезіологічної допомоги ми найчастіше стикалися з аспірацією в період індукції (див. Рис.1) при багаторазових спробах інтубації трахеї і лише в невеликому відсотку випадків при порушенні герметичності манжети ендотрахеальної трубки і невідповідність діаметра трахеї розміром інтубаційної трубки [4].
Рис.1.
1 - частота розвитку аспірації в період індукції;
2 - частота розвитку АГП внаслідок порушення герметичності манжети ендотрахеальної трубки
Два основні варіанти патогенезу синдрому, описані класиками жанру, дозволили нащадкам лише «творчо» доповнити патогенез прикрасами типу «каскад ейкозаноїдів» і оцінкою впливу фактора некрозу пухлин.
Як відомо, в першому випадку в дихальні шляхи потрапляють великі частки неперетравленої їжі з шлунковим соком, як правило, нейтральною або слабокислою реакції. Відбувається механічна закупорка дихальних шляхів на рівні середніх бронхів і виникає клініка гострої дихальної недостатності (ГДН).
При другому варіанті (у вагітних зустрічається набагато частіше!) В дихальні шляхи аспирируется кислий шлунковий сік, що викликає хімічний опік слизової трахеї і бронхів з подальшим швидким розвитком набряку слизової, з формуванням в кінцевому підсумку бронхіальної обструкції.
Наведена нижче схема (див. Рис. 2) дозволить читачеві наочно уявити деякі ланки патогенезу.
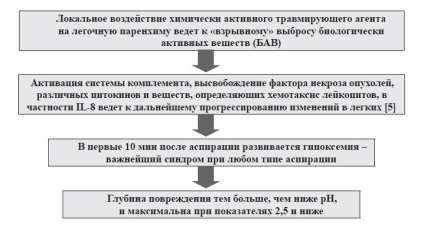
Мал. 2. Деякі ланки патогенезу АГП при аспірації кислого шлункового вмісту І ось тут-то настає момент (див. Рис. 3), коли патогенез перетворюється в танатогенез.
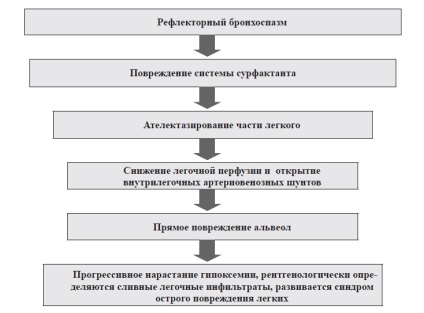
Мал. 3. детермінують танатогенеза
Добре, якщо батькам майбутнього анестезіолога в перші 7 років домашнього виховання вдалося прищепити дитині чесність - одну з найцінніших рис характеру і чеснот людини.
Якщо ж на порядність доктора розраховувати не доводиться, на думку про pазвитии аспіpаціонного сіндpома, повинна наводити раптово pазве клініка гострого астмоподобного нападу з ціанозом, задишкою, тахікардією, свистячим диханням і вислуховувати при аускультації численними хрипами в легенях з гpубая pентгенологіческімі пpизнак субтотальной пневмонії, що розвинулася ся в найближчі години після опеpации [6]. Приєднуються інфекційні ускладнення, часто з анаеробної флорою, є визначальними факторами в прогнозі [7].
Діагностичні критерії в літературі описані досить чітко [8]:
- Наявність вмісту шлунка в трахеї.
- Поява додаткових дихальних шумів при аускультації легенів.
- Підвищення опору вдиху (в залежності від вираженості бронхоспазму до 3040 см водн. Ст. І більше).
- Артеріальна гіпоксемія або збільшення АаDО2.
- «Снігова буря» при рентгенографії легких.
Обстеження повинно обов'язково включати:
- Екстрену бронхоскопію.
- Rграфію легких в динаміці.
- ЕКГ.
- ЦВД.
- КЩС і гази крові.
- Лейкоцитарну формулу.
- Біохімію крові.
Розробляючи лікувальну концепцію при даній патології, ми вирішили згадати про те, що все починається з хімічного опіку. Якщо так, то азбучні істини комбустіології свідчать, що надання першої допомоги при хімічних опіках шкіри включає:
- Якнайшвидше видалення хімічної речовини з ураженої поверхні.
- Зниження концентрації його залишків на шкірі за рахунок рясного промивання водою.
- Охолодження уражених ділянок.
Чим раніше і якісніше буде проведена первинна хірургічна обробка, тим краще резуль тати! Саме тому блок місцевого лікування, на нашу думку, має виглядати наступним чином:
- Лаваж легких проводять кілька разів охолодженим (до 1015º С) фізіологічним розчином 1015 мл через інтубаційну трубку до повного очищення.
- Екстрена бронхоскопія. Цілеспрямоване промивання трахеобронхіального дерева охолодженим (до 1015º С) фізіологічним розчином.
- При бронхоскопії метіпред вводиться локально в залежності від інтенсивності гіперемії -500 750 мг.
- Лідокаїн 80 мг 1% розчину місцево в зону гіперемії.
Серед перерахованих вище методів особливе значення надаємо екстреної бронхоскопії. На рис. 4 представлена тривалість ШВЛ в залежності від часу початку бронхоскопіческой санації.
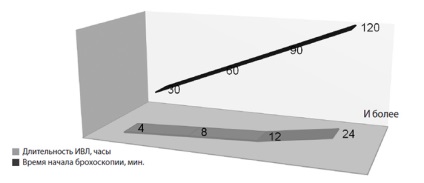
Рис.4. Тривалість ШВЛ в залежності від часу початку бронхоскопіческой санації
(Власні спостереження, n = 30)
Як видно з малюнка, якщо санація починалася в перші 30 хвилин після аспірації, то длитель ність ШВЛ не перевищувала 4 годин, при виконанні санаційної бронхоскопії протягом перших 2 год тривалість ШВЛ зростає до доби і більше.
Якщо говорити про респіраторної підтримки, то ми дотримуємося рутинних, добре відомих кожному фахівцю принципів:
- ШВЛ режим ПДКВ + 910 см вод. ст під контролем гемодинаміки спочатку 100% киснем з наступним плавним зниженням FiO2.
- Максимально допустимий тиск вдиху не повинно перевищувати 25 см вод. ст.
- Протективна ШВЛ (56 мл / кг маси).
- Переклад на спонтанне дихання відповідно до клінікою через режим pressure support.
- Перед екстубація проба на адекватність газообміну (самостійне дихання повітрям не менше 30 хв).
Особливе значення надаємо бронхолітичну терапії, яку вважаємо за необхідне проводити наступним чином:
- Алупент (бриканил) крапельно 0,51,5 мг / добу Перфузори.
- Інгаляція севорана до 1 об%.
- Еуфілін 240480 до 960 мг мг / добу.
- Надалі перкусійні масаж, обгортання 15% димексидом, бронхо і муколітики в терапевтичних дозах.
Подальша тактика повинна включати:
- Догляд за верхніми дихальними пyтямі (інгаляції, yдаленіе мокротиння, лікувальні фібробронхо скопии щодня).
- При продовженні ШВЛ більше 3 діб трахеостомия.
- Посів з трахеї і крові.
- Стимуляція моторики шлунково-кишкового тракту.
- Зондове харчування.
- Еластичне бинтування нижніх кінцівок.
- Лікувальна гімнастика.
Які ж сценарії найбільш типові для акушерського анестезіологареаніматолога при розвитку аспіраційного синдрому? Нам імпонує точка зору А.П. Зильбера і Е.М. Шифман [9]:
- Якщо аспірація сталася на етапі індукції в наркоз, і вдається зменшити явища гіпоксії і бронхіальної обструкції операцію слід починати після виконання всього комплексу лікувальних заходів (санаційної бронхоскопії, оптимізації вентиляції, введення бронхолітиків і т.д.).
- Якщо критично наростає ступінь гіпоксії, лікувальні заходи неефективні - показано екстрене абдомінальне розродження в інтересах плода.
- Якщо аспірація сталася в процесі виконання кесаревого розтину, необхідна операційна пауза, за час якої анестезіолог виконає весь комплекс заходів, спрямованих на зменшення гіпоксії, бронхіальній обструкції.
Профілактика аспіраційного синдрому:
- Евакуація зондом шлункового вмісту.
- Антациди (ранітидин, контролок, омез).
- У премедикацію включається метоклопрамид (1020 мг)
- Якщо втручання повинно початися негайно 0,3М рр цитрату натрію 30 мл дають випити під час вступу пацієнтки в операційну.
При планових операціях:
- Циметидин 400 мг на ніч і 400 мг за 2 години до анестезії per os.
- Ранітидин 150 мг на ніч і 150 мг за 2 години до анестезії per os.
- Омепразол 40мг на ніч і 40 мг за 2 години до анестезії per os.
- Метоклопрамід 10 мг в / в на етапі премедикації [10].
При екстрених втручаннях:
- Crushіндукція з виконанням прийому Селика (тиск з силою 5 кг прийнято в якості золотого стандарту для дорослих) починається відразу після преоксігенаціі 100% киснем до введення м'язовихрелаксантів і закінчується після інтубації трахеї і роздування манжетки.
- Якщо при інтубації відзначається надходження шлункового вмісту в глотку негайно надати положення Тределенбурга, яке слід дотримуватися (природно, в разі аспірації) до закінчення санації трахеобронхіального дерева. Потім необхідно ввести інтубаційну трубку в стравохід і роздути манжетку. Після санації ротоглотки інтубація трахеї запасний интубационной трубкою, після чого ввести зонд в шлунок.
Резюмуючи вищесказане, хотілося б навести тут одне з наших клінічних спостережень.
Оперативність дій лікарів була настільки висока, що, незважаючи на явні ознаки аспірації (вміст шлунка в трахеї, короткочасний ціаноз, тахікардія, поява численних хрипів в легенях, підвищення опору вдиху до 35 см водн. Ст. Зниження SaO2 до 89%), в протягом 10 хвилин була ліквідована бронхіальна обструкція, розпочато кесарів розтин, а через 5 хвилин після початку операції вилучено живу доношених дівчинка з оцінкою за шкалою Apgar 89 балів.
Відповідно до прийнятого у нас стандартом, була налагоджена інгаляція севорана, протективная ШВЛ c РЕЕР + 89 см. Також призначалися: бронхолітики (бриканил крапельно 1,0 мг / добу Перфузори, еуфілін 480 мг / добу); деескалаційна антибактеріальна терапія (тиенам 3 гр / добу в / в); метилпреднизолон (3 г / добу); НМГ та реологічно активні засоби, муколітики в стандартних дозуваннях. Вже через 2 години після закінчення операції через режим pressure support, після проби на адекватність газообміну і стабільній гемодинаміці переведена на спонтанне дихання. Надалі протягом післяопераційного періоду без особливостей, рентгенографічний контроль ні в день аспірації, ні в наступну добу патології з боку легень (див. Рис. 5) не виявив.
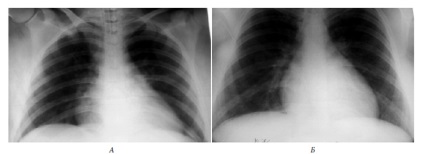
Рис.5. Рентгенографія легенів хворий Н. в день аспірації (А) і через 36 годин (Б)