Люмінесценція - цікаве фізичне явище, зміст якого полягає у випромінюванні «холодного» світла речовинами за рахунок поглиненої ними енергії збудження. Речовини, що володіють даними властивістю, називаються люминофорами. Люмінесценція ділиться на кілька типів, в залежності від процесу, який її викликає. Найбільший інтерес для мене представляє фосфоресценція - тип люмінесценції, при якому речовина випромінює поглинену світлову енергію не відразу, а поступово. Такі речовини називаються крісталлоф # 243; Сфорім або просто ФОСФО # 243; рами. Не варто плутати ці речовини з фосфором, елементом п'ятої групи, який до них не має ніякого відношення. Біла модифікація фосфору здатна слабо світиться в темряві, але природа явища тут інша, заснована на окисленні його киснем повітря (перебуваючи під водою, білий фосфор не світиться). Так що світяться в темряві іграшки, брелоки, фарби і т.д. - не мають з фосфором нічого спільного, і в їх складі фосфор не міститься.
Крісталлофосфори - це складні неорганічні речовини, які можуть світиться в темряві після попередньої засвічення видимим світлом або ультрафіолетом. У промисловості і побуті найчастіше поширені зелені крісталлофосфори, які додають в іграшки, брелоки, лаки для нігтів, стрілки годинника, наносять на футболки і т.д. Їх зачаровує світіння давно привертає мою увагу, і мені як хіміку природно захотілося зробити такі речовини самостійно. Сама хімічна технологія синтезу даних речовин не складна, але вимагає терпіння і акуратності. Необхідно ретельно очищати вихідні речовини до високого ступеня чистоти і потрібні досить високі температури для синтезу (900 ° C і вище).
Фосфор на основі борної кислоти - найпростіші «кухонні» склади, які можна без проблем приготувати вдома. Для їх синтезу необхідна борна кислота, яка купується в аптеці і добавка, що впливає на колір і яскравість світіння. Вимоги до чистоти невисокі (але з землею змішувати їх не варто). Готуються ці склади над полум'ям газової плити. Яскравість складів виходить дуже високою, особливо при опроміненні ультрафіолетом, але тривалість післясвітіння невисока і складає всього кілька секунд. Крім того, у даних фосфорів досить погана водостійкість, при контакті з водою вони моментально втрачають свої властивості. Та й на відкритому повітрі довго зберігати їх не можна. Найяскравіший склад виходить з добавкою флуоресцеїну - жовто-зеленого кольору. з добавкою саліцилової кислоти виходить менш яскравий склад блакитного кольору світіння. Спроба отримати борні люмінофори з іншим кольором післясвітіння не увінчалася успіхом.
Більш цікаві склади виходять на основі сульфідів кальцію, стронцію і барію. Вони мають набагато більш тривалий післясвічення і можуть бути отримані самих різних кольорів і відтінків, від червоного до фіолетово-синього. Недоліки - порівняно не висока яскравість і недостатня хімічна стійкість (на відкритому повітрі довго зберігати не можна).
Для синтезу цих складів вихідні реактиви повинні бути очищені до високого ступеня чистоти, інакше вся робота піде на смарку. Синтез проводиться при високих температурах, від 950 ° C до 1100 ° C в залежності від складу.
Нижче наведені основні фотографії найбільш вдалих складів, які вдалося зробити.
CaS • Bi (сульфід кальцію активоване вісмутом)

CaS / SrS • Bi (сульфід кальцію / стонція 3: 1 активоване вісмутом)

SrS / CaS • Bi (сульфід стронцію / кальцію 3: 1 активоване вісмутом)

SrS • Bi (сульфід стронцію активоване вісмутом)
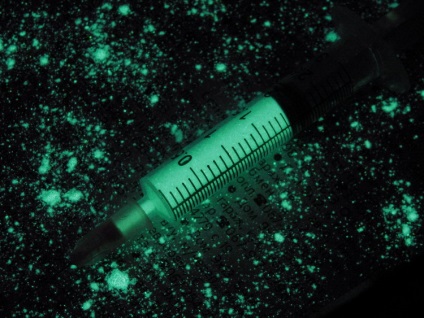
BaS • Bi (сульфід барію активоване вісмутом)

BaS • Cu (сульфід барію активоване міддю)

SrS • Eu, Tb (сульфід стронцію активоване европием і тербием)

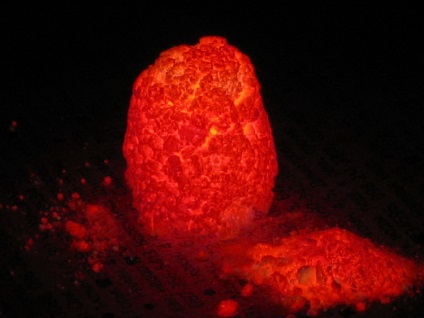
CaS / SrS • Eu, Tb (сульфід кальцію / стронцію 1: 1 активоване европием і тербием)
Мої статті по даній темі на elements.dp.ua: