Зараження вірусними інфекціями реципієнтів компонентів донорської крові залишається серйозною проблемою сучасної медицини. У Росії найчастіше переливають плазму, тому питання її вірусінактивації набуває особливої актуальності.

Принциповими недоліками існуючих методів профілактики передачі вірусів при переливанні плазми (відбір донорів, лабораторне обстеження, карантинізація, видалення лейкоцитів) є:
а) можливість помилки оператора і пропуску інфекції (ВІЛ, вірусні гепатити В і С) в клінічно безсимптомний період «серологічного вікна»;
б) обмежений спектр перерахованих вище тестованих вірусів, фактично допускає передачу герпесвирусов, Т-лімфотропної вірусу людини (HTLV), вірусу Західного Нілу (WNV), вірусів інших гепатитів, парвовіруса В19 і т.д. включаючи віруси, невідомі сучасній науці.
Зазначених вище недоліків позбавлені технології редукції патогенів (часто використовуються синоніми: інактивації патогенів, вірусінактивації).
Методи вірусінактивації плазми
В даний час для практичного використання в деяких країнах дозволені такі методи противірусної обробки:
- однієї дози плазми метиленовим синім [1, 2];
- пулу плазми методом «розчинник / детергент».
Вірусінактивація пулу плазми методом «розчинник / детергент» передбачена на створюваний російському заводі з виробництва препаратів крові [3].
Інактивації патогенів з метиленовим сініім
Метиленова синь - фенотіазинового основний барвник. Барвники цього класу здатні впроваджуватися в структуру нуклеїнових кислот вірусів і міцно зв'язуватися з залишками гуанозіна ДНК / РНК.
Після опромінення світлом з довжиною хвиль від 590 до 630 нм фотоактівірованний барвник окисляє кисень до синглетного, хімічно що ушкоджує генетичний матеріал вірусу. Тим самим процес його реплікації, отже, і зараження реципієнта стають неможливими [5].
Технологія інактивації вірусів являє послідовність стандартних операцій, відтворюваних співробітником центру крові:
- фільтраційне видалення лейкоцитів з плазми;
- додавання до плазми метиленового синього;
- опромінення видимим світлом в апараті «Макотронік»;
- фільтраційне видалення з плазми метиленового синього;
- переливання плазми пацієнту або заморожування плазми для подальшого зберігання [6].
Складові частини видаткової системи:
1. лейкофільтром PLAS4 - для видалення лейкоцитів з плазми.
2. Таблетка метиленового синього, інтегрована в замкнуту систему.
3. Контейнер для експозиції.
4. Фільтр «Блюфлекс» (Blueflex) для видалення метиленової сині з обробленої плазми 5. Контейнер для зберігання плазми при температурі нижче - 30 ° С.

Кількість метиленового синього, використовуваного в процесі «Макотронік» (0,085 мг на одну одиницю плазми), в сотні разів нижче, ніж клінічна доза, що застосовується при лікуванні метгемоглобінемії (до 7 мг / кг) і гіпотензії, індукованої високим рівнем оксиду азоту (1 мг / кг).
Понад 4,5 мільйона одиниць свіжозамороженої плазми (МС-СЗП), обробленої метиленовим синім, було успішно перелито в Європі і Азії.
Повідомлень про побічні ефекти, викликаних застосуванням плазми, обробленої метиленовим синім, немає.
Всі частини системи «Макотронік» за ступенем ризику застосування відносяться до Класу III згідно Європейської директиві по медичним приладам 93/42 / ЄЕС та виготовлені відповідно до Стандартів якості ISO 9001.
ефективність
Для отримання дозволу уповноваженого органу (Єврокомісія в Євросоюзі, FDA в США і т.д.) на практичне використання технології інактивації і видалення вірусів має бути чітко показано, що застосовуються процеси здатні видалити або інактивувати широкий спектр вірусів і є безпечними.
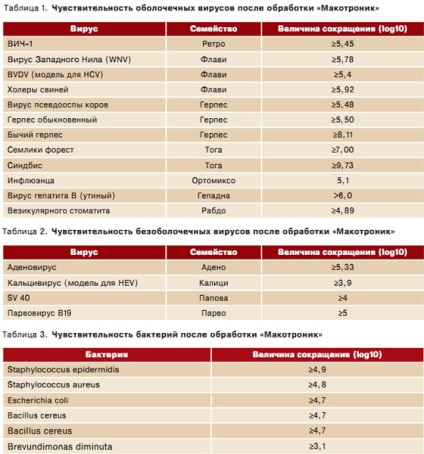
Доведено максимальна (серед усіх відомих методів) ступінь інактивації вірусів метиленовим синім і видимим світлом - як у відношенні оболонкових вірусів (табл. 1), так і безоболочечних вірусів (табл. 2) і бактерій (табл. 3).
При реєстрації медичної технології отримання і застосування МС-СЗП в Росії випробування, проведені в шести провідних науково-клінічних центрах, підтвердили дані зарубіжних колег [6].
Фактори згортання і інші білки
У Європі та Росії провели детальне вивчення показників гемокоагуляції на п'яти різних етапах отримання МС-СЗП: до обробки; після фільтрації плазми через
PLAS4; після розчинення метиленового синього; після опромінення; після фільтраційної елімінації метиленового синього.
Встановлено, що в процесі інактивації вірусів лише етап опромінення впливає на активність факторів згортання. Найбільш лабилен (до 20% зниження) фактор VIII, в меншій мірі - фібриноген і фактор X. Проте, зміна змісту цих факторів не виходить за фізіологічні межі.
переваги
Робота з одиничною дозою плазми, приготовленої з крові одного донора, має низку переваг:
1. Відсутній ризик перехресного зараження, що виникає при об'єднанні кількох доз плазми різних донорів.
2. Обробка на місці - методика доступна будь-якої медичної організації, яка отримує чи застосовує донорську плазму.
3. Можливість застосування як для свежезаготовленной, так і для свіжозамороженої плазми (СЗП).
4. Можливість отримання вірусінактивовані криопреципитата і кріосупернатантной плазми.
5. Можливість вибору донора-чоловіки (для профілактики передачі антілейкоцітарних антитіл - причини гострого ураження легень, пов'язаного з трансфузией).
6. Можливість вибору плазми групи АВ (для профілактики переливання імунних анти-А і анти-В-антитіл).
7. Доведена максимальне (у порівнянні з іншими методами) зниження ризику передачі відомих або невідомих збудників вірусних захворювань.
Тим самим створено правові передумови для впровадження передових технологій в практику російської служби крові та охорони здоров'я в цілому.

Існують три способи впровадження вірусінактивації однієї дози плазми метиленовим синім:
1. Всі дози плазми для переливання в країні (Бельгія, 12 з 14 регіонів Франції, регіони Іспанії, Німеччини).
2. Всі дози плазми в країні, призначені для переливання дітям до 16 років (Великобританія).
3. В ініціативному порядку в якості додаткового методу підвищення безпеки трансфузійної терапії (Франція, Іспанія, Італія, Швеція, Бразилія, Греція,
Австрія і т.д.).
висновок
В арсеналі російських трансфузіологов вже більше п'яти років є технологія інактивації патогенів метиленовим синім / видимим світлом (МС-СЗП), що гарантує вірусну безпеку реципієнтів донорської плазми.
Устаткування для одержання МС-СЗП входить в базовий комплект оснащення центру крові, передбачений національним проектом «Охорона здоров'я». У пілотних регіонах показана можливість повного забезпечення МС-СЗП педіатричних, пологових, гінекологічних відділень - з розширенням контингенту реципієнтів. Зберігання, транспортування та застосування (включаючи показання) МС-СЗП не відрізняються від таких для звичайної свіжозамороженої плазми. *
Також на HealthyNation.ru