Будова гепатоцитів. Гістологія, функції
Гепатоцити є клітинами багатогранної форми з шістьма або більшою кількістю поверхонь і діаметром 20-30 мкм. На зрізах, забарвлених гематоксиліном і еозином, цитоплазма гепатоцитів - еозинофільна, головним чином, через велику кількість мітохондрій і деякої кількості елементів аЕПС. Гепатоцити, розташовані на різній відстані від портальних просторів, розрізняються своїми структурними, гистохимическими і біохімічними характеристиками.
Поверхня кожного гепатоцита знаходиться в контакті зі стінкою синусоидов через простір Діссе, а також з поверхнею інших гепатоцитів. У тих ділянках, де контактують два гепатоцита, вони обмежують трубчасте простір між ними, яке відоме як жовчний капіляр, або жовчний каналець. Жовчні капіляри, які є початковою частиною системи жовчних проток, є трубочками діаметром 1-2 мкм. Вони обмежені тільки плазматическими мембранами двох гепатоцитів, причому в їх просвіт звернені нечисленні мікроворсинки.
Клітинні мембрани близько цих капілярів міцно пов'язані щільними з'єднаннями. Щілинні з'єднання часто зустрічаються між гепатоцитами і є ділянками міжклітинних з'єднань, забезпечуючи важливий процес координації фізіологічної активності цих клітин. Жовчні капіляри утворюють складні анастомозирующие мережі, які простягаються вздовж платівок печінкової часточки і закінчуються в області портальних просторів. Таким чином, струм жовчі відбувається в напрямку, протилежному напрямку течії крові, тобто від центру часточки до її периферії. На периферії часточки жовч потрапляє в жовчні проточки, або канали Герінга, утворені кубічними клітинами.
Проходячи на невелику відстань. проточки перетинають ряд гепатоцитів, що обмежують часточку, і переходять в жовчні протоки в портальних просторах. Жовчні протоки вистелені кубічним або стовпчастим епітелієм і мають виразну соединительнотканную оболонку. Вони поступово збільшуються і зливаються, утворюючи правий і лівий печінкові протоки, які в подальшому виходять з печінки.
Поверхня гепатоцита. звернена в простір Діссе, покрита численними микроворсинками, які виступають в цей простір, але завжди між ними і клітинами стінки синусоїдів залишається зазор. Гепатоцит містить одне або два круглих ядра з одним або двома ядерця. Деякі ядра є поліплоїдні, тобто вони містять парну кількість гаплоїдних наборів хромосом. Поліплоїдні ядра характеризуються великими розмірами, які пропорційні їх плоїдності. У гепатоците сильно розвинена ЕРС, як аЕПС, так і гранулярних ендоплазматичної мережі (грЕПС). ГрЕПС в гепатоците утворює агрегати, розсіяні по цитоплазмі - базофільні тільця.
У цих структурах на полірібосомамі синтезується ряд білків (наприклад, альбумін і фібриноген крові). Різні важливі процеси відбуваються в аЕПС, яка дифузно розподілена по всій цитоплазмі. Ця органела відповідальна за процеси окислення, метилування і кон'югації, необхідні для інактивації або детоксикації різних речовин до їх виведення з організму. аЕПС є лабільною системою, швидко реагує на молекули, що потрапили в гепатоцит.
Одним з найбільш важливих процесів. що відбуваються в аЕПС, є кон'югація гидрофобного (водонерозчинного) токсичного білірубіну глюкуронилтрансфераза з утворенням водорозчинного нетоксичного глюкуронида білірубіну. Цей кон'югат виділяється гепатоцитами в жовч. Якщо не відбувається екскреції білірубіну або глюкуроніду білірубіну, можуть розвинутися різні захворювання, які характеризуються жовтяницею - наявністю жовчних пігментів в крові. Однією з серйозних причин жовтяниці у новонароджених є нерідко зустрічається недорозвинення аЕПС в їх гепатоцитах (неонатальна гіпербілірубінемія). Сучасне лікування в таких випадках полягає у впливі синім світлом від звичайних флюоресцентних ламп, яке викликає трансформацію некон'югованого білірубіну в водорозчинний фотоізомер, який може віддалятися нирками.
Гепатоцит часто містить глікоген. Цей полісахарид виглядає під електронним мікроскопом як великі електронно-щільні гранули, які часто накопичуються в цитоплазмі поблизу аЕПС. Кількість глікогену, що є в печінці, змінюється відповідно до добового ритму; воно залежить також від стану харчування індивідуума. Глікоген печінки є сховищем глюкози і мобілізується, якщо рівень глюкози в крові падає нижче нормального. Таким шляхом гепатоцити підтримують постійний рівень глюкози в крові, яка є одним з головних джерел енергії, використовуваної організмом.
Комплекс Гольджі в гепатоцитах також є множинним - до 50 в одній клітині. Функції цієї органели включають освіту лізосом і секрецію білків плазми (наприклад, альбуміну, білків системи комплементу), глікопротеїнів (наприклад, трансферину) і ліпопротеїнів (наприклад, ліпопротеїнів дуже низької щільності).
Зазвичай гепатоцити не накопичують білки в своїй цитоплазмі у вигляді секреторних гранул, а безперервно виділяють їх в кровотік. Близько 5% білка, що секретується печінкою, виробляється клітинами макрофагальної системи (клітинами Купфера); інші синтезуються гепатоцитами.
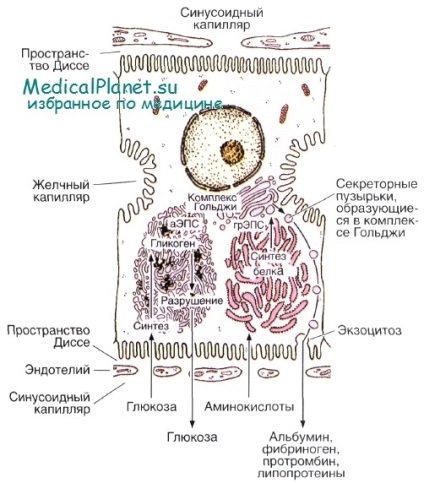
Секреція жовчі є екзокринної функцією в тому сенсі, що гепатоцити забезпечують захоплення, переробку і виведення компонентів крові в жовчні капіляри. Жовч містить декілька інших важливих компонентів вдополненіе до води і електролітів: жовчні кислоти, фосфоліпіди, холестерол, лецитин і білірубін. Близько 90% цих речовин виходять завдяки всмоктуванню епітелієм дистальної кишки і транспортуються гепатоцитами з крові в жовчні капіляри (ентерогепатична рециркуляція). Приблизно 10% жовчних кислот синтезуються в аЕПС гепатоцита за допомогою кон'югації холевой кислот (синтезованих печінкою з холестеролу) з амінокислотами гліцином або таурином, в результаті чого утворюються глікохолевой або таурохолевая кислоти. Жовчні кислоти володіють важливою функцією в емульгуванні ліпідів в травному тракті, забезпечуючи їх більш легке перетравлювання ліпазами і подальше всмоктування.
Від 70 до 90% білірубіну утворюється внаслідок руйнування гемоглобіну старіючих циркулюючих еритроцитів, яке здійснюється, головним чином, в селезінці, але відбувається також і у всій решті периферичної системі мононуклеарних фагоцитів, включаючи клітини Купфера в печінці. У крові білірубін тісно пов'язаний з альбуміном. Після перенесення в гепатоцит, ймовірно, за допомогою механізму полегшеного транспорту, гідрофобний білірубін кон'югується в аЕПС з глюкуроновою кислотою, з утворенням водорозчинного глюкуронида білірубіну. На наступному етапі глюкуронід білірубіну секретується в жовчні капіляри.
Часто використовуваними функціональними тестами печінки є вимірювання рівня білірубіну в сироватці крові (показник печінкової кон'югації і екскреції), альбуміну і протромбіну-вого часу (показники білкового синтезу). Аномальні результати цих тестів типові для дисфункції печінки.
Ліпіди і вуглеводи накопичуються в печінці у формі тригліцеридів і глікогену. Ця здатність запасати метаболіти грає важливу роль, тому що вона забезпечує організм енергією в проміжках між прийомами їжі. Печінка також служить головним місцем накопичення вітамінів, особливо вітаміну А. Вітамін А потрапляє в організм з їжею, досягає печінки з іншими харчовими ліпідами в формі хіломікронів. У печінці вітамін А запасається в клітинах Іто. Гепатоцит забезпечує також синтез глюкози з інших метаболітів - таких, як ліпіди та амінокислоти, за допомогою складного ферментного процесу, відомого як глюконеогенез (грец. Glykys - солодкий + neos - новий + genesis - вироблення).
Він являє собою також і головне місце дезаминирования амінокислот, в результаті чого виробляється сечовина. Сечовина транспортується кров'ю до нирок і виділяється цими органами. Різні лікарські препарати і речовини можуть инактивироваться шляхом окислення, метилування або кон'югації.
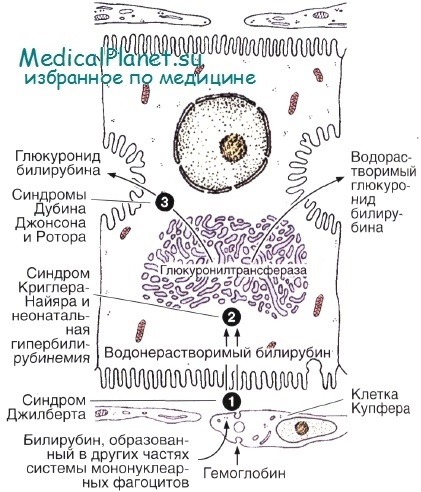
Ферменти. які беруть участь в цих процесах, локалізовані, головним чином, в аЕПС. Глюкуронилтрансфераза, фермент, який забезпечує кон'югацію глюкуронової кислоти з білірубіном, також викликає кон'югацію ряді інших сполук, таких, як стероїди, барбітурати, антигістамінні і протисудомні препарати. У деяких умовах лікарські препарати, які інактивуються печінкою, можуть індукувати збільшення обсягу аЕПС гепатоцитів, тим самим посилюючи здатність органу до детоксикації.
Введення барбітуратів лабораторним тваринам викликає швидкий розвиток аЕПС в гепатоцитах. Барбітурати можуть також посилити синтез глюкуронілтрансферази. Ці дані привели до використання барбітуратів потяг недостатності глюкуронілтрансферази.
регенерація печінки
Незважаючи на низьку швидкість відновлення клітин. печінку володіє надзвичайною здатністю до регенерації. Втрата тканини печінки внаслідок хірургічного видалення або дії токсичних речовин запускає механізм, завдяки якому гепатоцити починають ділитися, що триває до тих пір, поки не відновиться початкова маса тканини. У людини ця здатність істотно обмежена, але все ж залишається досить вираженою, тому фрагменти печінки можуть бути використані при хірургічної трансплантації печінки.
Тканина регенерувати печінки зазвичай добре організована, в ній виявляється типове дольковое будова, і функціонально вона заміщає зруйновану тканину. Однак коли відбувається безперервне або повторне ушкодження гепатоцитів протягом тривалого періоду часу, розмноження клітин печінки супроводжується істотним збільшенням вмісту сполучної тканини. Замість утворення нормальної тканини печінки відбувається формування вузликів різних розмірів, велика частина яких видно неозброєним оком. Ці вузлики складаються з центральної маси дезорганізованих гепатоцитів, оточених значною кількістю сполучної тканини, дуже багатою колагеновими волокнами.
Таке порушення. відоме як цироз, є прогресуючим і незворотним процесом, який викликає печінкову недостатність і зазвичай призводить до смерті. Етоттіп фіброзу є дифузним, що вражає всю печінку. Цироз являє собою кінцевий результат ряду захворювань, які порушують архітектоніку печінки, зазвичай внаслідок тривалого прогресуючого пошкодження гепатоцитів, викликаного такими факторами, як етиловий спирт, лікарські препарати або інші хімічні речовини, вірус гепатиту (головним чином, типів В, С або D) і аутоімунне захворювання печінки. У деяких регіонах світу частою причиною цирозу є інфекція кишковим паразитом Schistosoma.
Яйця цього паразита переносяться венозною кров'ю і захоплюються печінковими синусоїдами з пошкодженням гепатоцитів. Пошкодження печінки, викликане алкоголем, обумовлює велику частину випадків цирозу, тому що етанол метаболізується переважно в печінці. Деякими передбачуваними патогенетичними механізмами ушкодження печінки, індукованими алкоголем, є утворення кисневих радикалів (ймовірно, внаслідок перекисного окислення ліпідів), ацетальдегіду і прозапальних і профіброгенних цитокінів. Етанол також змінює регенерацію печінки за допомогою невідомого механізму, що сприяє розвитку цирозу.
