Електропровідність води -фізико-хімічний показник води
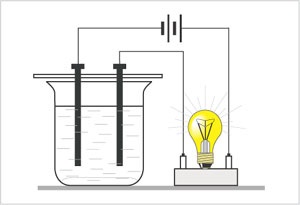
Електропровідність природної води залежить, головним чином, від двох основних показників: від рівня розчинених в ній мінеральних солей і від температури води. Така залежність дозволяє робити і зворотні висновки, тобто визначати ступінь мінералізації води за величиною електричної провідності. Існують прилади оперативного вимірювання загального вмісту солей у воді (TDS-метри), які активно використовують даний метод вимірювання.
Природні води - це розчини сумішей слабких і сильних електролітів. Електропровідність цих вод обумовлюється, головним чином, що містяться в них іонами калію, кальцію, натрію, хлору, бікарбонату і сульфату. Іони тривалентного і двовалентного заліза, а також іони алюмінію, марганцю, нітрату і т.п. також впливають на електричну провідність води, але в значно меншому ступені. Хоча вплив цих іонів може бути більш відчутним, якщо вони містяться у воді в дуже великих кількостях, що може бути притаманне, наприклад, господарсько-побутовим або виробничих стічних вод.
При вимірюванні рівня мінералізації води за величиною її електропровідності може виникати деяка похибка, пов'язана з тим, що розчини різних солей мають неоднакову питому електричну провідність. Також дана похибка може бути викликана підвищенням електропровідності, викликаним збільшенням температури. Проте, сучасні технічні засоби дозволяють зводити ці похибки до мінімуму, що відбувається внаслідок попереднього підрахунку залежностей і їх занесення в пам'ять.