Легкість і зручність в новому обсязі.
Біля ліжка пацієнта, в операційній або на спортивному майданчику - завжди готовий до використання.
Незважаючи на досягнуті успіхи, як і раніше важко розпізнавати ряд захворювань верхніх сечових шляхів і уретри, так як при відсутності дилатації неможливо візуалізувати чашечно-мискової систему і сечовід. Тільки при порушеному пасажі сечі по верхніх сечових шляхах або медикаментозної поліурії можна визначити розширення чашечно-мискової системи і лише частково побачити сечовід. Оцінка морфологічних змін сечових шляхів і навколишніх тканин звичайним методом ультразвукового дослідження неможлива. Традиційно застосовувані методи ультрасонографии теж високоінформативними при папілярних утвореннях балії і сечоводу, при виявленні причин гидронефротической трансформації, при каменях сечоводу, невеликих конкрементах миски та чашок, хвороби Ормонда [23,34,36]. Візуалізація простатичного відділу сечівника можлива шляхом трансректального ехосканірованія в момент мікціі (мікційна трансректальная ехоуретрографія) або при введеному по уретрі катетер [15]; пенильной частини уретри - при неінвазивному ультразвуковому дослідженні статевого члена. Ці методики не завжди можуть оцінити взаємозв'язок патологічних утворень з уретрою, неможлива візуалізація сечівника на всьому протязі. Крім ультразвукових інші, наявні в арсеналі уролога методи діагностики (рентгенологічні, ендоскопічні, магнітно-резонансна томографія) не завжди відповідають на питання про ступінь поширення патологічного процесу в стінці сечових шляхів і навколишніх тканинах, що вкрай важливо в діагностиці та визначенні лікувальної тактики. Все це дало передумови для пошуку нових способів отримання більш якісного зображення сечових шляхів, розробки різних модифікацій ультразвукових датчиків для інвазивної ультрасонографии.
Вважаємо за доцільне обговорення назв застосовуються в даний час ультразвукових методик в урології. Очевидно, що проведення датчика по сечових шляхах відноситься до інвазивних або інтервенційних методів ультрасонографії. Разом з тим в ряді публікацій поняття "інвазивний ультразвук" має на увазі малоінвазивні хірургічні втручання, що проводяться під контролем ехосканірованія. На нашу думку, існуючі ультразвукові методики можна розділити наступним чином:
- неінвазивна ультрасонографія - найбільш широко застосовуваний метод, дослідження проводиться через неушкоджений шкірний покрив;
- интраоперационная ехографія - проводиться при встановленні датчика безпосередньо на досліджуваний орган під час відкритих оперативних втручань;
- инвазивная (інтервенційна) ультрасонографія - використання спеціальних ультразвукових датчиків, безпосередньо вводяться через природні отвори. До цих методів належать: трансректальная, трансвагінальна, трансуретральная ультрасонографія (дослідження сечового міхура за допомогою ригідного датчика, що проводиться за уретрі в сечовий міхур), ендолюмінальная (Інтрауретральная і інтрауретеральная) ультрасонографія;
- малоінвазивні хірургічні втручання під контролем ультразвукової візуалізації - пункція кіст нирок, пункційна нефростомія, пункційна цистостомія, біопсія органів і т.п.
Дослідження сечоводу, уретри шляхом їх ехосканірованія зсередини ми назвали інтрауретрально і інтрауретеральной ультрасонографія.
матеріали та методи
Використовували мініатюрний ультразвуковий механічний датчик з радіальним типом сканування частотою 9-12 МГц, вмонтований в проксимальний кінець гнучкого катетера-провідника діаметром 7-9 Fr "Sonicath" (рис. 1) Досліджували уретру і навколишні її тканини шляхом безпосереднього проведення катетера-провідника зі вбудованим датчиком ретроградно по уретрі в сечовий міхур і при його виведенні. Отримували послідовно ультрасонограмми уретри і парауретральних тканин у всіх її відділах. При стриктурах уретри, непрохідних для катетера, дослідження поєднували з уретроскопія. Вводили катетер з датчиком по робочому каналу цистоскопа до зони звуження. Отримували прицільні ультрасонограмми зони стриктури. Верхні сечові шляхи досліджували в поєднанні з цистоськопієй. За робочому каналу цистоскопа проводили датчик в сечовід до миски, отримуючи в міру проведення датчика послідовні зображення сечоводу, парауретеральних тканин від гирла до миски. Дослідження проводили під рентгентелевізіонним контролем.
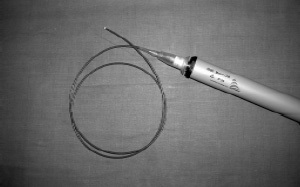
Мал. 1. Гнучкий катетер-провідник з ультразвуковим датчиком в проксимальному його кінці для ендолюмінальной ультрасонографии.
Всього обстежено 64 пацієнта віком від 21 до 61 року. Інтрауретральная ультрасонографія виконана у 21 пацієнта. У 19 були стриктури уретри різної локалізації, у 1 - склероз шийки сечового міхура. Одному хворому дослідження проведено для виключення рецидиву раку після радикальної простатектомії. Поєднання стриктури уретри і гіперплазії простати мало місце у 3 пацієнтів. У 43 хворих досліджували верхні сечові шляхи (сечовід, чашково-мискової систему). З них 33 пацієнта з обструктивними захворюваннями: 3 - зі стриктурами середньої і нижньої третини сечоводу, 30 - зі стенозом мисково-сечовідного сегмента. У 10 пацієнтів показанням до інтрауретеральной ультрасонографии була підозра на папілярні освіти чашечно-мискової системи і (або) сечоводу. Всім хворим виконували загальне ультразвукове дослідження, комп'ютерну томографію, магнітно-резонансну урографию, екскреторну рентгенівську урографию, ретроградну уретеропієлографії і ендоскопічні дослідження.
результати
При інтрауретрально ультрасонографии в незмінених відділах чоловічої уретри в міру проведення датчика ми визначали головку статевого члена, губчасте тіло, кавернозні тіла з оточуючими їх оболонками, судини. У більш широкому цибулинні відділі реєструвалися спонгіозна тканину з тоншою стінкою і прикріпляються до неї м'язами (рис. 2). У мембранозному відділі (рис. 3) спонгіозна тканина не визначається, візуалізуються підвищеноїехогенності платівка тазової фасції, далі сечостатева діафрагма з проходять судинами. При проведенні датчика в область простатичного відділу добре визначається передміхурова залоза, її транзиторная, центральна, частково периферична зони, капсула. Чітко візуалізуються патологічні утворення в паренхімі (рис. 4). У зоні стриктури сечівника визначається різної протяжності і глибини фіброзна тканина у вигляді гіперехогенних ділянок. На рис. 5а представлена нормальна ехограма губчастої частини уретри, на рис. 5б - ехограма спонгиозной частини уретри в зоні її стриктури. Визначається фіброзний ділянку у вигляді гіперехогенних кільця навколо уретри, що зачіпає всю товщу спонгиозного тіла (спонгіофіброз). На рис. 6а, б представлені ультрасонограмми в зоні стриктури на кордоні мембранозного і простатичного відділів. Визначаються підвищеноїехогенності ділянки фіброзу, що поширюються за межі уретри в парауретральной тканину. У міру проведення датчика визначається протяжність фіброзно-змінених тканин.
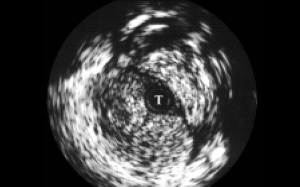
Мал. 2. УЗ-ехограма нормального цибулинного відділу уретри; Т - трансдуктор.
Мал. 5. УЗ-ехограма сечівника:
а - нормальної губчастої частини; б - зони стриктури (стрілка).
При інтрауретеральном ехосканірованіі в незміненій частині сечоводу чітко візуалізуються зниженою ехогенності м'язовий шар, навколо гіперехогенна адвентиція. Товщина стінки сечоводу коливалася в межах 0,7-1,2 мм. Навколо його стінки визначається підвищеною відлуння генності парауретеральная клітковина (рис. 7). У міру проведення датчика візуалізуються межують з сечовими шляхами судини, м'язи, чашечно-лоханочная система, ниркова паренхіма (рис. 8а, б). У сечоводі при стенозі мисково-сечовідного сегмента нижче стенозированного сегмента спостерігалися наступні зміни: при початкових стадіях - потовщення стінки за рахунок м'язового шару, а при виражених - витончення. Зона стенозу була представлена єдиної гіперехогенной тканиною. При поширенні склеротичного процесу в навколишні тканини адвентиція не визначалась, зона стенозу представляла гіперехогенну тканину, що поширюється в парауретеральную клітковину. Якщо мали аберантних посудину, останній чітко визначався (рис. 9). При прохідних для катетера стриктурах середньої і нижньої третини сечоводу ми визначали їх протяжність і досліджували сечовід вище звуження. У зоні стриктури ми спостерігали ідентичну, описану при стенозі мисково-сечовідного сегмента картину, з разіцей лише в ступені залучення в процес періуретеральной клітковини. У сечоводі вище стриктури - витончення його стінки в залежності від вираженості гидронефротической трансформації. Отримані нами попередні висновки знайшли своє підтвердження при наступних оперативних втручаннях і підкріплені результатами морфологічних досліджень змінених ділянок сечоводу.
З 10 обстежених пацієнтів з підозрою на папілярні освіти чашечно-мискової системи і сечоводу, у 8 діагноз не підтвердився. У 1 хворого за допомогою інтрапельвікального ехосканірованія була виявлена невеликих розмірів (0,7 см в діаметрі) парапельвікальная кіста, що створює дефект наповнення при екскреторної урографії, ретроградної уретеропієлографії, комп'ютерної томографії з контрастуванням (рис. 10). Комп'ютерна навігація, виконана на підставі даних спіральної томографії, дозволила отримати віртуальну ендоскопічну картину чашечно-мискової системи, сечоводу і визначити пролабирование стінки балії, відповідне дефекту наповнення на рентгенограмах (рис. 11). При оптичної уретеропіелоскопіі також констатовано пролабирование балії. Таким чином, інтрауретеральная ультрасонографія - єдиний метод, що дозволив найбільш чітко не тільки виявити зміна форми балії, а й визначити причину цього стану - парапельвікальная кіста (рис. 12). У 1 пацієнтки виявлено невеликих розмірів (2 мм) рентгеннегатівний камінь сечоводу. У 2 хворих діагноз пухлини підтвердився. На інтрауретеральних ультрасонограммах пухлина визначалася як освіта неоднорідною ехоструктури, переважно гіпоехогенні, що створює нерівність внутрішнього контуру балії, сечоводу. У 1 пацієнта виявлено 3 папілярних освіти сечоводу розмірами 0,3-0,4 см, що не инфильтрирующие м'язовий шар і адвентіцію (рис. 13). За допомогою даного методу була встановлена ступінь інвазії - стадія Т1, що в поєднанні з іншими клінічними даними дозволило виконати ендоскопічну резекцію стінки сечоводу з пухлиною. У 1 пацієнта інтрауретеральная ультрасонографія поряд з іншими методами, крім візуалізації множинних об'ємних утворень чашечно-мискової системи і сечоводу, дозволила визначити їх структуру та оцінити глибину інвазії (рис. 14). Пацієнту була виконана нефруретеректомія з резекцією гирла і лімфаденектомія.
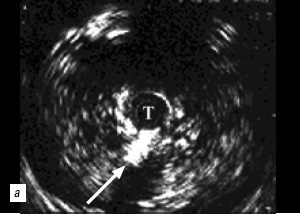
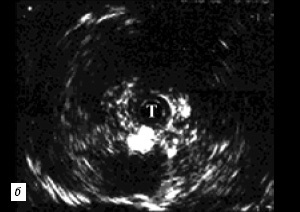
Мал. 6. УЗ-ехограми зони стриктури на кордоні мембранозного (а) і простатичного (б) відділів; стрілка - ділянку склерозу.
Мал. 14. УЗ-ехограма множинної пухлини миски.
Отримана інформація при інтрауретрально ехосканірованіі допомагає вибрати найбільш правильний метод оперативного лікування. При значному залученні в процес навколишніх тканин в області стриктури показана відкрита пластична операція сечівника, а при стриктурах з поверхневими фіброзними змінами, що не виходять за межі уретри в парауретральной тканину, найбільш доцільна оптична уретротомія, яка може виконуватися під контролем интрауретрального ехосканірованія для визначення радикальності висічення фіброзно-зміненої тканини.
Інформація, що отримується при інтрауретеральной ультрасонографии, дозволяє виявити не тільки протяжність стриктури, але і ступінь поширення склеротичних змін в стінці сечоводу і за її межами, що також важливо в виборі методу оперативного лікування. При мінімальних склеротичних змінах в стінці сечоводу або неможливості виконання відкритої пластичної операції на верхніх сечових шляхах доцільно ендоскопічне розсічення стриктури сечоводу. Для визначення кордону розтину склеротично зміненої тканини, а також контролю розташування судин в зоні резекції оперативне втручання можливо і доцільно проводити під контролем інтрауретеральной ультрасонографии. За допомогою інтрауретеральной ультрасонографии можна виявити не тільки наявність пухлини сечоводу і чашково-мискової системи, а й визначити поодинокі або множинні папілярних утворень, ступінь інвазії пухлини, стан ниркового синуса, парауретеральной клітковини, що важливо для визначення обсягу оперативного посібники. У випадках можливої резекції стінки сечоводу з пухлиною оперативне лікування доцільно проводити під контролем інтрауретерального ехосканірованія для визначення радикальності видалення пухлини в зоні резекції.
література
Легкість і зручність в новому обсязі.
Біля ліжка пацієнта, в операційній або на спортивному майданчику - завжди готовий до використання.