Аеробні клітини отримують енергію в вигляді молекулярного кисню. У той же час з О2 постійно виникають в невеликих кількостях токсичні речовини. так звані активні форми кисню [АФК (ROS від англ. reactive oxygen species)]. Ці сполуки є сильними окислювачами або вкрай реакційноздатними вільними радикалами (див. С. 20), які руйнують клітинні структури і функціональні молекули. Особливо схильні до АФК-пошкодження еритроцити, для яких через їх транспортної функції характерна висока концентрація кисню.
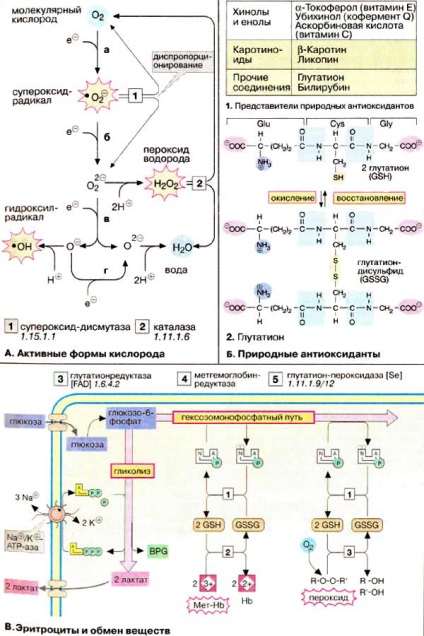
Молекула кисню (О2) містить два неспарених електрона і. таким чином, є бірадікали. Однак неспарені електрони розташовані так, що молекула О2 залишається відносно стабільною. Проте, якщо молекула приєднує додатковий електрон (стадія а), утворюється високо реакційноздатні супероксид-радикал (• О2 -) Наступна стадія відновлення (стадія б) призводить до пероксид-аніони (• О2 2), який легко пов'язує протони і внаслідок цього переходить в пероксид водню (Н2 О2). Приєднання третього електрона (стадія в) веде до розщеплення молекули на іони О 2- і Про -. У той час як О2 - шляхом приєднання двох протонів утворює воду. протонирование Про - призводить до особливо небезпечного гідроксил-радикалу (• ОН). Приєднання четвертого електрона і заключне протонирование Про - закінчується утворенням води.
Освіта АФК каталізують, наприклад, іони заліза. АФК постійно проводяться при взаємодії О2 з ФМН (FMN) або ФАД (FAD) (див. С. 108). Навпаки, відновлення О2 цитохром с-оксидазой нічим не ускладнене (протікає без накопичення АФК), так як цей фермент не звільняє проміжні продукти в середу. Поряд з антиоксидантами (схема Б) є ферменти. які також перешкоджають утворенню вільних АФК. Наприклад, супероксид-дисмутаза [1] викликає ДІСПР-порционирование двох супероксид-радикалів на О2 і менш небезпечний Н2 О2. Останній знову диспропорционирует на О2 і Н2 Про гемсодержащих каталазой [2].
Для захисту від АФК та інших радикалів все клітини містять антиоксиданти. Останні є відновниками. які легко реагують з окислюючими речовинами і внаслідок цього захищають важливіші молекули від окислення. До біологічних антиоксидантів належать вітаміни С і # 917; (Див. Сс. 352. 355), кофермент Q (див. С. 142) і деякі каротиноїди (див. Сс. 58. 352). Утворений при руйнуванні гема білірубін (див. С. 196) також служить захистом від окислення. Особливо важливий глутатіон. трипептид Glu-Cys-Gly, що знаходиться майже у всіх клітинах у високій концентрації. Глутатіон містить нетипову # 947;-зв'язок між Glu і Cys. Відновлювачем тут є тіольний група цістеінового залишку. Дві молекули відновленої форми (GSH. На схемі вгорі) при окисленні утворюють дисульфід (GSSG. На схемі внизу).
Еритроцити також володіють системою (супероксид-дисмутаза, каталаза, GSH), здатної інактивувати АФК і ліквідувати завдані ними пошкодження. Для цього необхідні речовини. щоб забезпечити підтримку в еритроцитах нормального обміну речовин. Метаболізм в еритроцитах по суті обмежений анаеробним гликолизом (див. С. 148) і гексозомонофосфатного шляхом [ГМП (HMW)] (див. С. 154).
Утворений при гліколізі АТФ служить насамперед субстратом Na + / К + -АТФ-ази, яка підтримує мембранний потенціал еритроцитів. При гліколізі утворюється також ефектор 2,3-ДФГ (див. С. 276). У ГМП утворюється НАДФН + Н +. який поставляє Н + для регенерації відновленого глутатіону (GSH) з глутатіон-дисульфіду (GSSG) за допомогою глутатіон-редуктази [3]. Відновлений глутатіон - найважливіший антиоксидант еритроцитів. він служить коферментом при відновленні метгемоглобіну (див. с. 274) в функціонально активний гемоглобін [4]. Важливим захисним ферментом є також селенсодержащих глутатіон-пероксидаза [5].
За допомогою відновленого глутатіону здійснюється детоксикація Н2 О2. а також гидропероксидов, які виникають при реакції АФК з ненасиченими жирними кислотами мембрани еритроцитів.
