Завдання з рішенням. Термодинаміка.
1) Ідеальний газ, маса якого т і молярна маса μ. розширюється і зобарно при деякому тиску. Початкова температура газу Т1. кінцева Т 2. Визначити роботу, що здійснюються газом.
Рішення.
Робота в изобарном процесі
З рівняння Менделєєва-Клапейрона
Виявилося, що роботу в изобарном процесі можна виразити не тільки через зміну обсягу за формулою а й через зміну температури: По-
лучанин результат слід мати на увазі, так як він часто використовується при вирішенні більш складних завдань.
відповідь:
2) Гелій (Не) нагрівається при постійному тиску. При цьому йому повідомлено Q = 20 кДж теплоти. Визначити зміну внутрішньої енергії газу і досконалу їм роботу.
Рішення.
Так як за умовою завдання р = const. то здійснюється газом робота де т - маса газу, μ - його молярна маса, # 8710; T - зміна температури.
Гелій - одноатомний газ, тому його внутрішня енергія а її зміна Порівнюючи формули для роботи А і зміни внутрішньої енергії # 8710; U. отримуємо, що Запишемо перший закон термодинаміки для цього процесу:
Отже, робота Зміна внутрішньої енергії
відповідь:
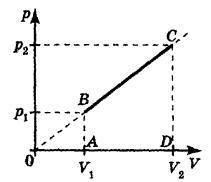
3) Температура деякої маси т ідеального газу з молярною масою μ змінюється за законом де а = const> 0 Знайти роботу, зроблену газом при збільшенні обсягу від V1 до V2. Поглинається або виділяється теплота при такому процесі?
Рішення :
Процес не є ні Ізобаричний, ні ізохорним, ні тим більше ізотермічним. Запи ш їм для будь-якого стану в цьому процесі рівняння Менделєєва-Клапейрона: Так як то після підстановки отримаємо залежність тиску від об'єму у вигляді Графік цієї залежності представлений на малюнку.
Досконала газом робота
Для відповіді на друге питання завдання скористаємося першим законом термодинаміки: Так як газ розширюється, то його робота А> 0. Зміна внутрішньої енергії ідеального газу пропорційно зміні температури: # 8710; U
# 8710; T. Так як і обсяг зростає, то зростає і температура, тому # 8710; U> 0. Тоді і Q> 0, що відповідає поглинанню газом теплоти.
4) При адіабатні стисненні 1 благаючи одноатомного газу зовнішніми силами була здійснена робота А. У скільки разів збільшилася середньоквадратична швидкість молекул цього газу, якщо початкова температура газу дорівнює Т 1?
Рішення.
Перший закон термодинаміки для адиабатного процесу записується у вигляді 0 = # 8710; U + А '. де # 8710; U - зміна внутрішньої енергії газу, А '- робота газу в цьому процесі. Так як газ стискають, то А '<0. в то же время внешние силы совершают положительную работу А, причем А' = -А. Следовательно, Внутренняя энергия 1 моля идеального одноатомного газа поэтому . Отсюда выражаем конечную температуру газа
Середня кінетична енергія молекул де Т - температура. Тоді середньоквадратична швидкість
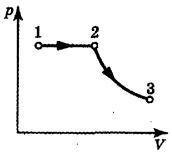
Рішення :
Побудуємо графік залежності тиску від об'єму в осях р, V (малюнок): 1-2 - ізобарно нагрівання, супроводжуване збільшенням обсягу; 2-3 - адіабатне розширення. Робота в адіабатні процесі
тому
отже,
Кількість теплоти, отримане газом в изобарном процесі:
Підставляючи з формули (1) різниця температур знаходимо, що
відповідь:

6) Маса т ідеального газу, що знаходиться при температурі Т. охолоджується ізохорно так, що тиск падає в п раз. Потім газ розширюється при постійному тиску. В кінцевому стані його температура дорівнює первісної. Молярна маса газу μ. Визначити досконалу газом роботу.
Рішення.
Г рафік зазначеного процесу наведено на малюнку. Тут 1-2 - ізохора, 2-3 - ізобара. Шукана робота де А 1 _2 - робота на ділянці 1-2, а А2-3 - робота на ділянці 2-3. На ділянці 1-2 V - const. тому А1-2 = 0. На ділянці 2-3 р = const і Вирази подібного виду перетворюють так, щоб виділити твір тиску на обсяг в стані, в якому задана температура:
З рівняння Менделєєва-Клайперона для стану 3 знаходимо, що
так як Зі стану 1 в стан 3 можна переходити по изотерме 1-3 (в цьому випадку говорять, що точки 1 і 3 розташовані на одній изотерме). Згідно із законом Бойля-Маріотта
Після постановки в формулу (1) отримаємо
відповідь:
1,484,303 унікальних відвідувачів