Мал. 2.4.19. Комбінації скоротних фібрил саркомера при нормальному (В, С) і суперсокращеніі (D, E) скелетного м'яза.
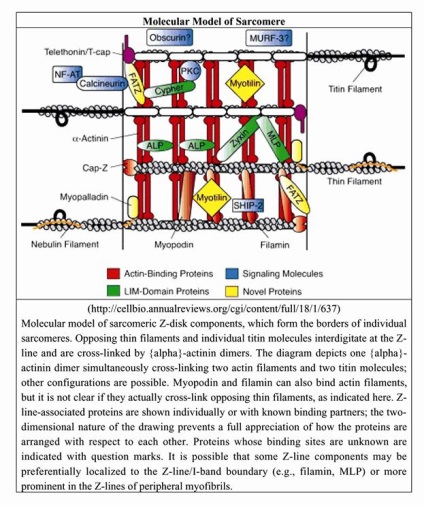
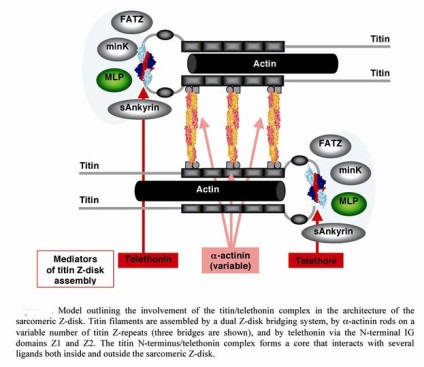
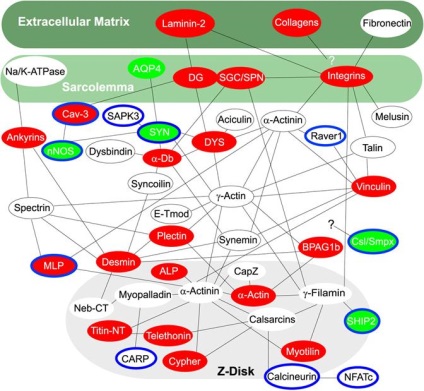
Мал. 2.4.12. Структура Z- диска і ряд білків, що входять до його складу.
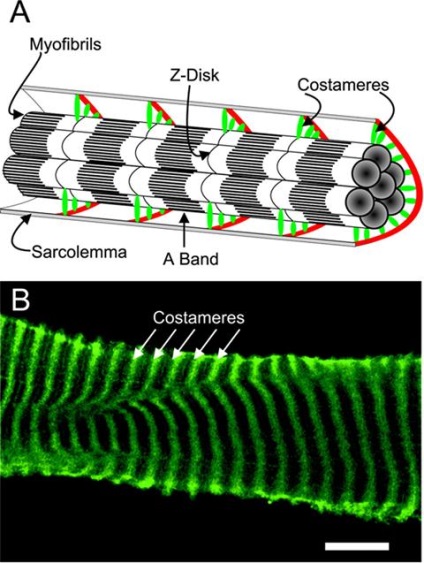
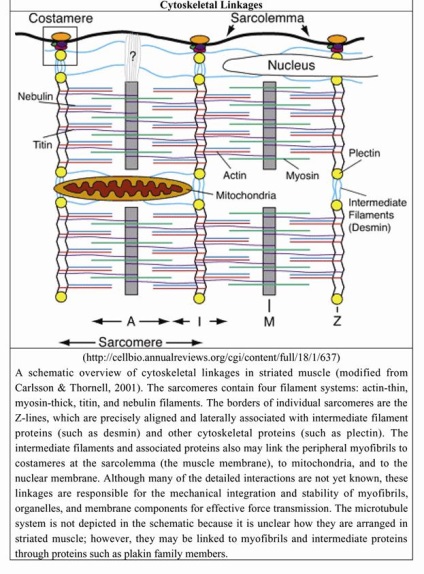
Костамери - система цитоскелетних білків, що утворюють поперечний і поздовжній каркас навколо міофібрили. Костамери забезпечують жорсткість всієї системи міофібрили, пов'язуючи її з сарколеммой.
До складу костамеров входить велика кількість білків: ацікулін. # 947; -актін. # 945; - актінін. анкирин, колаген IV і XII типів. десмин. дістроглікан. дистрофин, інтегрини # 945; 7, і # 946; 1. ламінін-1. Мелузіна, дорівнює-1, спектрин. сінкоілін, сінтрофін, Е-тропомодулін, виментин, вінкулін, талин. і ряд інших білків.
Велика кількість білків з різними назвами, можливо, свідчить, з одного боку, про складність будови цієї структури м'язового волокна і, з іншого, про інтенсивні дослідження в цій області міології і можливе дублювання досліджень і відсутність уніфікованої класифікації білків костамеров і саркомерів.
Питання розвитку тканин в онтогенезі або відновлення тканин в процесі розвитку або пошкодження - найважливіше питання гістології конкретної тканини, в тому числі і м'язової
Поняття камбий прийшло в гістологію з ботаніки і найбільшим фахівцем в питанні визначення поняття камбіального тканин був акад А. А. Заварзін
«Камбіальнгие клітини - це клітини в складі дефінітивних тканин, які зберегли потенції до розмноження і диференціювання, в тому числі і до дивергентной, але в межах певного тканинного типу»
Міогенез соматичної м'язової тканини
Великий внесок у вивчення міогенезе внесли роботи вітчизняних гістологів: Н.Г. Хлопіна, А. А. Заварзін, П.П.Румянцева, А.А.Клішова, Р.К.Данілова і ін.)
Виділяють кілька стадій міогістогенеза:
- стадія миотубах (м'язові трубочки, міотубули)
- молоді і зрілі м'язові волокна
Поперечно смугаста мускулатура утворюється з міогенних стовбурових клітин мезенхимного походження.
Однак шляхи розвитку клітинної і сімпластіческой популяцій в процесі розвитку м'язових волокон різний.
Клітинний компонент - міосаттеліти - одноядерні малодиференційовані клітини, розташовані під базальноїмембраною м'язового волокна, здатні до мітозу і беруть участь в оновленні волокна і їх новоутворенні при регенерації шляхом їх злиття з волокнами на різних стадіях гистогенеза.
Виділяють два типи мілосаттелітов
1 тип - більш диференційовані клітини з активним ядром, вузьким обідком ціпоплазми
2 - тип -коммітірованние напівстовбурові клітини (проміобласти). Саме ця популяція міосаттелітов і є джерелом обох компонентів м'язового волокна і становлять проліферативний пул волокна.
Проіміобласти формують клони перших термінально диференційованих клітин -ініціальних міобластів. які стають центрами формування перших миосимпластами. Нездатні до м ітозу ініціальні міобласти легко зливаються один з одним і утворюють спочатку симпласти, потім миотубах, потім волокно.
З появою перших симпластов і миотубах, поблизу них з'являються одноядерні клітини, представлені іншим клоном проіміобластов, спрямованим на формування клітин - сателітів
Так утворюється ПЕРША ГЕНЕРАЦІЯ м'язових волокон, сформована за участю ініціальних міобластів. вони
Одночасно починає формуватися ДРУГА ГЕНЕРАЦІЯ волокон з прооміоцітов. Вони перебували в стані пролиферативного спокою (стадія G0). Вони проникають між сусідніми первинними миотубах, зливаються, подовжуються і утворюють вторинні миотубах.
Спочатку миотубах розташовуються у вигляді пучків. Оточених загальною сполучно тканинної оболонкою. Далі відбувається поділ миосимпластами і кожен з них покривається базальноїмембраною і ендомізіем. Тоді ж з'являються перші синапси.
Виникнення контактів з моторними нейронами є критичним етапом міогенеза. Після цього настає етап
Вторинна генерація миотубах відділяється при цьому від первинної, утворюючи самостійні одиниці скорочення - м'язові волокна.
Утановлено, що первинна генерація миосимпластами утворює повільні м'язові волокна, тоді як втоічние - швидкі м'язові волокна. Вони, як зазначалося вище, значно відрізняються один від одного за рядом параметрів (див. Табл. ХХ).
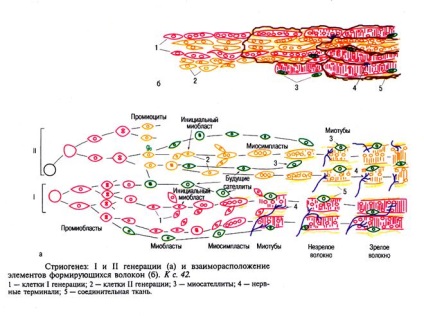
В результаті ембріонального міогістогенеза зі стовбурових клітин міотома сегментированной мезодерми шляхом дивергентной диференціювання розвиваються два взаємодіючих між собою дифферона: камбіальний і сімпластіческій, які формуються паралельно і визначають в постнатальному періоді репаративні властивості
Перший дифферона представлений миосателлитоцитов, вперше описаними A. Mauro (1961), що розвиваються з проміоцітов, локалізуюется між базальної платівкою і сарколеммой м'язових волокон і є морфофункциональной основою камбіального резерву тканинної системи скелетного м'яза. У постнатальному періоді активна проліферація миосателлитоцитов визначається вже на третій день після пошкодження тканини. Після серії мітозів в посттравматичному рабдоміогенезе з них формується популяція міобластів, які, зливаючись, утворюють нові м'язові симпласти ..
Сімпластіческій дифферона також бере участь в репаративної регенерації: поблизу лінії розриву волокна діляться ядра, симпласти колбообразно товщають з формуванням «м'язових нирок», зростаючих у напрямку один до одного з тенденцією до злиття [Однак питання про механізми репаративної регенерації м'язових симпластов до теперішнього часу залишається дискусійним. Це пов'язано з появою даних про можливість реалізації репаративного процесу за рахунок клітин, що утворюються шляхом відокремлення ядерні частини симпластов.

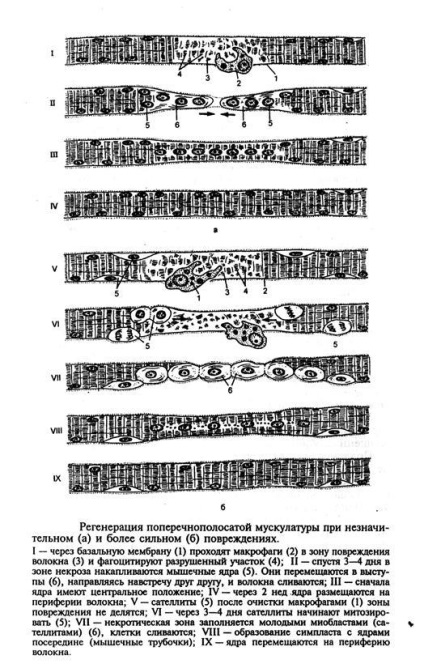
Регенерація скелетних м'язів
Джерелом регенерації м'язового волокна як в разі фізіологічної, так і репаративної регенерації служать міосаттеліти.
Умовами регенерації м'язів є:
- натяг, уставновленіе зв'язків зі скелетом за допомогою зв'язок і сухожиль
- встановлення нервової зв'язку
Стимулом до вступу міосаттелітов в цикл розмноження і диференціювання є мітогени, комплекс біологічно активних речовин, що знаходяться в цитоплазмі м'язового волокна, а також нейротрофические субстанції, що виділяються з нервноих закінчень пророслих до формується нової миотубах аксонів. (Якщо до моменту утворення миотубах не утворюється контакту з нервовими волокнами - процес регенерації зупиняється і відбувається розпад м'язового волокна).
Атрофія м'язових волокон - виникає внаслідок гіпокінезії, голодування або деіннерваціі - м'язові волокна стоншуються, зникає поперечнасмугастість, розщеплюються м'язові волокна. Ендомізій розростається, відбувається заміщення м'язової маси жировою тканиною.
Є спадково обумовлені міоатрофіі: аміотрофічний латеральний склероз, злоякісна міастенія.
Дистрофія - пошкоджується не вся м'яз, а тільки її частину. Можлива компенсація пошкодженої тканини шляхом регенерації. Прикладом м'язової дистрофії (спадкової) - є м'язова дістофіей Дюшена.
Некроз м'язів - загибель м'язової тканини в результаті припинення кровопостачання (інфаркт м'язів), або в результаті поранення. Некроз часто супроводжується жирової дістофіей або ліпоматозом - відкладенням жиру в самій м'язової тканини.
Гіпертрофія - спостерігається при тренуваннях, інших навантаженнях. Важливо відзначити, що при тривалих тренуваннях, їх різке припинення може призвести до атрофічних змін в м'язах.
Регенерація скелетних м'язів має важливе клінічне значення при м'язовій дистрофії і різних травмах, і залежить від камбіального резерву, який формується клітинами-міосателлітамі. Як формують структурний м'язове волокно міобласти, так і клітини-міосателліти утворюються з єдиних м'язових попередників з високим проліферативним потенціалом [2]. Після завершення формування м'язового волокна під час ембріонального розвитку скелетного м'яза клітини-міосателліти розташовуються поза многоядерного волокна і залишаються проліферативно-неактивними. Виживання і поширення цих клітин засноване на експресії транскрипційного фактора Pax7
Було показано, що в покояться клітинах-міосателлітах спостерігається постійна експресія Pax7
У дослідах, проведених в лаб ембріології Інституту Карнегі (США) було показано, що після травми, викликаної кардіотоксіном, у гетерозиготних по алельним варіантів гена Pax7 (Pax7 + / РЄ) мишей на 60-90 добу після народження все м'язові волокна, отримані в результаті регенерації, виявилися # 946; -гал +. Це показує, що основним джерелом регенеруючих волокон є нащадки клітин, що експресують Pax7. Виявилося несподіваним, що і у мишей з повністю виключеним геном Pax7 міофібрили регенерували, причому в волокнах не було виявлено ні мРНК Pax7, ні самого білка Pax7. Таким чином, функціональний білок Pax7 не потрібно для регенерації скелетних м'язів після травми в дорослому віці.
У мутантів Pax7 - / - в зародковій лінії, навпаки, після травми регенерували лише рідкісні тонкі волокна.
В результаті виявилося, що регенерація м'язових фібрил перестає бути залежною від клітин-нащадків Pax7 + попередників після 21 діб постнатального розвитку. Саме на цьому терміні розвитку завершується формування «архітектурного вигляду» м'язового волокна, розподіляються ядра, і відокремлюються мовчазні клітини-міосателліти