Перніциозная анемія (хвороба Аддісона-Бірмера) - захворювання, що характеризується Мегалобластна кроветворением і (або) змінами нервової системи внаслідок дефіциту вітаміну B12, який виникає при важкому атрофічному гастриті. Частота пернициозной анемії складає 110-180 випадків на 100 000 населення. Серед осіб старше 60 років частота досягає 1%. При сімейної схильності до пернициозной анемії контингент хворих був молодшим. Співвідношення хворих жінок і чоловіків постійно становить 10: 7.
Симптоми Хвороби Аддісона-Бірмера:
Хворі пернициозной анемією скаржаться на стомлюваність, сонливість, втрату життєвого тонусу. Двадцять п'ять відсотків хворих скаржаться на болі в роті або в мові, а одна третина - на симетричні парестезії в нижніх і (або) верхніх кінцівках. Спостерігаються деяке зниження маси тіла і втрата апетиту. Набагато рідше зустрічаються порушення ходи, сечовипускання, імпотенція, розлади зору і зовсім рідко - галюцинації і навіть психічні порушення.
При обстеженні зазвичай виявляють лакований мову; в разі більш вираженої анемії - блідість шкіри і деяку желтушность склер. Неврологічне обстеження дозволяє виявити втрату вібраційної чутливості, пасивної рухливості, а іноді й інші ознаки ураження бічних і задніх стовпів спинного мозку.
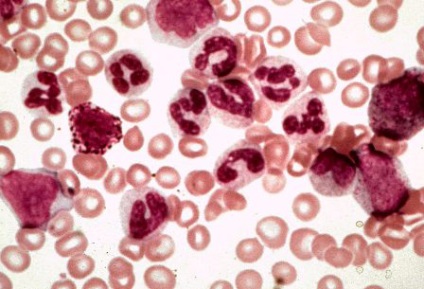
Картина крові при хворобі Аддісона-Бірмера
Причини Хвороби Аддісона-Бірмера:
Три фактори причетні до розвитку перніциозної анемії. а) сімейна схильність, б) важкий атрофічний гастрит. в) зв'язок з аутоімунними процесами.
Минуло понад 130 років з тих пір як Fenwick (1870) виявили у хворих перніциозної анемії атрофію слизової оболонки шлунка і припинення вироблення пепсиногену. Ахлоргідрією і практична відсутність внутрішнього фактора в шлунковому соку характерні для всіх хворих. Обидві речовини виробляються парієтальних клітинах шлунка. Атрофія слизової захоплює проксимальні дві третини шлунка. Велика частина секретирующих клітин або всі вони гинуть і заміщуються слізеобразующімі клітинами, іноді кишкового типу. Спостерігається лимфоцитарная і плазмоцитарна інфільтрація. Така картина, проте, характерна не тільки для пернициозной анемії. Вона виявляється також при простому атрофічному гастриті у хворих без гематологічних відхилень, причому у них навіть через 20 років спостереження не розвивається перніциозної анемії.
Третій етіологічний фактор представлений імунним компонентом. У хворих перніциозної анемії виявлені два типи аутоантитіл: до парієтальні клітини і до внутрішнього фактору.
Методом імунофлюоресценції в сироватці 80-90% хворих перніциозної анемії виявляють антитіла, що реагують з парієтальних клітинах шлунка. Такі ж антитіла присутні в сироватці 5-10% здорових осіб. У жінок похилого віку частота виявлення антитіл до парієтальних клітинах шлунка досягає 16%. При мікроскопічному дослідженні біоптатів слизової шлунка майже у всіх осіб, що мають в сироватці антитіла до парієтальних клітинах шлунка, виявляється гастрит. Введення щурам антитіл до парієтальних клітинах шлунка призводить до розвитку помірних атрофічних змін, значного зниження секреції кислоти і внутрішнього чинника. Ці антитіла, очевидно, грають важливу роль в розвитку атрофії слизової оболонки шлунка.
Антитіла до внутрішнього фактору присутні в сироватці 57% хворих перніциозної анемії і рідко виявляються в осіб, які не страждають на цю хворобу. При пероральному введенні антитіла до внутрішнього фактору пригнічують всмоктування вітаміну B12 внаслідок з'єднання їх з внутрішнім фактором, що перешкоджає зв'язуванню останнього з вітаміном B12.
Такі антитіла присутні не тільки в сироватці, але і в шлунковому соку і виробляються плазматичними клітинами в слизовій шлунка. Так, в шлунковому соку можуть міститися антитіла класу IgA, а в сироватці - класу IgG. У деяких хворих антитіла присутні тільки в шлунковому соку. На підставі даних про виявлення антитіл і в сироватці, і в шлунковому соку можна зробити висновок, що такі антитіла до внутрішнього фактору виявляються приблизно у 76% хворих.
Іншою формою імунної відповіді на внутрішній фактор є клітинний імунітет, що виявляються в тестах інгібіції міграції лейкоцитів або бласттрансформации лімфоцитів. Клітинний імунітет виявляється у 86% хворих. Якщо об'єднати результати всіх тестів, т. Е. Дані про наявність гуморальних антитіл в сироватці, в шлунковому секреті, імунних комплексів в шлунковому секреті і клітинного імунітету до внутрішнього фактору, то виявиться, що імунний компонент присутній у 24 з 25 хворих перніциозної анемії.
За сучасними уявленнями, в лімфоцитах міститься вся необхідна інформація для вироблення будь-яких антитіл, але продукція антитіл контролюється супресорних Т-лімфоцитами. За незрозумілих причин при ряді захворювань В-лімфоцити вислизають з-під контролю супресорних клітин і виробляють «аутоантитіла» проти парієтальних клітин, внутрішнього фактора і досить часто проти клітин щитовидної залози, паращитовидних залоз, наднирників і острівців Лангерганса. Схильність до вироблення аутоантитіл носить сімейний характер, у всякому разі ці антитіла з високою частотою виявляються у здорових родичів, а у деяких родичів розвивається відповідні захворювання. Неясно, що є первинним у розвитку атрофічного гастриту. Антитіла до парієтальних клітин заважають нормальній регенерації слизової оболонки. Не виключено, що саме антитіла запускають атрофічний процес. Стероїди, руйнуючи лімфоцити, сприяють зворотному розвитку процесу і регенерації атрофованої слизової оболонки. Атрофія істотно знижує обсяг шлункової секреції і вироблення внутрішнього фактора.
Антитіла до внутрішнього фактору нейтралізують залишкові його кількості, внаслідок чого всмоктування вітаміну B12 знижується до неадекватного рівня. Виникає негативний баланс вітаміну B12 і повільно розвивається його дефіцит. Припинення всмоктування вітаміну B12 (після тотальної гастректомія) призводить до дефіциту через 5 років, а при меншій мірі негативного балансу потрібно відповідно більший період часу до розвитку манифестного дефіциту.
Лікування Хвороби Аддісона-Бірмера:
Для відновлення запасів вітаміну B12 спочатку зазвичай роблять приблизно 6 ін'єкцій по 1 мг оксікобаламіна. Оксикобаламін затримується в організмі значно краще, ніж ціанокобаламін. Так, з 1 мг введеного оксікобаламіна в організмі залишається близько 70-80%. При введенні порівнянної дози ціанокобаламіну затримується менше 30%. Немає ніяких даних про те, що група ціану молекули цианокобаламіна може надавати шкідливу дію.
Підтримуюча терапія повинна бути спрямована на щодобове споживання близько 5 мкг вітаміну B12, що досягається за допомогою введення один раз на місяць 250 мкг оксікобаламіна. Препарат необхідно вводити протягом усього життя пацієнта. Через 3-6 міс у невеликого числа хворих розвивається дефіцит заліза, про що свідчить падіння MCV нижче 80 фл. У таких випадках показаний короткий курс пероральних препаратів заліза.
Нормалізація показників крові залежить від вихідної тяжкості анемії. У хворих з тяжкою анемією час життя еритроцитів значно знижено, і відновлення нормального значення MCV відбувається особливо швидко (25-35 днів). При слабко вираженої анемії час життя еритроцитів нормально, і відновлення нормального значення MCV займає до 80 днів.
Лікування призводить до усунення невропатії, у всіх хворих зникає нетримання сечі та інші симптоми. Парестезії зникають через 4-6 міс. Зір, порушене внаслідок атрофії зорового нерва. не відновлюється, однак якщо порушення зору обумовлено крововиливами в область жовтої плями, то відновлення відбувається швидко.
Необхідно мати на увазі, що у багатьох хворих з пернициозной анемії через кілька років виявляється мікседема. З 5217 хворих перніциозної анемії у 1,8% був дифузний токсичний зоб і у 2,4% - мікседема. У 9% хворих з первинним гіпотиреозом виявлено перніциозної анемії.
За даними Zamcheck і співавт. у 5,8% хворих в кінцевому підсумку розвивався рак шлунка. У двох скандинавських дослідженнях показано, що частота перніциозної анемії серед хворих на рак шлунка, виявлених при аутопсії, становила 2,1-2,2%.