Освіта вільних радикалів можливо при дії хімічних і фізичних факторів, тому ініціювання радикальної полімеризації поділяють на фізичний і хімічний (дивись схему)
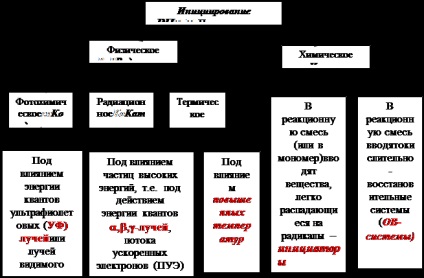
У технології виробництва полімерів переважно поширені хімічні методи ініціювання, коли в реакційну суміш вводять ініціатори (J) - речовини, які в певних умовах легко розпадаються на радикали.
До групи ініціаторів входять наступні речовини (таблиця 10)
Таблиця 10 -Типи ініціаторів радикальної полімеризації
Формула (в загальному вигляді)
Механізм розпаду на радикали
Конкретні представники ініціаторів, умови і механізм їх розпаду наведені в таблиці 11.
Легкий і швидкий розпад ініціаторів на радикали відбувається зі зв'язків кисень - кисень або вуглець - азот, так як ці зв'язки мають найменшої міцністю (енергією зв'язку).
Енергія зв'язку, кДж / моль
Найменші температури розпаду (50 ÷ 85 0 С) і відповідно найменша енергія активації (Е а і) у таких ініціаторів як персульфат амонію, динітрилу азобісізомасляной кислоти, пероксид бензоїлу. Ці ініціатори найчастіше використовуються в радикальної полімеризації.
Окислювально-відновні системи (ОВ-системи) - це комплексні системи, які включають в себе окислювач і відновник (промотор). Роль окислювача найчастіше грають вище наведені ініціатори J (пероксиди, гідропероксиди і ін.). Промотором називають речовину, яка прискорює розпад ініціаторів на радикали. Промоторами в ОВ-системах служать солі металів змінної валентності в нижчого ступеня окислення. такі як хлорид заліза двовалентного FeCl2. хлорид міді одновалентной CuCl, нафтенати кобальту, нафтенати нікелю () і ін. Крім них роль промоторів грають аміни, сульфіти і ін. В лакофарбової промисловості промотори - прискорювачі полімеризації називають сикативи.
Механізм дії окислювально-відновних систем різний. Найпростішою ОВ-системою є реактив Фентона - суміш з пероксиду водню Н-О-О-Н і хлористого заліза FeCl2. У цій системі нестабільний катіон Fe 2+ легко втрачає електрон `е і переходить у вищий ступінь окислення. Fe 3+. Що виділився електрон прискорює розпад пероксиду водню АЛЕ ----- О-Н на іон НО - і радикал НО ·.
Розпад ініціаторів на радикали в присутності ОВ-систем йде дуже швидко і енергія активації стадії ініціювання при використанні ОВ-систем нижче, ніж при використанні тільки одних хімічних ініціаторів (Е а і (ОВ) <Е а и (J) ). Обычно энергия активации окислительно-восстановительного инициирования Е а и (ОВ ) составляет 42÷84 кДж/моль, а энергия активации инициирования с применением только инициаторов Е а и (J) равна 112÷170 кДж/моль.
Ініціювання РП, тобто утворення вільних радикалів йде в два етапи. які схематично можна представити таким чином:
а) освіту радікаловJ · в результаті розпаду молекул ініціатораJ:
б) утворенням активних радикалів ростаJ- М · з молекул мономеровМ:
На прикладі мономера вінілхлориду ця реакція виглядає так:
Початковий етап (а) завжди вимагає витрат енергії активації Е а і, протікає з низькою швидкістю і лімітує весь процес. Не всі радикали ініціатора J · можуть викликати другий етап б) і утворити радикали ростаJ- М ·.
Частина радикалів ініціатора зникає в результаті протікання зворотної реакції рекомбінації J · + J · = J2.
Фотохімічне ініціювання використовується рідше, ніж хімічне. При фотохімічному ініціювання молекули мономера М поглинають енергію квантів (hn) випромінювання з довжиною хвилі 100 нм Енергія активації фотохімічного ініціювання Е а і (ф / г) значно нижче енергії активації чисто хімічного ініціювання Е а і (Е а і (ф / г) <<Е а и (J) ) и близка к 0 (Е а и (ф/х ) » 0 кДж/моль). Вследствие этого фотохимическая радикальная полимеризация может протекать при низких и даже отрицательных температурах. Однак швидкість розпаду мономерів на радикали при дії УФ-променів або видимого випромінювання (ВІ) невисока. Для прискорення фотохімічної полімеризації використовують 2 прийоми: 1. Вводять в мономер речовини - фотоініціатори 2. Вводять в мономер речовини - фотосенсибілізатори. Фотоініціатори - це речовини, які під впливом енергії квантів УФ-або ВІ - випромінювання легше розпадаються на радикали, ніж самі мономери. Фотоініціатор служать галогеналкіли (чотирихлористий вуглець ССl4. 1,2 -тріхлоретанC2 Cl6), металлорганические з'єднання. Механізм дії ССl4 наступний: Фотосенсибілізатори - це речовини, які поглинають і накопичують енергію квантів УФ-або ВІ - випромінювання в більш широкому діапазоні довжин хвиль, ніж сам мономер, потім порціями більшої величини віддають накопичену енергію мономеру. Молекули мономера швидко переходять в збуджений стан і розпадаються на радикали. Роль фотосенсибилизаторов грають речовини, що містять у своїй структурі пов'язану подвійну зв'язок (хромофорні групи) або ароматичні цикли, наприклад, дібензфенон або флуоресцин Механізм дії фотосенсибилизаторов (Ф) наступний: Ф + hn Ф * Ф * + М Ф + М * М * М · + М · Таблиця 11 - Основні групи ініціаторів радикальної полімеризації, механізм і умови їх розпадуСхожі статті