Ознаки нестачі і надлишку азоту для рослин.
При нестачі знижується інтенсивність кущіння, зменшується розмір листя, знижується зростання рослини. У той же час прискорюється репродуктивний розвиток, що призводить до істотного зниження врожайності. Азот реутілізіруется тому ознаки нестачі проявляються на нижніх листках, вони жовтіють, червоніють в залежності від виду. При сильному голодуванні відмирають. Надлишок азоту призводить до інтенсивного росту вегетативної маси, формуються широкі соковиті листя темно-зеленого кольору. Затягується фаза вегетації, подовжується вегетаційний період, сповільнюється утворення репродуктивних органів, і дозрівання рослини.
Форми азоту в ґрунті
Азот в грунтах міститься в органічній і мінеральній формах, переважає органічний азот, який становить 97-99% загального змісту. Він не доступний для живлення рослин. Органічний азот знаходиться в складі гумусу, деяка частина в м.о. негумусірованних залишках живих організмів.
48. Агрохімічні показники, що характеризують забезпеченість грунтів азотом. Принципи методів визначення вмісту нітратного, амонійного і легкогідролізуемого азоту в грунтах, нітріфікаціонной здатності грунтів.
Жоден з цих показників не є достатньо надійним, що б отримати широке поширення в практиці землеробства.
^ Визначення змісту амонійного азоту (N-NH4) в грунті по Арінушкіной
Принцип методу: катіони амонію витісняються з грунтового по-глощающего комплексу за допомогою 2% розчину хлориду калію (КCl) при со-відношенні грунту до розчину 1:10. При цьому відбувається наступна реакція:
При взаємодії утворився хлориду амонію з реактивом Несслера (лужним розчином K2HgJ4) розчин забарвлюється в жовтий колір, так як утворюється забарвлене відповідним чином комплексне соеди-ня - йодистий меркураммоній (NH2Hg2OJ):
Інтенсивність забарвлення пропорційна концентрації амонійного азоту в розчині. Оптична щільність розчину, що характеризує інтенсив-ність забарвлення, визначається на фотоелектроколориметри. При порівнянні опти-чеський щільності досліджуваного і зразкових розчинів визначається концен-трація амонійного азоту в витяжці.
Заважає вплив катіонів Са і Mg усувається додаванням сег-Нетов солі.
^ Визначення змісту легкогідролізуемого азоту в грунті по Тюріну-Кононової
Принцип методу: лепсогідролізуемий азот витягується з грунту 0,5 н. розчином сірчаної кислоти (H2SO4). При цьому в витяжку переходить азот низькомолекулярних орга-нічних сполук, гідролізуються під дією сірчаної кислоти, а також амонійна і нітратна форми азоту.
Нітратний азот відновлюється до аміаку нагріванням отриманої витяжки до кипіння з додаванням суміші металевих заліза і цинку (співвідношення Fe: Zn = 1: 9) У результаті таких реакцій:
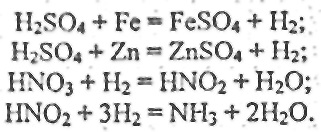
Азот амінокислот, амідів та інших органічних сполук, що містяться в рас-творе, переходить в форму аміаку під дією концентрованої H2SO4 і 10% розчину біхромату калію (К2Сr2О7) при кип'ятінні, в процесі якого відбувається їх разложеніe c виділенням кисню:
Вирізняється кисень окисляє вуглець і водень органічних сполук до вуглекислого газу і води відповідно, а сірчистий газ (SO2) переводить азот аминогрупп
Аміак, що утворюється при відновленні нітратів і розкладанні органічних з- єднань, зв'язується сірчаною кислотою в формі сульфату амонію:
При взаємодії останнього з 40% розчином гідроксиду калію (КОН) відбувається із-дит виділення аміаку:
який відганяється на апараті Кьельдаля і поглинається певною кількістю 0,02 і. розчину H2S04:
49. Перетворення азоту в грунтах. Основні процеси, значення їх у зв'язку з живленням рослин і застосуванням добрив, регулювання агротехнічними прийомами.
Амонійний азот утворюється в результаті процесу аммонификации, тобто розпаду азот містять органічних сполук до NH3.
схема аммонификации
Гумус, білки амінокіслоти, аміди NH3
У аммонификации беруть участь різні групи аеробних і анаеробних мікроорганізмів - бактерії, гриби, актиноміцети. Тому аммонификация протікає в присутності кисню і без нього, і при різній реакції середовища. Різко знижується аммонификация тільки в анаеробних умовах сильнокислому або сільнощелочних грунтів.
Швидкість аммонификации залежить також від температури і вологості грунту. Утворений NH3 реагує з органічними і мінеральними кислотами ґрунтового розчину.
При дисоціації солей NH4 поглинається ППК, і досить міцно закріплюється.
ППК) H NH4HCO3 = ППК) H Mg (HCO3) 2
тобто амонійний азот міцно закріплюється в ППК, але залишається доступним для рослин.
Процес нітрифікації.
Нітратний азот утворюється в результаті процесу нітрифікації. Окислюється NH3 до нітратів під дією специфічних аеробних бактерій - нитрификаторов.
Виділяться 2 стадії процесу:
1) окислення аміаку до азотистої кислоти бактеріями Nitrosamonas, Nitrosocystis і ін.
2NH3 3O2 = 2HNO2 2H2O
2) окислення азотної кислоти до азотної бактеріями роду Nitrobacter
Утвориться азотна кислота нейтралізується катіонами Са, Mg та ін. Знаходяться в грунтовому розчині або ППК.
2HNO3 Ca (HCO3) 2 = Ca (NO3) 2 2H2CO3
Ca 2H
ППК) H nHNO3 = ППК) H Ca (NO3) 2
Mg Mg
Всі солі азотної кислоти добре розчинні у воді, крім того нітрати негативно фізично поглинаються грунтом. Нітратний азот завжди знаходиться в ґрунтовому розчині володіючи високою рухливістю. При вирощуванні культур нітрати відразу поглинаються рослинами. Накопичення нітратів в значних розмірах до 300 кг / га за літо відбувається тільки в чистому пару. Оптимальні умови для нітрифікації: хороша аерація, вологість 60-70%, t = 25-32, близька до нейтральної рН, такі умови є оптимальними і для рослин. Таким чином інтенсивне накопичення нітратів свідчить про підвищений накопиченні його в грунті.
Продуктами аммонификации і нітрифікації є форми мінерального азоту, тому значення має регулювання темпів цих процесів. Кількість органічної речовини бере участь в аммонификации можна підвищити внесенням органічних добрив. Реакцію середовища можна оптимізувати вапнуванням. Водно-повітряні властивості і температурний режим обробкою і структурою посівних площ. На окультурених добре удобрених грунтах ці процеси протікають з великою швидкістю і багато в чому задовольняють потребу с / г рослин в азоті. Нітрифікація може грати і негативну роль тому нітрати дуже рухливі і в значній мірі вимиваються.
Процеси біологічної і непрямої денітрифікації.
Денітрифікація - це відновлення нітратного азоту до газоподібних сполук (N2O, NO, NO2) за участю анаеробних бактерій денітрифікатори Bact. Denitrificans.
Найбільш інтенсивно протікає денітрифікація в анаеробних умовах перезволожених або переущільнених грунтів при лужної реакції середовища рН = 6,5-7,5 і надлишку органічної речовини багатого вуглеводами.
Разом з тим йде і при оптимальних рН, вологості і аерації, тому що всередині ґрунтових мікроагрегатів завжди існують анаеробні мікрозонах. Утворені гази основні з яких N2 і N2O випаровуються з грунту обумовлюючи тим самим втрату азоту. Тому необхідно прагнути до зниження інтенсивності денітрифікації використовую агротехнічні спрямовані на підтримку в грунті оптимального водно-повітряного режиму.
На ряду з біологічної виділяється і непряма хемоденітріфікація - це утворення газоподібних форм азоту в результаті протікають в грунті хімічних реакцій. Істотні втрати відбуваються при розкладанні HNO2 в кислому середовищі рН<5, с выделением окиси азота.
3HNO2 HNO3 H2O 2NO
Процеси іммобілізації мінерального азоту і Необмінна поглинання (фіксації) амонію.