отримання коричної к-ти або її похідних взаємодій. ароматич. альдегідів з ангідридами карбонових кислот у присутності. слабких основ (лужних солей карбонових кислот, третинних амінів і ін.):
Р-цію здійснюють зазвичай при т-ре 80-180 0 C. Електро-ноакцепторние заступники (CN, COOCH3. Cl, Br, NO2) в ароматич. альдегіди прискорюють р-цію, електронодонорні (напр. алкіл) -замедляют (якщо заступник-NR'2. то П. р. не йде). Як кислотної компоненти м. Б. використані разл. ангідриди, що містять в a-положенні до карбонільної групі атоми H. Вихід р-ції 50-80%. Аліфатіч. альдегіди в умовах П. р. реагують з дуже маленьким виходом.
Вінілог бензальдегида (коричнева альдегід) реагує з оцтовим ангідридом з утворенням b-стірілакріловой к-ти:
Механізм П. р. обумовлений СН-кислотними св-вами ангідриду карбонової к-ти і включає стадію його еноліза-ції:
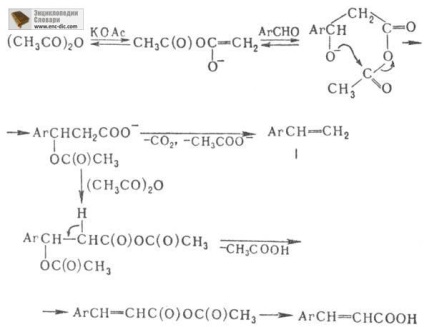
У деяких випадках (гл. Обр. В залежності від природи активують заступників в бензольному кільці) арил-етилен (ф-ла I) може стати головним продуктом. Ароматіч. діальдегіду (фталевий, ізофталеву і тере-фталевий) утворюють фенілен- біс -акрилові к-ти, напр .:
При використанні в р-ції саліцилового альдегіду утворюється кумарин:
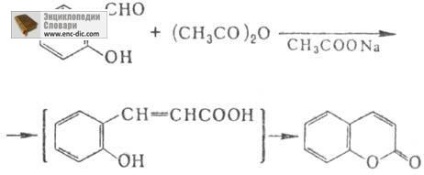
Для синтезу a-арілкорічних к-т використовують також оцтовий ангідрид і сіль лужного металу відповідної карбонової к-ти (модифікація Ольялоrо):
В умовах П. р. похідні коричної к-ти утворюються при взаємодій. бензальдегида з солями дикарбонових к-т, напр .:
Р-цію ароматич. або аліфатіч. альдегідів з Na-сіллю бурштинової к-ти або бурштиновим ангідридом використовують для отримання параконових к-т (модифікація Fіттіга), напр .:
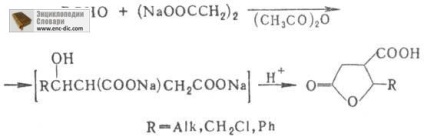
В р-цію, подібну П. р. вступають гетероароматіч. альдегіди, напр. фурфурол, 2-тіофенкарбальдегід і ін. Р-ція відкрита У. Г. Перкін-старшим в 1868.
Літ .: Органічні реакції, пер. з англ. зб. 1. M. 1948, с. 267-344; Хімічна енциклопедія. - М. Радянська енциклопедія Под ред. І. Л. Кнунянц 1988