Перш ніж позначити системні ефекти застосування статевих стероїдних гормонів, слід ще раз зупинитися на їх спектрі в організмі жінки. Це, в першу чергу, жіночі статеві гормони фолликулиновой фази менструального циклу: естрогени (естрон - Е. естрадіол - Е2 і естріол - Е,), які виробляються гранулезнимі клітинами яєчників, а також утворюються в результаті ароматизації андрогенів в жировій тканині; андрогени - чоловічі статеві гормони (тестостерон і андростендиол), синтезовані в жіночому організмі тека-клітинами яєчників і надниркових залоз, і, нарешті, прогестерон, гормон лютеїнової фази менструального циклу, який називають також гормоном жовтого тіла, вказуючи при цьому на місце його синтезу. Як відомо, основною точкою докладання статевих стероїдних гормонів є, в першу чергу, яєчники і матка. Збалансоване дію цих гормонів направлено на дозрівання яйцеклітини і овуляцію, а також подальшу імплантацію заплідненої яйцеклітини в підготовлений ендометрій порожнини матки і подальше виношування вагітності. Органом-мішенню для статевих стероїдних гормонів є також молочна залоза - її протоки і альвеоли, функціонування яких забезпечує процес лактації, тобто функцію вигодовування потомства. Крім того, впливаючи на тканину мозку, статеві стероїдні гормони впливають на функціональний стан центральної нервової системи (емоції, пам'ять, мислення), в тому числі забезпечуючи лібідо, що грає певну роль в реалізації репродуктивної функції. Таким чином, саме збалансоване взаємодія статевих стероїдних гормонів, здійснюване при взаємозв'язку з рядом гормонів тропів, факторів росту та інших біологічно активних речовин (біогенних амінів), забезпечує нормальну репродуктивну функцію жінки, тобто запліднення, виношування вагітності, народження і годування дитини, а також, відповідно, стан функціонального здоров'я органів-мішеней - матки, яєчників і молочних залоз і, як показали дослідження останніх років, в значній мірі центральної нервової системи.
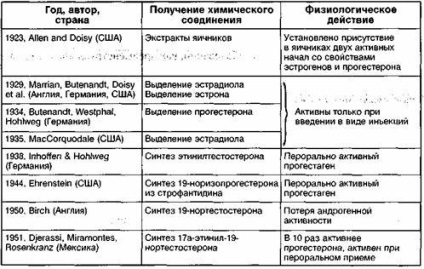
Науковий підхід до ендокринологічним аспектам репродукції у жінок бере початок в першому десятилітті минулого століття, коли експериментально було доведено ендокринна функція яєчників (табл. 1).
Підстава сучасним уявленням про оваріальних стероїдах було покладено Е. Allen і Е. Doisy (1923), які чітко показали, що яєчник виробляє два різних речовини: одне - відповідальне за ріст і нормальний стан статевих органів, а друге - за секреторні зміни в ендометрії і збереження вагітності.
Згодом майже одночасно в кількох лабораторіях було виявлено та ідентифіковано три основних естрогену людини: естрон, естріол і 17р-естрадіол - найбільш важливий і біологічно активний естроген, який був синтезований з сечі лошат кобил лише в 1935 році. У 1934 р A. Butenandt і V. Westphal вперше виділили речовину, що володіє прогес-тероновой активністю, a Slotta точно розшифрував структуру прогестерону. За методику синтезу прогестерону A. Butenandt і його група в 1935 р були удостоєні Нобелівської премії.
Подальше вивчення процесів синтезу статевих стероїдних гормонів і їх метаболізму, а також експресії рецепторів до цих гормонів в різних органах і тканинах жіночого організму і особливостей взаємодії стероїдів з цими рецепторами забезпечило розкриття механізмів розвитку ряду дис-гормональних захворювань у жінок і створення медикаментозних препаратів, що володіють властивостями статевих стероїдних гормонів, що, відповідно, надало можливість патогенетичної терапії цих захворювань.
Системні ефекти естрогенів, що застосовуються в замісної гормональної терапії (ЗГТ), детально викладені в розділі патології клімактеричного періоду. Там же визначено принципи диференційного підходу до застосування естрогенів. Системна дія синтетичних естрогенів, що застосовуються в комбінованих оральні контрацептиви (КОК), відображено в таблицях 2 і 3. Представлені дані, на нашу думку, можуть бути корисні клініцисту при оцінці тих чи інших лабораторних досліджень у жінок, які застосовують КОК.
Що стосується прогестерону, то сама назва гормону другої фази менструального циклу забезпечує його основне призначення: прогестерон - "pro gesta-tio", тобто "Для вагітності". Так, дефіцит прогестерону часто має місце при безплідді і невиношуванні, і, відповідно, саме ці патологічні стани в першу чергу є показанням до застосування прогестагенів.
Відомо також, що естрогени забезпечують процес проліферації ендометрія, а прогестерон - його секрецію в ході підготовки до імплантації заплідненої яйцеклітини. Таким чином, відносний або абсолютний дефіцит прогестерону обумовлює розвиток гіперпроліферативних процесів ендометрія. Саме гіперпластичні процеси ендометрія, а також стану з високим ризиком їх розвитку є другою за значимістю групою показань до застосування прогестагенів.
Таким чином, сьогодні сформульовані основні показання до застосування прогестагенів в гінекологічній практиці:
• Не виношування вагітності, безпліддя (особливо при недостатності II фази менструального циклу)
• Гіперпластичні процеси ендометрія
• Міома матки
• Протекторна вплив на ендометрій при замісної гормональної терапії
• Профілактика "синдрому спалаху" при застосуванні агоністів ГнРГ (за даними літератури відзначається в 10-15% випадків за рахунок кратковременногоповишенія рівня естрогенів на 10-12-й день після 1-ої ін'єкції агоніста і проявляється у вигляді межменструал'них кров'яних виділень або деякого посилення болів при ендометріозі)
• Передменструальний синдром
• Деякі види дисгормональних захворювань молочних залоз (ДЗМЖ)
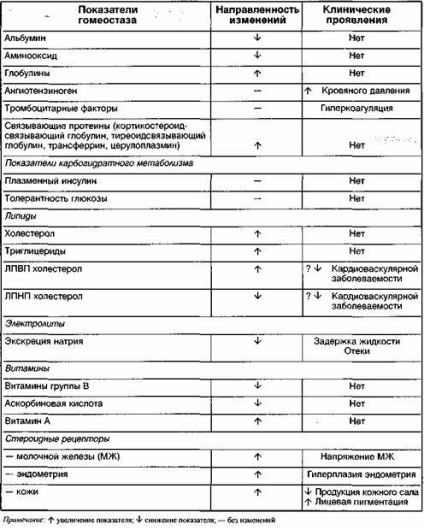
Примітка: I s зростає; ^ Злегка зростає; Ф знижується; v * злегка знижується; - без змін
Наявність в арсеналі лікаря чималого вибору препаратів, що мають прогестагенних дією, але кілька різних за як хімічною структурою, так і особливостями біологічних ефектів, зумовлює необхідність розробки принципів диференційованого підходу до вибору конкретного препарату при тій чи іншій патології з урахуванням індивідуальних особливостей організму кожної конкретної жінки.
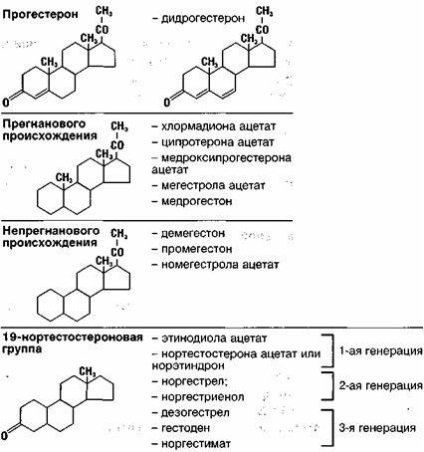
Спектр прогестагенів, що застосовуються сьогодні в клінічній практиці, включає природні і синтетичні препарати (табл. 4).
Таблиця 4Прогестагени, що застосовуються в гінекологічній практиці
Існує тільки один природний прогестаген, що має біологічне значення і застосовується в клінічній практиці, - прогестерон.
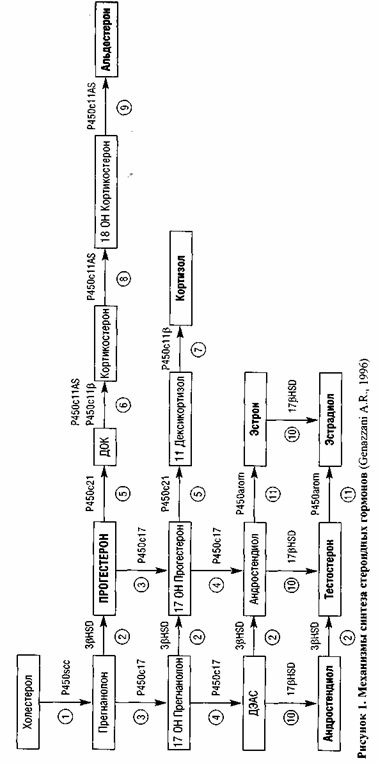
Маючи здатність зв'язуватися тільки з прогестеронові рецепторами (табл. 5), цей прогестаген не викликає множинних системних ефектів в організмі жінки, проте застосування його великих доз за рахунок впливу на ензими, що беруть участь у метаболізмі стероїдів (див. Рис. 1), забезпечує антимінералокортикоїдними, а також слабке антиандрогенное і глю-кокортікоідное дію (табл. 6).
Наявність в даний час микронизированной форми прогестерону (Утрожестан) забезпечує можливість як перорального, так і вагінального його застосування.
Таблиця 5Способность різних типів гестагенів взаімодействоватьс прогестеронові рецепторами для андрогенів
В даний час є також можливість застосування прогестерону трансдермально у вигляді гелю (Прожестожель). Трансдермальне застосування прогестерону забезпечує надходження гормону безпосередньо в кровоносне русло, минаючи первинний метаболізм в печінці. Це дуже важливо для пацієнток з патологією печінки і шлунково-кишкового тракту. Однак для досягнення в сироватці крові концентрації гормону, необхідної для лікування більшості патологічних станів, в терапії яких використовуються прогестагени, необхідно було б застосування досить великих доз Про-жестожеля. Саме тому найбільш широке клінічне застосування цей препарат отримав в лікуванні ряду дисгормональних захворювань молочних залоз, з огляду на наявність локального біосинтезу естрогенів, що більш докладно висвітлено в розділі, присвяченому патології молочної залози.
Проізводние19-нортестостерона
Що стосується наявного на сьогодні різноманіття синтетичних прогестагенів, то класифікуються вони по будові вихідної стероидной молекули, з якої їх отримують (див. Табл. 4), і, відповідно, мають різну здатність зв'язуватися з різними рецепторами (див. Табл. 5, 6) .
Першим з'єднанням, синтезованим С. Djerassi et al. (1951), був 17а-етініл-19-нортестостерон (норетіндрон), який став родоначальником цілого покоління ге стагенних 19-норстероидов і володів деякими естрогенними властивостями.
Наступним відкриттям став норгестрел (похідне 19-нортестостерона 2-ий генерації), а потім і левоноргестрел, які є одними з найбільш сильних норстероидов, активних при пероральному застосуванні і, як уже згадувалося, при локальному введенні в порожнину матки.
Заміщення метильної групи у С ,, - молекули норгестрела призвело до утворення іншого сильного прогестагену 3-ої генерації - дезогестрела, який входить до складу ряду вироблених в Європі пероральних контрацептивів.
Не менш цікаво отримання прогестагенів, структурно пов'язаних з прогестероном. Відомо, що прогестерон втрачає свою біологічну активність при приєднанні гідроксильної групи до С17 в а-положенні. Однак що утворюється речовина - 17а-гідроксіпрогестерон після Етері-ції дає 17а-ацетоксіпрогестерон - помірно активну гестагенну з'єднання. Воно стало вихідним для подальшого отримання ряду важливих речовин. Подовження алкільного ланцюга 17а-гідрокси-ефірів дозволило отримати довготривалі прогестагени для парентерального застосування, такі як 17а-гидроксипрогестерона валерат і 17а-гидроксипрогестерона капронат. В результаті модифікації С6 -молекули гідроксіпрогесте-рона ацетату синтезовані потужні пероральні гестагени. Один з 6-метил-аналогів - медроксипрогестерона ацетат (Провера, Депо-провера).
Окремо слід зупинитися на Неацетильований прегнановом похідному, структурно пов'язаний з прогестероном, - дидрогестерон (Дуфа-стогін). Будучи за хімічною структурою максимально схожим з натуральним прогестероном (рис. 2), цей прогестаген за рахунок наявності всього однієї додаткової подвійний зв'язку має більшу в порівнянні з прогестероном здатністю зв'язуватися з прогестеронові рецепторами (див. Табл. 5) і надавати більш виражений прогестагенних ефект при відсутності впливу на андрогенні і естрогенні рецептори. Антимінералокортикоїдними дію дидрогестерона забезпечує стабільність або навіть зниження маси тіла при застосуванні препарату як в якості монотерапії, так і в складі комбінованих гормональних препаратів для лікування клімактеричних порушень.
Таким чином, різноманіття наявних на сьогодні натуральних і синтетичних прогестагенів, як уже зазначалося, вимагає індивідуального підходу до вибору препарату в кожному конкретному випадку
Диференційовані підходи до застосування прогестагенів визначаються:
• взаємодією зі специфічними прогестеронові рецепторами - ПРАіПРВ;
• взаємозв'язком з неспецифічними рецепторами - андрогенів, естрогенів, кортизолу, альдостерону;
• впливом на ензими, які беруть участь у метаболізмі стероїдів, - сульфа-таза, ЗР-гідростероід дегидрогеназа, 17Р-гідростероід дегидрогеназа, 5а-редуктаза, ароматаза, каталаза, сульфотрансфераза.
При визначенні здатності взаємодії з рецепторами статевих стероїдних гормонів слід враховувати розглянуті субтипу як про-гестеронових, так і естрогенних рецепторів (рис. 3).
Малюнок 3. Субчіпи рецепторів естрогену і прогестерону
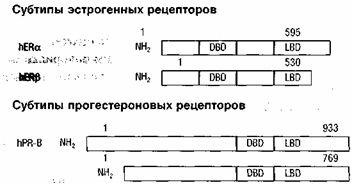
Відмінності ж в експресії субтипов естрогенних рецепторів в різних органах і системах (табл. 7), а також здатність різних видів синтетичних прогестагенів надавати стимулюючу дію на ці рецептори (рис. 4) забезпечують можливість диференційованого підходу до вибору виду гормональних препаратів, у тому числі і контрацептивів, особливо у пацієнток з екстрагенітальною патологією і високим онкоризику.
Таблиця 7 Експресія естрогенних рецепторів аїр в різних органах і системах
Естрогенні рецептори а
♦ напруга в грудях
Метаболічні побічні ефекти прогестагенів відзначаються, як правило, при тривалому застосуванні високих доз препаратів, і механізми їх розвитку в даний час остаточно не вивчені.
Попередження згаданих ефектів особливо важливо в лікуванні пацієнток з порушенням ліпідного обміну, інсулінонезалежним цукровим діабетом, ожирінням або підвищеним ризиком розвитку цих станів. Для даного контингенту виняткове значення має вибір оптимальної дози і тривалості лікування з урахуванням вищевказаних принципів, а також вибір типу прогестагенів. Так, клінічними дослідженнями доведено відсутність будь-якого впливу на ліпідний метаболізм дидрогестерона (дуфастон) в дозі до 30 мг на добу, а також індиферентність щодо карбогідратного метаболізму 30 мг дидрогестерону і 10 мг норетистерону при тривалому застосуванні.
Фізікал'ние побічні ефекти прогестагенів обумовлені їх андро-генним дією за рахунок зв'язування з рецепторами для андрогенів (див. Табл. 5) - це, частіше за все, акне, себорея, алопеція, а також за рахунок міні-ралокортікоідного ефекту, обумовленого особливостями метаболізму прогестагенів (див . рис. 1) - це, в першу чергу, набряки, збільшення ваги, здуття живота, головний біль. У таких випадках рекомендується підбір препаратів з урахуванням їх можливих системних ефектів (див. Табл. 5) - застосування прогестагенів, що володіють антимінералокортикоїдними дією (дроспіре-нон, дидрогестерон), а також що не володіють андрогенним впливом (дезоге-стріл, гестоден, дидрогестерон) або забезпечують антиандрогенное вплив на організм (ципротерону ацетат, дієногест).
Розвиток психопатологічної складової синдрому непереносимості гестагенів обумовлено особливостями їх метаболізму в ЦНС. В результаті
обміну ряду синтетичних прогестагенів утворюються прегнанолон і Прегна-нолон сульфат, які є антагоністами ГАМК-рецепторів, тобто блокують як А, так і В ГАМК-рецептори. Наявність ГАМК В-рецепторів не тільки в ЦНС, а й в інших органах і системах може в деякій мірі пояснити поліморфізм клінічних проявів синдрому непереносимості прогестагенів.
Крім впливу на рецептори ГАМК, прегнанолон впливає на моноаміни, підвищуючи активність моноаміноксидази і катехол-О-метілтранс-ферази, тобто ферментів, що інактивують катехоламін (норадреналін, адреналін і дофамін) і індоламін (серотонін), а також збільшує зворотне захоплення серотоніну. Цим пояснюються депресивні стани, що розвиваються на тлі застосування ряду синтетичних прогестагенів.
У таких випадках доцільно віддавати перевагу застосуванню натурального прогестерону, який метаболізується в аллопрегнанолон і забезпечує м'який седативний ефект (при відсутності порушень метаболізму стероїдів в ЦНС), або дидрогестерона, дії метаболітів якого на ЦНСне відзначено.
Таким чином, визначаючи режим, схему і вид прогестагенів в лікуванні гінекологічних захворювань, клініцисту слід враховувати особливості місцевого та системного впливу призначуваного препарату і керуватися сучасними принципами застосування гормональних препаратів у лікуванні дисгормональной патології:
• селективність і детермінований короткий період дії призначуваних препаратів;
• висока компетентність лікаря в даній проблемі;
• комплаентность терапії, що складається в адекватної освіченості пацієнтки і найбільш зручною використанні препаратів, зручних в застосуванні.
Популярне:
ЛІКУВАННЯ ЖІНОЧИХ ЗАХВОРЮВАНЬ nbspnbspnbspnbspnbspnbspnbspnbsp ЛІКУВАННЯ СУГЛОБІВ nbspnbspnbspnbspnbspnbspnbspnbsp ЛІКУВАННЯ ЗУБОВ