Уявіть собі інтелектуальні медичні імплантати, здатні, перебуваючи в організмі, постійно відстежувати свій стан і автоматично реагувати на такі зміни, як інфекція, виділенням антибактеріальних препаратів. Завдяки нанотехнологій дослідження в галузі медицини швидко наближаються до цієї мети.
Ринок медичних імплантуються пристроїв величезний і продовжує швидко зростати - тільки в США він досяг річного обороту в 23 мільярди доларів і, як очікується, буде щорічно збільшуватися на 10 відсотків протягом найближчих декількох років. Серед лідерів продажів - кардіологічні дефібрилятори і ресінхронізатори, кардіостимулятори, ортопедичні імпланти для лікування хребта, протези великих суглобів, інтраокулярних лінз і косметичні імплантати. Щорічно тільки в США проводиться майже 500000 операцій по протезуванню стегнових і колінних суглобів, і приблизно такій же кількості пацієнтів необхідна кісткова реконструкція через травми або вроджених дефектів. Щороку 16 мільйонів американців втрачають зуби і потребують зубних імплантатах.
Головною проблемою, з якою вченим і лікарям доводиться стикатися на шляху до успішної і довгострокової службі штучних суглобів, залишається знос і інфікування імплантатів. Дослідження показали, що в процесі експлуатації ортопедичних імплантатів утворюються дрібні частки їх матеріалів, як металів, так і пластмас. Велика кількість таких частинок викликає каскад подій, здатний, в кінцевому підсумку, зруйнувати кістка навколо імплантату (процес, відомий як остеолізис). Виник в результаті «розхитування» імплантату призводить до того, що штучний суглоб не може виконувати свою функцію. Діагностика стану імплантату грунтується на рентгеноскопії і інших методах візуалізації. Ці технології недостатньо чутливі, не дають картини в режимі реального часу і вимагають госпіталізації хворого. Хірургічні операції по заміні таких протезів не тільки більш складні і дороги, ніж первинне протезування суглобів, а й менш ефективні.
Нове дослідження показує, що якість кісткових імплантатів можна значно поліпшити. Завдана на їх поверхню плівка з поліпіррола (polypyrrole) може використовуватися в якості електрично контрольованого пристрою для виділення лікарських препаратів. Використовуючи антибіотики або протизапальні засоби, введені в полімерне покриття методом електролітичного покриття, вчені Університету Брауна (Brown University) продемонстрували, що ці препарати можуть виділятися з поліпіррола «на вимогу» - при подачі напруги - і контролювати поведінку клітин, тобто пригнічувати запалення і вбивати бактерії .
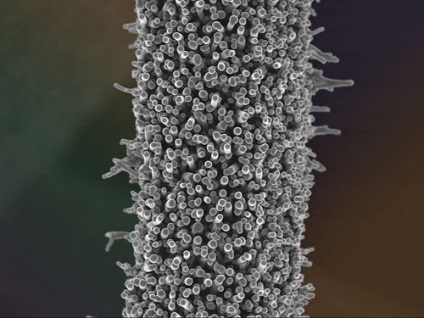
Поліпіррол - проводить полімер, покритий вуглецевими нанотрубками (фото: EMSL / Flickr)
«Поліпіррол - традиційно проводить полімер, який можна синтезувати електрохімічними методами у вигляді тонкої плівки на провідних матеріалах», - пояснює Томас Дж. Вебстер (Thomas J. Webster). Можливість його використання була вивчена в області захисту від корозії і розробки електродних покриттів, електрохімічних біосенсорів, напівпровідникових приладів, а також в біоелектроніці та інших областях. Однак хоча він і зарекомендував себе як перспективний матеріал зі значними можливостями в галузі біомедицини та контрольованої доставки ліків, його потенційна роль в зниженні інфікування і придушенні запальних реакцій в ортопедії досліджена недостатньо.
Ця робота є продовженням попередніх досліджень наномедіцінской лабораторії Вебстера, що продемонстрували, що такі наноструктурні матеріали можуть впливати на зростання кістки і сприяють йому.
Для створення своїх полімерних покриттів вчені спочатку виростили багатошарові вуглецеві нанотрубки (близько 55 нм в діаметрі) на анодируваному нанотрубчатом титані методом хімічного осадження з парової фази (chemical vapor deposition, CVD) з кобальтом як каталізатор. Мономери поліпіррола були окислені або антибіотиками, або дексаметазоном до проведення електрохімічної полімеризації поліпіролла навколо вуглецевих нанотрубок.

Зліва - поліпіррол, електроосадження на звичайному титані,
праворуч - на багатошарових вуглецевих нанотрубках
(Фото: Webster Lab, Brown University)
«У нашому останньому дослідженні аніонні лікарські препарати, пов'язані електростатично всередині тонкої поліпоррольной плівки, виділялися при додатку негативного напруги», - пояснює Вебстер. «Протягом перших п'яти циклів ми спостерігали вихід аніонних молекул з тонкої поліпіррольной плівки і їх зворотне переміщення, викликані постійним процесом відновлення і окислення. Піки вивільнення пеніциліну / стрептоміцину, обумовлені відновленням препаратів, зникли через 15 циклів циклічної вольтамперометрії. Пік відновлення дексаметазону спостерігався і після 25 циклів і зник після 40 циклів ».
Збільшення кількості вивільняються препаратів після електричного збудження було значним до 5 циклів. Сукупна вивільнення пеніциліну / стрептоміцину і дексаметазону було близько до 80 відсоткам від вихідних кількостей препаратів, і наступні цикли не викликали їх вивільнення.
Хоча вчені встановили, що при більш високих напругах або при більш тривалих періодах його подачі поліпіррол може бути сверхокіслен і втрачає свою електричну активність, вуглецеві нанотрубки підтримують і пролонгують його електроактивних завдяки своїм чудовим провідникові властивостями.
Вебстер зазначає, що поліпіррол можна насичувати не тільки антибіотиками і такими препаратами, як дексаметазон, але і багатьма іншими биомолекулами - факторами росту, пептидами, ферментами, антитілами, білками та ін. Щоб змінити їх біологічні, фізичні, хімічні та електричні властивості і отримати контрольовану систему виділення, придатну в багатьох біомедичних додатках.
Крім того, поліпіррол можна інтегрувати в імплантуються чіпи для виведення сигналу в біологічне середовище.
«Ці попередні результати закладають фундамент розробки інтелектуальних технологій доставки препаратів для застосування в ортопедії, здатних використовувати зчитування інформації в замкнутому контурі для управління введенням препаратів на основі цієї інформації», - говорить Вебстер. «Як засновані на вуглецевих нанотрубках сенсори, так і системи контрольованої доставки ліків можуть стати відмінним засобом збільшення термінів використання ортопедичних імплантатів, що дозволяє імплантатів вбивати бактерії, проявляти меншу чутливість до тривалих запальних реакцій і, в кінцевому підсумку, посилювати процес утворення кістки».
Читати статті за темами:
Помилка в тексті?
Виділи її та натисни ctrl + enter