Ацетон знаходить широке застосування в якості розчинника, використовується як вихідна речовина для синтезу хлороформу і йодоформ. З'являється в сечі хворих на цукровий діабет. Для його виявлення використовується іодоформная проба.
Хімічний склад і будова молекули ацетону
Хімічний склад молекули ацетону можна виразити за допомогою емпіричної (C3 H6 O) і раціональної (CH3 -C (O) -CH3) формул (рис. 1).
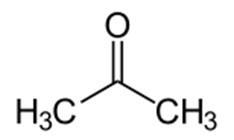
Мал. 1. Будова молекули ацетону.
Як представник класу кетонів ацетон відноситься до групи карбонільних сполук, тобто мають в своєму складі карбонільну групу (= C = O), яка з'єднана з двох сторін метильних радикалами.
Атоми вуглецю і кисню карбонільної групи знаходяться в стані sp 2-гібридизації та пов'язані σ- і π-зв'язками, складовими подвійну зв'язок. π-Зв'язок утворюється в результаті перекривання негібридних p-орбіталей обох атомів. З шести валентних атомів кисню один витрачається на освіту σ-зв'язку, другий - на освіту π-зв'язку. Дві неподіленого пари електронів розташовуються на гібридних орбіталях, які лежать в площині σ-зв'язків. Карбонільна група і безпосередньо пов'язані з нею атоми знаходяться в одній площині.
Короткий опис хімічних властивостей і щільність ацетону
Ацетон - перший представник гомологічного ряду кетонів. Для нього характерні реакції нуклеофільного приєднання-відщеплення. Наприклад, при приєднанні гидроксиламина утворюється оксим, гідразину - гідразон, а фенілгідразину - фенілгідразон:
Ацетон відновлюється воднем в присутності платини в якості каталізатора. Продуктом реакції є вторинний одноатомний спирт: