Сумарна реакція відновлення трікальцийфосфата вугле-родом виражається рівнянням 47> 48:
Са3 (Р04) 2 + 5С = Р2 + 5СО + ЗСАТ (- 418,9 ккал) 49 (-413,0 ккал) 50 (1)
Реакція починається (без флюсів) при 1100 ° і при 1400 ° завер-щує протягом 1 год (рис. 260) 51
Зі збільшенням коли-пра вуглецю ступінь відновлення Трікалі-ційфосфата зростає (рис. 261) 49, 61 При високих температурах (1500- 1550 °) вплив надлишку вуглецю менш заметно52. Велике значення має природа вуглецю. Чим дрібніше кристалики гра-фіта, тим вище його хімічна актив-
Ність 51, 52, 61, 62_ За возра-Стань відновник-ної здатності углер-дист матеріали распо-лагаются в ряд: кокс неф-тяной, графіт, антрацит, кокс металургійний, деревне вугілля.
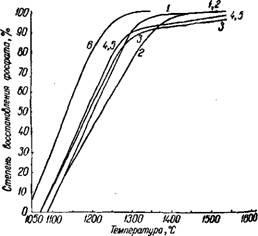
Мал. 260. Вплив температури иа ступінь відновлення фосфатів кальцію (протягом 60 хв):
/ Синтетичний Саз (Р04) 2; 2 синтетичний Ca5 (p04) 3F; 3 - апатито-нефелііовая руда; 4 - вятский фосфорит; 5 -фосфоріт Каратау; 6 - синтетичний Са4Р209.
На практиці сублімацію фосфору здійснюють з введенням В шихту кремнезему в якості флюсу. досліджувався також
застосування глинозему і алюмосілікатов60. Вплив флюсів пояс-вується тим, що вони, пов'язуючи окис кальцію, зміщують рівновагу реакції в бік утворення фосфору. Процес відновлення в цих випадках може бути представлений наступними рівняннями: Ca3 (P04) 2 + 5C + 2Si02 = P2 + 5C0 + Ca3Si207 (-368,9 ккал) 49 (-348,8 ккал) 50 (2) Са3 (Р04) 2 + 5С + ЗА1203 = Р2 + 5С0 + 3 (А1203- СаО) (-386,0 ккал) 50 (3)
У присутності кремнезему відновлення йде при більш низ-ких температурах49-61: від 1000 до 1200-1300 °. Установлено52-63 що при відновленні трікальцийфосфата утворюється переважно-ного трікальційдісі - Ликата Ca3Si207, інші ж силікати, зокрема ме- тасілікат CaSiCb, можуть утворюватися в резуль-таті вторинних реакцій.
Кремнезем, введений в шихту в кількості більшій, ніж потрібно для утворення трикальций - дісілікат і не прореагі-рова з останнім - переганяється, забруднюючи фосфор64. Ступінь вос-становлення трикальций-фосфату зростає зі збільшенням відносини Si02: Ca0 в шихті. Впливав-ня SiC> 2 стає мало помітним (особливо при температурах вище 1300 °) при кількістю-стве SiC> 2, більшому ніж в трікальційдісілікате49-61.
У присутності SiC> 2 полегшується також видалення з печі відо-сти, яка в цьому випадку випускається у вигляді легкоплавкого йшла-ка силікату кальцію. На рис. 262 видно, що температура плав-лення шлаку залежить від співвідношення в ньому Si02: СаО. Про склад шлаку судять за показником кислотності-відношенню вагового со-тримання Si02 і СаО. Наприклад, для метасилікат кальцію, пла-вящегося при 1540 ° і містить 51,7% Si02 і 48,3% СаО, поки-затель кислотності дорівнює 1,07. Шлаки з меншим показником кислотності, містять більше СаО, ніж метасиликат, називаються основними, а шлаки з великим показником кислотності кислими.
Основні і кислі шлаки, показник кислотності яких менше або більше 1,07, плавляться при температурах нижчих, ніж метасиликат кальцію.
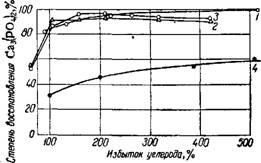
Мал. 261. Вплив надлишку вуглецю на збіль-личение ступеня відновлення трикальций-фосфату. Тривалість нагріву 60 хв: 1 - Саз (Р04) 2 + ХС, 1400 °; 2 - Са3 (Р04) 2 + ХС + 3 Si02, 1300 °; 3 - Са3 (Р04) 2 + Яс 4 2 Si02, 1300 °; 4-Са3 (Р04) 2 + + xC + 3Si02, 1200 °.
Глинозем і алюмосилікати також позитивно впливають на відновлення трікальцийфосфата, але в меншій мірі, ніж
кремнезем61> 65
67. Для відновлення має значення і природа флюсів. Аморфні двоокис кремнію або глинозем дають при про-чих рівних умовах більш високу ступінь відновлення, ніж крісталліческіе61,66-69. Лужні солі підвищують ступінь віднов-лення трікальцийфосфата вуглецем, особливо при низьких тим-пература 65,70
Наведені вище сумарні рівняння реакції восстанов-лення трікальцийфосфата вуглецем не дають уявлення про механізм процесу, погляди на кото-рий різні 74
Встановлено, що при термічному отриманні фосфору з шихти апатитів і вуглецю в присутності Si02, остання не може витісняти Р4Ою з апатитів навіть при 1400 °. При тим-пературі вище 1000 ° апатит реагує з Si02, утворюючи CaSi03 і Са3 (Р04) 2 з виділенням Н ^ О і SiF4. Потім Са3 (Р04) 2 відновлюється углер-будинок (легше, ніж апатит), а надлишок окису кальцію реагує з Si02, обра-чаплі легкоплавкий шлак.
Мал. 262. Діаграма плавкості в сістемеSi02-СаО.
Відновлення фосфатів водоростей-будинок, природного газу та інших га-зообразнимі реагентами протікає значно повільніше, ніж твердим
Вуглецем. Показано92, що в присутності ствии природного газу при температу-рах до 1250 ° (до оплавлення шихти) відновлення йде переважно вуглецем, відкладалися при піролізі метану на поверхні і в порах фосфорита; при тим-пература вище 1300 ° - воднем, що утворюється при піролізі метану. Для промислових процесів, що протікають при 1400- 1450 °, продування шихти метаном недоцільно, так як вос-становлення за рахунок водню йде повільніше, ніж металургійне-ським коксом. У той же час виділився при піролізі метану вуглець має більшу відновлювальної здатністю, ніж кокс. Взаємодія природних фосфатів з газоподібними вос-становітелямі прискорюється в присутності солей натрію і магнію, знижують температуру плавлення шіхти93. З лужних солей найбільш активно действует94 добавка Na2S'04. Максимальна впливав-ня флюсів спостерігається при температурі плавлення шихти (- 1300 °).
Відновлення фосфатів газами пов'язано з необхідністю застосування великого надлишку відновника (20-30-кратного кількості) і громіздкою аппаратури95.
Швидкість реакції відновлення трікальцийфосфата углер-будинок лімітується дифузією реагуючих компонентів 52-60'96. Досвідчені дані підтверджують, що фактори, що прискорюють Діффі-зию в твердих тілах, підвищують ступінь відновлення Трікалі-ційфосфата вуглецем. Ступінь відновлення зростає з умень-ням розміру часток шихти. Особливо показово поклади-тельное вплив брикетування шихти. Швидкість дифузії, а отже і відновлення, зростає зі збільшенням температури. Введення в шихту флюсів, що утворюють поліевтектіческіе суміші, прискорює процес. Температура перетворення кремнезему в менш щільні модифікації збігається з початковою температурою вос-становлення трікальцийфосфата в присутності кремнезему (900- 1000 °). Прискорення дифузії може бути пояснено внутрікрістал - лическими перетвореннями. Взаємодія між фосфатом і коксом у присутності кварцу, що супроводжується крісталлохімі - тичними перетвореннями з утворенням сполук проміжний-них ступенів окислення фосфору, протікає головним чином в расплаве90. Тільки до його появи йде пряме відновлення фосфату окисом вуглецю і вуглецем в результаті дифузії в твердих фазах.
У процесі сублімації протікають побічні реакції. При темпі-ратури вище 1600 ° і великому надлишку вуглецю відбувається обра-тання фосфіду і карбіду кальцію: •
Са3 (Р04) 2 + 8С = С. а3Р2 + 8СО Са3Р2 + 6С = ЗСаС2 + Р2
Інформація, що міститься в фосфатах окис заліза пов'язує частина фос-фора в Фосфіди заліза, наприклад:
Fe203 + ЗС = 2Fe + ЗСО
Вони випускаються з печі в розплавленому вигляді і застигають в чугунноподобную масу - феррофосфор.
Суттєве значення має сублімація лугів і виділення фтористих з'єднань:
2CaF2 + Si02 = 2СаО + SiF4
Четирехфторістий кремній при конденсації фосфору поглинутої-ється водою з виділенням кремнієвої кислоти, яка загряз-няет продукт. Вміщені в сировину сульфіди і сульфати обра-товують сірководень. Йде також розкладання карбонатів; виділяю-щаяся при цьому двоокис вуглецю відновлюється до окису. Наявна в шихті волога реагує з фосфором, утворюючи фосфо-Рісто водень і фосфористу кислоту, що знижує вихід фос-фора. Для зменшення втрат фосфору сировину піддається іноді попередньої прокалке.