
Головна | Про нас | Зворотній зв'язок
У процесі екстракції можна розглядати три умовних компонента: розчинник, що екстрагуються компоненти і неізвлекаемой компоненти. Для подання складів такий потрійний суміші використовують трикутну діаграму (рисунок 16.2), що представляє собою рівносторонній трикутник, кожна вершина якого відповідає умовному компоненту, а концентрації цих компонентів відкладаються на сторонах трикутника. Вершина L відповідає розчинника, A -неізвлекаемим компонентам, B -ізвлекаемим. Оскільки при екстракції тиск практично не впливає на обсяг рідкої фази, а правило адитивності обсягів добре виконується при змішуванні, потоки можуть бути виражені як масових, так і в об'ємних одиницях. Тоді концентрації компонентів відповідних компонентів дорівнюватимуть:
У рівносторонньому трикутнику сума довжин перпендикулярів, опущених з довільної точки, що лежить всередині трикутника, на його боку, дорівнює висоті трикутника. Якщо прийняти висоту трикутника за одиницю, то довжини відрізків a. b і l будуть висловлювати склад суміші в частках одиниці.
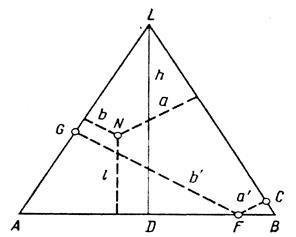
Мал. 16.2. трикутна діаграма
Будь-яка суміш трьох компонентів відповідає точці всередині трикутника (наприклад, точка N), подвійна суміш відповідає точці на сторонах трикутника. Наприклад, суміш компонентів А і В представлена точкою F на стороні АВ.
Вершини трикутника відповідають концентраціям чистих компонентів.
Крива РІВНОВАГИ ФАЗ на трикутній діаграмі
Для розрахунку процесу екстракції із застосуванням трикутної діаграми необхідно розташовувати кривої рівноваги фаз, що визначає склади фаз, що утворюються при розшаровуванні системи.
На поле трикутної діаграми відкладена бінодальная крива, що відповідає рівноважним рафінатним м екстрактивних розчинів. Пряма RS, що зв'язує точки рівноважних складів на бінодальной кривої, називається Коноді. Коноді не паралельні одна одній.
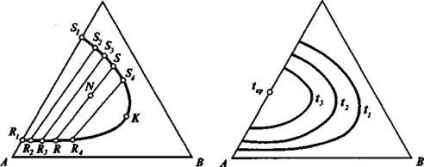
Мал. IX-9. Бінодальная (рівноважна) крива Рис. IX-10. Бінодальние криві,
І Коноді на трикутної діаграмі відповідають різним температурам на трикутної
При значному розведенні розчину компонентом В взаємна розчинність компонентів настільки зростає, що утворюється гомогенний розчин, який характеризується точкою К. Цю точку називають критичною. При подальшому збільшенні концентрації компонента В в розчині він буде залишатися гомогенним.
Будь-яка точка, наприклад N, що лежить всередині контуру, обмеженого бінодальной кривої, відповідає двофазної системі, тоді як будь-яка точка, що знаходиться поза цього контуру, характеризує однофазную систему (гомогенний рідкий розчин).
Якщо взяти суміш трьох компонентів, обумовлену крапкою N, то така система утворює два расслаивающихся розчину (дві рівноважні рідкі фази), склади яких після розшаровування характеризуються точками R і S, що знаходяться на перетині Коноді, що проходить через точку N, з нижньої і верхньої гілками бінодальной кривої.
Нижня гілка бінодальной кривої відповідає невеликим концентрацій компонента L (розчинника), що характеризує рафінатние розчини Rf. Верхня гілка бінодальной кривої відповідає високих концентрацій компонента L і характеризує екстрактивні розчини S ,.
Трикутна діаграма має такими основними властивістю, яке випливає з матеріальний балансу змішання. Якщо при змішуванні двох систем R і S виходить нова система N, то точка характеризує всі три системи, розташовується на одній прямій. При цьому точка N розташовується між точками R і S на відстанях, назад пропорцінальноих масам (обсягами) вихідних систем R і S. тобто SR відрізок пропорційний масі системи N. відрізок NR - масі системи S, а відрізок NS - масі системи S
де gR і gs - відповідно кількість рафінатного і екстрактного розчину.
Кожна бінодальная крива відповідає певній температурі і може бути побудована на підставі експериментальних даних.
При зміні розчинності зі зміною температури бінодальная крива буде змінювати своє положення. Оскільки в більшості випадків взаємна розчинність компонентів підвищується зі збільшенням температури, область існування расслаивающихся систем скорочується. При деякій температурі Ткр. званої критичної, компоненти, що входять до складу трифазної системи, будуть повністю розчинятися один в одному, утворюючи гомогенний рідкий розчин.
На рис. IX-10 наведені бінодальние криві для декількох температур за умови tx Схожі статті