Використання віртуальної лабораторії на уроці хімії дозволить вчителю познайомити учнів з об'ємним будовою неорганічних кислот, наочно провести хімічний експеримент зі зміни забарвлення індикаторів в кислотах, що дозволяє в умовах даного уроку істотно заощадити час при вивченні нового матеріалу.
Тип уроку: Урок вивчення нового матеріалу і первинного закріплення знань
Особистісні. Розвиток пізнавальних інтересів, інтелектуальних і творчих здібностей
пізнавальні:- Знаходити схожість і відмінність між об'єктами, узагальнювати отриману інформацію, вести спостереження, класифікація об'єктів за запропонованими критеріями
- Уміння формулювати визначення, підбирати аргументи.
- Застосовувати ІКТ, в процесі навчання хімії.
- Виконувати навчальне завдання відповідно до мети.
- Співвідносити навчальні дії з відомими правилами.
- Виконувати навчальний дію відповідно до плану.
- Оцінка своїх навчальних досягнень.
Давати визначення "кислоти", розпізнавати оксиди, підстави і кислоти серед інших речовин, складати формули оксидів неметалів і називати їм відповідні кислоти, розуміти значення кислот в житті людини, розпізнавати кислоти за допомогою індикаторів, "Віртуальної хімічної лабораторії".
Методи навчання: словесні (розповідь, пояснення, бесіда);- ілюстративні;
- демонстраційні;
- Частково-пошуковий, проблемний, ІКТ.
Устаткування і реактиви: комп'ютер, проектор, демонстраційний екран, ЕП "Віртуальна хімічна лабораторія 8-11 клас", зразки кислот: соляна, сірчана, оцтова, пробірки, зошити, робочі листи, плакати, таблиці з формулами кислот.
Девіз уроку: "День прожитий не дарма, якщо ти дізнався щось нове".
1. Організаційний момент.
Привіт, дорогі хлопці. Сьогодні ми з вами працюємо за допомогою таких засобів: підручник, ваша робочий зошит, командна карта уроку і довідковий матеріал кожного учня. Підпишемо інструктивну карту уроку.
2. Актуалізація знань.
Хлопці, ми з вами розпочали вивчення класів неорганічних сполук. З якими класами речовин ми вже встигли познайомитися? (Оксиди, гідриди і летючі водневі сполуки, підстави). Давайте попрацюємо з формулами. Серед запропонованих формул вкажіть оксиди і підстави. А невідомі вам речовини підкресліть.
Дан ряд речовин: СО2. НNО3. Н2 SО4. Са (ОН) 2. Nа2 СО3. Н3 РО4. КОН, НСI, СаО, SО2. Fе2 О3. Nа2 О, Сl2 О7. Н2 СО3. КОН, Ва (ОН) 2. Сu (ОН) 2.- 1 питання. Які речовини вам знайомі з цього переліку? Дайте визначення оксидів і підстав?
- 2 питання. Які речовини з даного списку - оксиди? У командному мапі запишіть формули оксидів в 1 стовпчик.
- 3 питання. Які речовини з даного переліку підстави? У командному мапі запишіть формули підстав у 2 стовпчик.
Учні роблять записи в зошит. Третя група учням не знайома.
Учитель: Зверніть увагу на формули хімічних сполук, які ми не вибрали. У даному переліку речовин залишилися формули, у яких на першому місці стоїть водень. (Работаучащіхсяс інструктивно картою, завдання 1.)
Перед вами стоїть проблема: що це за з'єднання? Давайте спробуємо відповісти на це питання.
Учні дають відповіді.
3. Вивчення нового матеріалу
У третю групу ви помістили поки що незнайомі вам речовини, які відносяться до класу кислот. Саме з речовинами цього класу ми і будемо знайомитися сьогодні. Отже, тема нашого уроку "Кислоти: склад, класифікація і значення". Запишіть тему уроку в робочий зошит.
Питання учням: Що ж нам необхідно знати про кислотах? (Склад, формули, назви, класифікації, значення, правила техніки безпеки).
Таким чином, ми разом сформулювали мету нашого уроку - вивчити склад, формули, назви, класифікації, значення, правила техніки безпеки.
1. Записуємо визначення кислот.
Ви бачите на плакаті формули трьох кислот: соляної або соляної НСl. сірчаної Н2 SО4 і фосфорної кислот Н3 РО4. Що спільного в їх складі?
Учні дають свої відповіді.
Так, це присутність в їх складі атомів водню, з якого починаються всі три формули. Інша частина називається кислотним залишком.
Кислоти - складні речовини, молекули яких складаються з атомів водню і кислотного залишку.
Записуємо визначення кислот в зошит.
2. Розглядаємо класифікацію кислот.
У довідковому матеріалі перед вами схема "Класифікації кислот". Кислоти класифікують за кількістю атомів водню, за наявністю кисню, ознакою розчинності.
а) за кількістю атомів водню (основності):
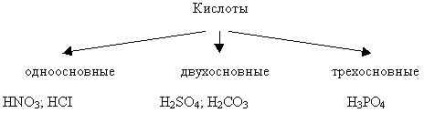
б) за наявністю атомів кисню:
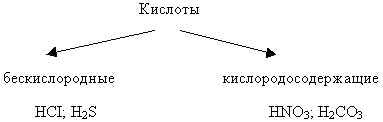
Подивіться на формули кислот. Вони розподілені на три групи за певною ознакою. Як ви думаєте, що це за ознака?
Основность - число атомів водню в кислоті.
А який ще може бути ознака класифікації? Давайте попрацюємо з таблицею розчинності з підручника, де ми розглядали властивості підстав. Це ознака розчинні. Знайдемо нерастворимую кислоту. Це кремнієва кислота.
Учитель наводить зразок класифікації на прикладі вугільної кислоти Н2 СО3.
3. Дати характеристику Н3 РО4 за класифікацією (учні виконують завдання 2 по інструктивно карті). Виконуємо перевірку.
4. Перед нами проблема: як назвати кислоти? Знайдіть в довідковому матеріалі запис з формулами і назвами кислот. Читаємо формули кислот разом з учнями.- НСI - соляна кислота
- НNО3 - азотна кислота
- HBr - бромистий кислота
- Н2 SО4 - сірчана кислота
- Н2 СО3 - вугільна кислота
- Н3 РО4 - фосфорна кислота
5. Робота в ВІРТУАЛЬНОЇ ЛАБОРАТОРІЇ.
Хлопці, а які молекули даних кислот в просторі? Може вони плоскі? Або об'ємні? Ми можемо побачити будову молекул в просторі за допомогою віртуальної хімічної лабораторії, в якій є Конструктор молекул.
Працюємо в віртуальної лабораторії, будуємо молекули соляної і сірчаної кислот.
6. Учитель. Давайте перевіримо, що ви встигли запам'ятати з формул кислот. Я назву і покажу формули деяких кислот (показ карток з формулами). Попрошу відтворити по пам'яті формули кислот і їх назва. (Учні без карток по пам'яті називають формули і назви кислот.)
Гімнастика для очей
Сіли спокійно. Виконуємо вправи.
Ми зараз очі замружимо - Раз, два, три, чотири, п'ять!
На таблицю вгору подивимося,
А тепер у свій зошит,
Вліво, вправо, поморгай,
І по колу пробігли.
Ми очі замружимо знову.
Продовжувати урок готові?
Відкриваємо очі знову!
7. Визначення ступенів окислення.
Так само ми повинні працювати з формулами кислот, визначаючи в них ступеня окислення. Хлопці, давайте з вами, визначимо ступеня окислення елементів в кислотах і відповідні кислотам оксиди.
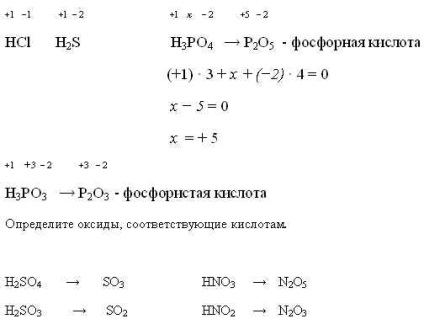
- одна помилка або без помилок- "5"
- дві помилки - "4"
- три помилки-"3".
8. Хлопці, а чи можна провести хімічний експеримент без пробірок і реактивів? Виявляється можна. Для цього ми звернемося до ВІРТУАЛЬНОЇ ЛАБОРАТОРІЇ з хімії. Виконуємо віртуальний експеримент.
Простежимо зміна забарвлення індикаторів в розчинах кислот лугів.
У командному карті учні фіксують висновки: як змінюється колір індикатора в кислотах (завдання № 4):
1) метиловий оранжевий - стає червоно-рожевим;
2) фіолетовий лакмус - червоним;
3) безбарвний фенолфталеин - залишається безбарвним.
Асоціація - КИСЛИЙ - ЧЕРВОНИЙ
9 Значення кислот в природі та житті людини. (Повідомлення учнів).
10. Демонстрація кислот. Техніка безпеки при роботі з кислотами. (Плакат)
5. Етап рефлексії
Мета: ініціювати рефлексію учнів з приводу свого психо-емоційного стану, мотивації своєї діяльності і взаємодії з учителем і однокласниками.
Учитель. Я задоволена вами, ви порадували мене своїми відповідями, бажанням багато чого довідатися, вашим інтересом до хімії. Наша дошка як книга. Ми відкрили сторінку, вивчили тему і закрили сторінку. До якого ж висновку ми прийшли?
Учні роблять висновки про урок.
Завершіть речення:- Тепер я знаю, що ......
- Я зрозумів, що……
- Я буду……
6. Домашнє завдання. Параграф 21, с. 119-124, вивчити формули кислот - "4".
2. Завдання 4 с.126 (підручник). - "5".