3. Молекула води
У житті людини, як і в житті будь-якого іншого істоти, вода відіграє величезну роль. Вода потрібна для пиття і для приготування їжі, вода потрібна для миття. Давно людина зрозуміла і те, що вода необхідна для його полів. Тому немає нічого дивного, що ще стародавні народи, що жили тисячоліття до нас, дивилися на воду як на особливу речовину, першооснову всього існуючого.
«Вода як рідке, рухливе, всеохоплююче, стала початком всього» - вчив близько двох з половиною тисяч років тому «грецький мудрець Фалес. Років двісті тому найбільший філософ стародавнього світу Аристотель налічував вже кілька таких першооснов, "основних елементів" світу, але серед них була і вода.
У висловлюваннях стародавніх греків, якими б ці висловлювання не здавалися нам зараз по-дитячому наївними, вже відбивалося глибоке розуміння значення води у всіх явищах природи і в житті людини.
Минуло близько 20 століть. Саме поняття "елемент" істотно змінилося. Хімічним елементом стали вважати проста речовина, яке вже не може бути розкладено далі на більш прості речовини. Число елементів все збільшувалася і збільшувалася. У списку цих елементів знову значилася вода.
І цьому були причини. Адже вчені того часу, спостерігаючи різні явища, в яких бере участь вода, ніколи не помічали, щоб вона змінювалася хімічно. На очах їх вона твердне в лід, але лід при таненні давав ту ж воду. Вода нагрівалася до кипіння і випаровувалася, але, охолоджуючись, пари знову збиралися в краплі води. Вода як речовина залишалася у всіх процесах "самою собою" і її вважали нерозкладним, простим речовиною.
Тільки в кінці вісімнадцятого століття було зроблено важливе відкриття, що вода є складна речовина: вода була отримана штучним шляхом, при спалюванні газу водню в кисні. Цим було доведено, що вода складається з водню і кисню.
Приблизно в цей же час складний склад води вдалося довести і зворотним шляхом - розкладанням води на складові частини. Це зробив французький учений Лавуазьє. Через розпечений рушничний стовбур він пропускав пари води. Від дії високої температури вода розкладалася. Кисень з'єднувався з залізом, і на внутрішній поверхні ствола з'являлася окалина (з'єднання заліза з киснем), а зі стовбура виходив газ водень.
А кількома роками пізніше вода вперше була розкладена на її складові частини електричним струмом. Цим шляхом було точно встановлено, що в воді по вазі знаходиться 11,11 відсотка водню і 88,89 відсотка кисню, причому водню виділяється з води за обсягом в два рази більше, ніж кисню.
Якщо обидва ці виділилися газу змішати, то при кімнатній температурі ця суміш може залишатися без зміни дуже довго. Щоб тільки одна шоста частина цієї суміші перетворилася в воду, нам довелося б чекати 54 мільярди років. Але варто тільки піднести до цієї суміші запалений сірник або пропустити через неї електричну іскру, як між киснем і воднем моментально відбудеться хімічна реакція: водень згорить в кисні, і в результаті вийде вода. Такий досвід треба проводити з великою обережністю, так як горіння завжди супроводжується вибухом великої сили. Тому суміш з двох об'ємів водню і одного об'єму кисню і названа гримучою сумішшю.
Щоб викликати реакцію між киснем і воднем, зовсім не обов'язково нагрівати всю суміш. Достатньо нагріти самий незначний її обсяг. У цьому обсязі почнеться процес горіння водню - з'єднання його з киснем. При цьому виділяється дуже багато тепла (десять грамів гримучої суміші при горінні дають таку кількість тепла, якого достатньо, щоб закип'ятити майже півлітра води). Вирізняється тепло передається сусіднім ділянкам суміші, і процес горіння з надзвичайною швидкістю поширюється по всьому об'єму.
Температура в полум'я гримучого газу перевищує 3000 градусів. Тому гримучий газ і застосовують для автогенного зварювання.
Отже, вода - це складна речовина, що складається з кисню і водню. Як же побудована молекула води? Як розташовуються в ній атоми кисню і водню?
Сучасна наука має в своєму розпорядженні дуже точними методами дослідження, які дозволяють проникнути в будівлю речовини так глибоко, що вже тепер з повною впевненістю можна говорити не тільки про те, з яких атомів складені молекули того чи іншого речовини, а й про те, як розташовуються атоми в молекулах . Кожна молекула води складається з трьох атомів: одного атома кисню і двох атомів водню. Всі три атома розташовані в молекулі таким чином, що якщо подумки з'єднати їх лініями, то утворюється трикутник, тобто трикутник, у якого дві сторони рівні (рис. 3). У вершині знаходиться атом кисню, а в двох кутах при основі - по атому водню. Відстані між атомом кисню і водневими атомами однакові і рівні 97 десятимільярдним часток сантиметра. Відстань між атомами водню одно 154 десятимільярдним часток сантиметра, а кут при вершині, в якій знаходиться атом кисню, становить близько 105 градусів. Якщо розмір молекули збільшити в десять мільярдів разів, цей трикутник помістився б на столі середнього розміру.
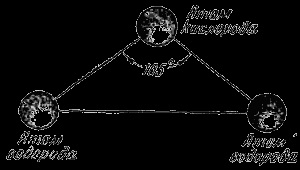
Мал. 3. Розташування атомів в молекулі води.
Читач може запитати: чому атоми в молекулі води розташовані у вигляді трикутника, а не по прямій лінії - в середині атом кисню, а по краях атоми водню?
Пояснити це можна так. Будь-яке тіло в природі прагне зайняти найбільш стійке положення. М'яч, кинутий на гладку дах, не залишиться лежати на її похилим поверхні і під дією сили тяжіння обов'язково скотиться вниз. Якщо ми прив'яжемо до нитки який-небудь грузик і будемо тримати нитку за вільний кінець, грузик натягне нитку і розташується точно по прямовисній лінії. Відведемо грузик трохи в сторону і відпустимо, - грузик не залишиться в новому нестійкому стані і під дією сили тяжіння швидко повернеться до свого початкового стану. Так і в молекулі води. Атоми з'єднані в ній один з одним силами, які називають силами хімічної спорідненості. Величина і напрям дії цих сил є такими, що молекула води є стійкою саме тоді, коли атоми утворюють трикутник. Будь-яка інша "споруда" з атомів виявляється менш стійкою. І якщо з яких-небудь причин розташування "атомів" зміниться, то по усуненні цієї причини атоми знову утворюють такий самий трикутник.
Потрібно сказати, що сили, які утримують атоми водню і кисню в молекулі води, досить великі. Необхідна дуже велика енергія, щоб зв'язок між атомами "розірвалася". Ми можемо нагріти воду до 1400 градусів, і з мільйона молекул води при цій температурі тільки близько ста молекул виявляться розкладеними на водень і кисень. Навіть при 3092 градусах руйнується тільки 13 відсотків всіх молекул води.
Будь-яка вода, звідки б вона не була взята, - з Північного Льодовитого океану, з глибокої шахти Донбасу, була укладена в снежинке або виблискувала рано вранці в крапельці роси на квітці, - будь-яка вода складаються з однаково побудованих молекул. Однак взаємне розташування окремих молекул один щодо одного в рідкій воді, снежинке або в парі з парового котла виявляється неоднаковим.
Пари води, нагріті градусів до трьохсот, при атмосферному тиску подібні звичайним газам: в них відстані між молекулами досить великі, так що кожна окрема молекула може існувати більш-менш самостійно, не відчуваючи суттєвої взаємодії з боку своїх сусідів, за винятком, звичайно, тих випадків, коли молекули в результаті безладного теплового руху стикаються один з одним.
У снежинке або шматочку льоду молекули зближені і закріплені в певних місцях кристалічної решітки; руху молекул в більшості своїй обмежуються коливанням близько деяких середніх положень.
А як розташовуються молекули в рідкій воді?
У науці досі ще немає суворої, твердо встановленої теорії, що стосується будови рідин, зокрема води. Передбачається, що рідка вода за своєю будовою представляє щось середнє між кристалами льоду і парою. Вивчення будови води за допомогою інфрачервоних і рентгенівського проміння дало можливість вважати, що при температурах, близьких до точки замерзання, молекули рідкої води збираються в невеликі групи і "упаковуються" в простір приблизно так, як в кристалах, а при температурах, близьких до точки кипіння води, при нормальному тиску, вони розташовуються більш вільно, безладно. Однак "каркас", складений в рідкій воді з окремих молекул, повинен бути дуже гнучким. Інакше важко було б пояснити рухливість води, здатність її бути "робочим тілом", що приводить в рух важке колесо турбіни, і переносником різних поживних речовин по найтонших судинах живих організмів.
Мабуть, і в водяній парі при невисоких температурах частина молекул води об'єднана або, як кажуть, асоційована.
Вода - найпоширеніша в природі рідина. Ми так звикли до води, до її різноманітних проявів, що вона нам здається звичайнісінької рідиною. Багато властивостей води покладені в основу нашої вимірювальної системи. Температуру танення льоду ми вважаємо за нуль градусів, а температуру кипіння за сто градусів (за прийнятою тепер майже всюди шкалою Цельсія). Масу води в обсязі одного кубічного сантиметра ми приймаємо за міру маси - один грам. Кількість тепла, яке поглинає один грам води при нагріванні на один градус, ми називаємо одиницею теплоти - калорій. Багато вимірювальні прилади фізиків і хіміків градуюються по воді, і величини, виміряні для інших речовин, зазвичай порівнюються з числами, отриманими для води. Але якщо ми уважно придивимося до поведінки води в різних умовах і порівняємо його з поведінкою більшості інших рідин, то виявимо, що наша "звичайна" рідина поводиться дуже дивно, якщо цими словами можна виразити своєрідний характер води, різко відрізняє її від всіх інших рідин .
Тепер ми і розповімо про деякі найбільш важливих і цікавих властивості води і її відступах від загальних "правил" поведінки рідин.