Фізична сутність і механізм процесу кристалізації
Кристалізація - це процес утворення ділянок кристалічної решітки в рідкій фазі і зростання кристалів з утворених центрів.
Кристалізація протікає в умовах, коли система переходить до термодинамічно більш стійкого стану з мінімумом вільної енергії.
Процес переходу металу з рідкого стану в кристалічний можна зобразити кривими в координатах час - температура. Крива охолодження чистого металу представлена на рис. 1.

Рис.1. Крива охолодження чистого металу
- теоретична температура кристалізації;
. - фактична температура кристалізації.
Процес кристалізації чистого металу:
До точки 1 прохолоджується метал у рідкому стані, процес супроводжується плавним зниженням температури. На ділянці 1 - 2 йде процес кристалізації, що супроводжується виділенням тепла, яке називається прихованою теплотою кристалізації. Воно компенсує розсіювання теплоти в простір, і тому температура залишається постійною. Після закінчення кристалізації в точці 2 температура знову починає знижуватися, метал охолоджується в твердому стані.
Механізм кристалізації металів.
При відповідному зниженні температури в рідкому металі починають утворюватися кристалики - центри кристалізації або зародки. Для початку їх росту необхідне зменшення вільної енергії металу, в іншому випадку зародок розчиняється.
Мінімальний розмір здатного до зростання зародка називається критичним розміром. а зародок - стійким.
Перехід з рідкого стану в кристалічний вимагає витрати енергії на утворення поверхні розділу рідина - кристал. Процес кристалізації буде здійснюватися, коли виграш від переходу в твердий стан більше втрати енергії на освіту поверхні розділу. Залежність енергії системи від розміру зародка твердої фази представлена на рис. 2.
Зародки з розмірами рівними і великими критичного ростуть зі зменшенням енергії і тому здатні до існування.
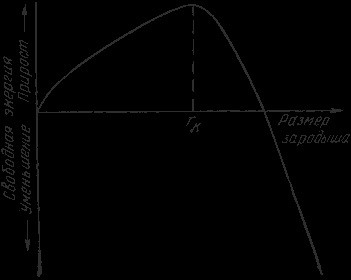
Рис.2. Залежність енергії системи від розміру зародка твердої фази
Механізм кристалізації представлений на рис.3.

Рис.3. Модель процесу кристалізації
Центри кристалізації утворюються в початковій фазі незалежно один від одного в випадкових місцях. Спочатку кристали мають правильну форму, але в міру зіткнення і зрощення з іншими кристалами форма порушується. Зростання триває в напрямках, де є вільний доступ живильної середовища. Після закінчення кристалізації маємо полікристалічне тіло.
Якісна схема процесу кристалізації може бути представлена кількісно кінетичної кривої (рис. 4).
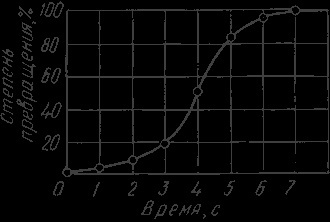
Мал. 4. Кінетична крива процесу кристалізації
Процес спочатку прискорюється, поки зіткнення кристалів це не починає перешкоджати їх росту. Обсяг рідкої фази, в якій утворюються кристали зменшується. Після кристалізації 50% обсягу металу, швидкість кристалізації буде сповільнюватися.
Таким чином, процес кристалізації складається з утворення центрів кристалізації і росту кристалів з цих центрів.
У свою чергу, число центрів кристалізації (ч.ц.) і швидкість росту кристалів (с.р.) залежать від ступеня переохолодження (рис. 5).
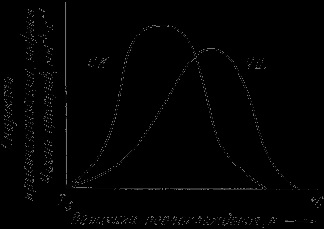
Мал. 5. Залежність числа центрів кристалізації (а) і швидкості росту кристалів (б) від ступеня переохолодження
Розміри утворилися кристалів залежать від співвідношення числа утворилися центрів кристалізації і швидкості росту кристалів при температурі кристалізації.
При рівноважної температурі кристалізації ТS число утворилися центрів кристалізації і швидкість їхнього зростання дорівнюють нулю, тому процесу кристалізації не відбувається.
Якщо рідина переохолодити до температури, відповідної т.а, то утворюються великі зерна (число центрів, що утворилися невелике, а швидкість росту - велика).
При переохолодженні до температури відповідної Т.В - дрібне зерно (утворюється велика кількість центрів кристалізації, а швидкість їх росту невелика).
Якщо метал дуже сильно переохолодити, то число центрів і швидкість росту кристалів дорівнюють нулю, рідина не кристалізується, утворюється аморфне тіло. Для металів, що володіють малою схильністю до переохолодження, експериментально виявляються тільки висхідні гілки кривих.
Рекристалізаційного отжиг (Рекристалізація) - отжиг I-го роду, процес зародження і зростання нових недеформірованних зерен при нагріванні наклепаного металу до певної температури.
Нагрівання металу до температур рекристалізації супроводжується різкою зміною мікроструктури і властивостей. Нагрівання призводить до різкого зниження міцності при одночасному зростанні пластичності. Також знижується електроопір і підвищується теплопровідність.
1 стадія - первинна рекристалізація (обробки) полягає в утворенні центрів кристалізації і зростання нових рівноважних зерен з неспотвореної кристалічною решіткою. Нові зерна виникають біля кордонів старих зерен і блоків, де решітка була найбільш спотворена. Кількість нових зерен поступово збільшується і в структурі не залишається старих деформованих зерен.
Рушійною силою первинної рекристалізації є енергія, акумульована в наклепаного металі. Система прагне перейти в стійкий стан з неспотвореної кристалічною решіткою.
2 стадія - збірна рекристалізація полягає в зростанні утворилися нових зерен.
Рушійною силою є поверхнева енергія зерен. При дрібних зернах поверхню розділу велика, тому є великий запас поверхневої енергії. При укрупненні зерен загальна протяжність кордонів зменшується, і система переходить в більш рівноважний стан.
Температура початку рекристалізації пов'язана з температурою плавлення
,
для твердих розчинів
для металів високої чистоти
На властивості металу великий вплив робить розмір зерен, одержані при рекристалізації. В результаті утворення великих зерен при нагріванні до температури t1 починає знижуватися міцність і, особливо значно, пластичність металу.
Основними факторами, що визначають величину зерен металу при рекристалізації, є температура, тривалість витримки при нагріванні і ступінь попередньої деформації (рис. 6).

Мал. 6. Вплив попередньої ступеня деформації металу на величину зерна після рекристалізації
З підвищенням температури відбувається укрупнення зерен, зі збільшенням часу витримки зерна також укрупнюються. Найбільші зерна утворюються після незначної попередньої деформації 3 ... 10%. Таку деформацію називають критичною. І така деформація небажана перед проведенням рекристаллизационного відпалу.
Практично відпал рекристалізації проводять для маловуглецевих сталей при температурі 600 ... 700 o С, для латунь і бронза - 560 ... 700 o С, для алюмінієвих сплавів - 350 ... 450 o С, для титанових сплавів - 550 ... 750 o С.
Перетворення в залізовуглецевих сплавах
Діаграма стану Fe-Fe3 C (рис. 7) показує фазовий склад і перетворення в сплавах з концентрацією від чистого заліза до цементиту.
Перетворення в залізовуглецевих сплавах відбувається як при кристалізації (затвердевании) рідкої фази (Ж), так і в твердому стані.
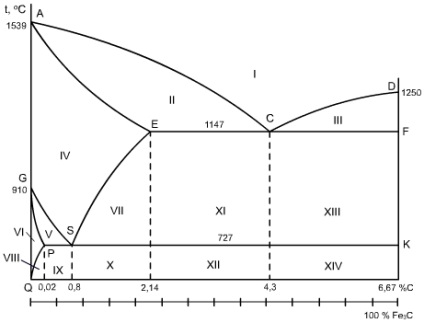
Мал. 7. Діаграма стану Fe - Fe3 C (в спрощеному і повному вигляді).
Первинна кристалізація йде в інтервалі температур, ограни-чинних лініями ликвидус (ACD) і солидус (AECF).
Вторинна кристалізація відбувається за рахунок перетворення заліза однієї аллотропическими модифікації в іншу і за рахунок зміни розчинності вуглецю в аустеніт і ферит, яка зменшується з пониженням температури. Надлишок вуглецю виділяється з твердих розчинів у вигляді цементиту. У сплавах системи Fe-Fe3 C відбуваються такі ізотермічні перетворення:
Евтектичну перетворення на лінії ECF (тисяча сто сорок сім ° C)
Евтектоїдних перетворення на лінії PSK (727 ° C)
Евтектична суміш аустеніту і цементиту називається ледебуріта (Л), а евтектоїдна суміш фериту і цементиту - перлитом (П). Ледебурит містить 4,3% вуглецю. При охолодженні ледебуріта нижче ліній PSK входить в нього аустенит перетворюється в перліт і при нормальній температурі ледебурит являє собою суміш перліту і цементиту і називається ледебуріта перетвореним (Л пр). Цементит в цій структурної складової утворює суцільну матрицю, в якій розміщені колонії перліту. Така будова ледебуріта пояснює його велику твердість (HB 700) і крихкість.
Перліт містить 0,8% вуглецю. Залежно від форми частинок цементит буває пластинчастий і зернистий. Є міцною структурної складової з твердістю (HB210).
Лінії діаграми стану Fе - Fе3 C
Лінії діаграми являють собою сукупність критичних точок сплавів з різним складом, що характеризують перетворення в цих сплавах при відповідних температурах.
Розглянемо значення ліній діаграми при повільному охолодженні.
ACD - лінія ликвидус. Вище цієї лінії все сплави знаходяться в рідкому стані.
AECF - лінія солидус. Нижче цієї лінії все сплави знаходяться в твердому стані.
АС - з рідкого розчину випадають кристали аустеніту.
CD - лінія виділення первинного цементиту.
AE - закінчується кристалізація аустеніту.
ECF - лінія евтектичного перетворення.
GS - визначає температуру початку виділення фериту з аустеніту (910-727 ° C).
GP - визначає температуру закінчення виділення фериту з аустеніту.
PSK - лінія евтектоїдних перетворення.
ES - лінія виділення вторинного цементиту.
PQ - лінія виділення третинного цементиту.
Області діаграми стану Fe - Fe3 C
Лінії діаграми: ділять все поле діаграми на області рівноважного існування фаз. Кожній області діаграми відповідає певний структурний стан, сформований в результаті відбуваються в сплавах перетворень.
I - Рідкий розчин (Ж).
II -рідку розчин (Ж) і кристали аустеніту (А).
III - Рідкий розчин (Ж) і кристали цементиту первинного (Цi).
IV - Кристали аустеніту (А).
V - Кристали аустеніту (А) і фериту (Ф).
VI - Кристали фериту (Ф).
VII - Кристали аустеніту (А) і цементиту вторинного (ЦII).
VIII - Кристали фериту (Ф) і цементиту третинного (ЦIII).
IX - Кристали фериту (Ф) і перліту (П).
X - Кристали перліту (П) і цементиту вторинного (ЦII).
XI - Кристали аустеніту (А), ледебуріта (Л) і цементиту вторинного (ЦII).
XII - Кристали перліту (П), цементиту вторинного (ЦII) і ледебуріта перетвореного (Л пр).
XIII -Крісталли ледебуріта і цементиту первинного (Цi).
XIV - Кристали цементиту первинного (Цi) перліту (П) і ледебуріта перетвореного (Л пр).
В цьому випадку при охолодженні аустеніту є тільки одна критична точка Аs. що відповідає температурі 727 ° С. При цій температурі аустеніт знаходиться в рівновазі з ферритом і цементитом:
Евтектоїдний розпад аустеніту складу точки S (0,8% С) на ферит складу точки Р (0,025% С) і цементит відбувається при деякому переохолодженні, тобто нижче 727 ° С. Евтектоїдних суміш фериту з цементитом називається перлітом. Співвідношення фериту і цементиту в перліті становить приблизно 7,3. 1.
Підрахунок ведеться за правилом важеля, трохи нижче евтектоїдной лінії:
При кімнатній температурі - склад феррит і перліт
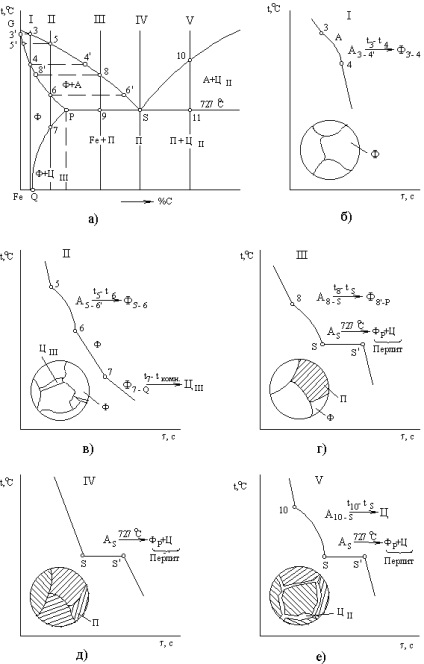
Мал. 8. Лівий нижній ділянку діаграми стану залізо-цементит. Вторинна кристалізація сплавів:
а) діаграма, б), в), г), д), е) криві охолодження сплавів
Схожі документи:
при нагріванні і охолодженні. Варіант 4 1.Опишите фізіческуюсущность і механізмпроцесса кристалів-зації. 2. Для чого проводиться. впливають модифікатори на процесскрісталлізаціі. Наведіть приклади практичного використання процесу модифікування. 2. Як.
Дисципліна «Фізичне матеріалознавство. Кристалізація Енергетичні умови процессакрісталлізаціі. Механізмпроцессакрісталлізаціі. Мимовільна і несамопроізвлольная кристалізація. механізму і механізму освіти і зростання зародків. Сутність.
і фільтрація, конденсація, кристалізація і взагалі процес утворення нових фаз -. що обмежує цю поверхню. Фізіческаясущность поверхневого натягу в цьому. необхідне використання уявлень про механізм адсорбції і конкретних моделей.
речовин немає горизонтальної ділянки? Який механізмпроцессакрісталлізаціі. При якому будову металів. 14. У чому полягає фізіческаясущностьпроцессов плавлення і кристалізації. 15. Поясніть сутність та цілі модифікування. 16.
розряд. Сущностьпроцесса - При зварюванні. стадія процессакрісталлізаціі. утворення центрів кристалізації. Специфічними особливостями фізичних властивостей. 3-касета; 4-механізм подачі дроту; 5-6-механізми вертикального і поперечного.