Більшість білків гідрофільних. Однак білкові молекули мають дуже великі розміри, тому білки не можуть утворювати істинних розчинів, а тільки колоїдні. Зовнішній прояв цього - це ефект Тиндаля (або конус Тиндаля). Ефект Тиндаля викликається розсіюванням тонкого пучка світла при проходженні через білковий розчин. Незважаючи на велику величину, багато білкові молекули не осідають у водних розчинах. Осадженню білкових молекул перешкоджають чинники стабілізації білкового розчину.
Фактори стабілізації білка в розчині.
Гідратної оболонки - це шар молекул води, певним чином орієнтованих на поверхні білкової молекули. Поверхня більшості білкових молекул заряджена негативно, і диполі молекул води притягуються до неї своїми позитивно зарядженими полюсами (дивіться малюнок).
Ч
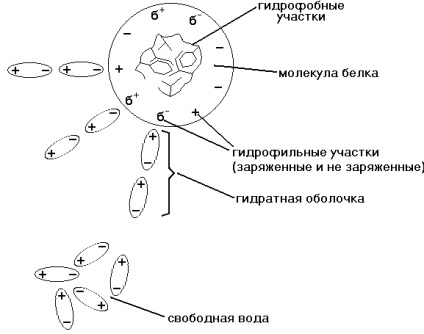
Властивості води гідратної оболонки
а) Температура кипіння вище 100 0 С.
б) Температура замерзання нижче 0 Про С.
в) У воді гідратної оболонки не розчиняються різні солі та інші гідрофільні речовини.
г) Оточуючи кожну молекулу білка, гидратная оболонка не дає цим білковим молекулам зблизитися, з'єднатися і випасти в осад.
2) ЗАРЯД БІЛКОВОЇ МОЛЕКУЛИ. Поверхня більшості білкових молекул заряджена тому, що в кожній молекулі білка є вільні заряджені СОО - і NH3 + групи. Ізоелектрична точка (ВЕТ) більшості білків організму знаходиться в слабокислою середовищі. Це означає, що у таких білків кількість кислотних (СООН) груп більше кількості основних груп (NH3). рН плазми крові близько 7,36 - це вище ВЕТ більшості білків, тому в плазмі крові білки мають негативний заряд.
Способи осадження білків
Діляться на дві групи:
1) Способи осадження нативного білка
2) Способи осадження денатурованого білка
Щоб осадити білок з розчину, треба позбавити його обох факторів стабілізації: і заряду, і гідратної оболонки.
Осадження нативних білків
Щоб зберегти нативну білкової молекули, її заряд можна усунути тільки одним способом: наблизити рН середовища до ізоелектричної точці білка (ВЕТ), а для більшості білків нашого організму ВЕТ знаходиться в слабокислою середовищі. Інший фактор стабілізації - гідрадну оболонку можна усунути різними способами.
Найбільш типовим прикладом осадження нативного білка є висолювання.
а) Висолювання - це осадження білків високими концентраціями нейтральних солей лужних і лужноземельних металів, оскільки такі солі дуже гідрофільних і мають у високих концентраціях водовіднімаючих властивостями. Найчастіше це NaCl, Na2 SO4. (NH4) 2 SO4. CaCl2. У міру додавання таких солей до розчину білка вони спочатку розчиняють у вільній воді, а потім, при подальшому підвищенні концентрації солі, конкурують з білком за володіння водою, яка входить до складу гідратних оболонок. Білки менш гідрофільні, які погано утримують воду гідратної оболонки, втрачають її раніше. Більш гідрофільні білки вимагають більшої концентрації солі для висолювання. Тому за допомогою висолювання можна розділити білки з різним ступенем гідрофільності. Таким способом, наприклад, можна розділити альбуміни і глобуліни плазми крові.
При Висолювання зберігається нативних білкових молекул. Якщо осадити білки за допомогою висолювання, а потім зменшити концентрацію солей, наприклад, методом діалізу, то білок знову розчиниться.
Осадження білків без втрати ними нативної можна досягти також за допомогою водоотнимающих засобів.
б) застосування водовіднімаючих ЗАСОБІВ. Такими засобами є розчинники, які змішуються з водою в будь-яких співвідношеннях. Найчастіше це ацетон, етиловий спирт. Ці речовини забирають гідратів оболонки білків, і білки випадають в осад, якщо вони позбавлені заряду. Але, на відміну від висолювання, осад відразу (негайно!) Повинен бути відділений від розчинника. Якщо розчинник і білок будуть тривалий час перебувати в контакті, то можуть статися безповоротні зміни структури білкової молекули (денатурація).