Органічні речовини займають важливе місце в нашому житті. Вони є основною складовою полімерів, які оточують нас всюди: це і поліетиленові пакети, і гума, а також безліч інших матеріалів. Поліпропілен займає в цьому ряду не останню сходинку. Він також входить до складу різних матеріалів і застосовується в ряді галузей, таких як будівництво, має побутове застосування в якості матеріалу для пластикових стаканчиків і інших дрібних (але не за масштабами виробництва) потреб. Перш ніж поговорити про такий процес, як гідратація пропілену (завдяки якому, до речі, ми можемо отримати ізопропіловий спирт), звернемося до історії відкриття цього необхідного для промисловості речовини.
Як такої дати відкриття пропілен не має. Однак його полімер - поліпропілен -був фактично відкритий в 1936 році відомим німецьким хіміком Отто Байєром. Звичайно, теоретично було відомо, як можна отримати такий важливий матеріал, але практично зробити це не вдавалося. Вдалося це тільки в середині двадцятого століття, коли німецький і італійський хіміки Циглер і Натт відкрили каталізатор полімеризації ненасичених вуглеводнів (мають одну і більше кратних зв'язків), який згодом так і назвали: каталізатор Циглера-Натта. До цього моменту рішуче неможливо було зробити так, щоб реакція полімеризації таких речовин пішла. Були відомі реакції поліконденсації, коли без впливу каталізатора речовини з'єднувалися в полімерну ланцюг, утворюючи при цьому побічні речовини. Але з ненасиченими вуглеводнями це зробити не вдавалося.
Ще одним важливим процесом, пов'язаним з цією речовиною, була його гідратація. Пропілену в роки початку його застосування було досить багато. І все це завдяки винайденим різними нафто- і газопереробних компаніями способам лікування пропена (так іноді теж називають описується речовина). При крекінгу нафти він був побічним продуктом, а коли виявилося, що його похідне, ізопропіловий спирт, є основою для синтезу безлічі корисних для людства речовин, багато фірм, такі як BASF, запатентували свій спосіб його виробництва і почали масову торгівлю цим з'єднанням. Гідратація пропілену була випробувана і застосована раніше полімеризації, саме тому ацетон, пероксид водню, ізопропіламін почали виробляти раніше поліпропілену.
Дуже цікавий процес виділення пропена з нафти. Саме до нього ми зараз і звернемося.
виділення пропілену
Насправді в теоретичному розумінні основним способом є лише один процес: піроліз нафти і попутних газів. Але ось технологічних реалізацій - просто море. Справа в тому, що кожна компанія прагне отримати унікальний спосіб і захистити його патентом, а інші такі ж компанії також шукають свої способи, щоб все-таки виробляти і продавати пропен як сировину або ж перетворювати його в різні продукти.
Піроліз ( "піро" - вогонь, "ліз" - руйнування) - хімічний процес розпаду складної і великої молекули на більш дрібні під дією високої температури і каталізатора. Нафта, як відомо, являє собою суміш вуглеводнів та складається з легких, середніх і важких фракцій. З перших, найбільш низькомолекулярних, і отримують пропен і етан при піролізі. Проводять цей процес в спеціальних печах. У самих передових фірм-виробників цей процес технологічно різниться: одні використовують пісок в якості теплоносія, інші - кварц, треті - кокс; можна також розділити печі по їх будові: бувають трубчасті і звичайні, як їх називають, реактори.
Але процес піролізу дозволяє отримати недостатньо чистий пропен, так як, окрім нього, там утворюється величезна безліч вуглеводнів, які потім доводиться розділяти досить енерговитратними способами. Тому для отримання більш чистого речовини для подальшої гідратації застосовують також дегидрирование алканів: в нашому випадку - пропану. Так само, як і полімеризація, вищеописаний процес просто так не відбувається. Відщеплення водню від молкули граничного вуглеводню відбувається під дією каталізаторів: оксиду тривалентного хрому та оксиду алюмінію.
Ну а перш ніж перейти до розповіді про те, як відбувається процес гідратації, звернемося до будови нашого непредельного вуглеводню.
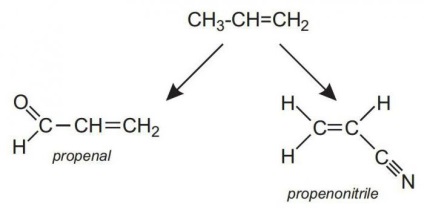
Особливості будови пропілену
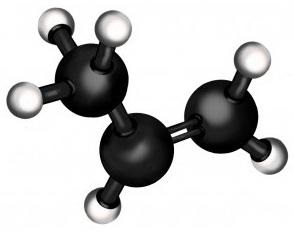
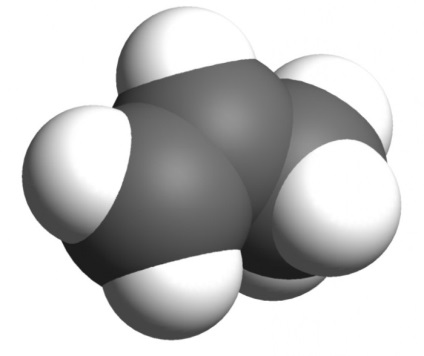
Пропен сам по собі - лише другий член ряду алкенів (вуглеводні з одним подвійним зв'язком). За легкості він поступається лише етилену (з якого, як можна здогадатися, роблять поліетилен - наймасовіший полімер в світі). У звичайному стані пропен - газ, як і його "родич" з сімейства алканів, пропан.
Але суттєва відмінність пропану від пропена - в тому, що останній має в своєму складі подвійну зв'язок, яка докорінно змінює його хімічні властивості. Вона дозволяє приєднувати до молекули непредельного вуглеводню інші речовини, в результаті чого утворюються сполуки з зовсім іншими властивостями, часто дуже важливими для промисловості та побуту.

теорія гідратації
Для початку звернемося до більш загального процесу - сольватації, - який включає в себе також і описану вище реакцію. Це хімічне перетворення, яке полягає в приєднанні молекул розчинника до молекул розчиненої речовини. При цьому вони можуть утворювати нові молекули, або ж так звані сольвати, - частинки, що складаються з молекул розчиненої речовини і розчинника, пов'язаних електростатичним взаємодією. Нас цікавить тільки перший вид речовин, адже при гідратації пропілену переважно утворюється саме такий продукт.
При сольватации вищеописаним способом молекули розчинника приєднуються до розчинених речовин, виходить нове з'єднання. У органічної хімії при гідратації переважно утворюються спирти, кетони і альдегіди, проте є і кілька інших випадків, наприклад освіту гликолей, але їх ми торкатися не будемо. Насправді цей процес дуже простий, але в той же час досить складний.

механізм гідратації
Подвійний зв'язок, як відомо, складається з двох видів з'єднання атомів: пі і сигма-зв'язків. Пі-зв'язок при реакції гідратації розривається завжди першою, так як вона менш міцна (володіє меншою енергією зв'язку). При її розриві утворюються дві вакантні орбіталі у двох сусідніх атомів вуглецю, які можуть утворити нові зв'язки. Молекула води, існуюча в розчині у вигляді двох частинок: гідроксид-іона і протона, здатна приєднуватися по розірвалася подвійного зв'язку. При цьому гідроксид-іон приєднується до центрального атому вуглецю, а протон - до другого, крайнього. Таким чином, при гідратації пропілену переважно утворюється пропанол 1, або ізопропіловий спирт. Це дуже важлива речовина, так як при його окисленні можна отримати ацетон, масово використовуваний в нашому світі. Ми сказали, що він утворюється переважно, проте це не зовсім так. Треба сказати так: єдиний продукт утворюється при гідратації пропілену, і це - ізопропіловий спирт.
Це, звичайно, все тонкощі. Насправді все можна описати набагато простіше. І зараз ми дізнаємося, як же в шкільному курсі записують такий процес, як гідратація пропілену.
Реакція: як вона відбувається
У хімії все прийнято позначати просто: за допомогою рівнянь реакцій. Ось і хімічне перетворення обговорюваного речовини можна описати таким способом. Гідратація пропілену, рівняння реакції якої дуже просте, проходить в дві стадії. Спочатку розривається пі-зв'язок, що входить до складу подвійної. Потім молекула води у вигляді двох частинок, гідроксид-аніону і катіона водню, підходить до молекули пропілену, що має на даний момент два вакантних місця для утворення зв'язків. Гідроксид-іон утворює зв'язок з менш гідрогенізовані атомом вуглецю (тобто з таким, до якого приєднано меншу кількість атомів водню), а протон, відповідно, - з рештою крайнім. Таким чином, виходить один-єдиний продукт: граничний одноатомний спирт изопропанол.
Як записати реакцію?
Зараз ми дізнаємося, як хімічною мовою записати реакцію, яка відображатиме такий процес, як гідратація пропілену. Формула, яка нам знадобиться: CH2 = CH - CH3. Це формула вихідної речовини - пропена. Як можна бачити, у нього є подвійний зв'язок, позначена знаком "=", і саме в це місце буде прісоедняться вода, коли буде відбуватися гідратація пропілену. Рівняння реакції можна записати так: CH2 = CH - CH3 + H2 O = CH3 - CH (OH) - CH3. Гідроксильна група в дужках означає, що ця частина знаходиться не в площині формули, а нижче або вище. Тут ми не можемо показати кути між трьома групами, що відходять від середнього атома вуглецю, але скажімо, що вони приблизно рівні між собою і складають по 120 градусів.
Де це застосовується?
Ми вже говорили, що отримується в ході реакції речовина активно використовується для синтезу інших життєво важливих нам речовин. Воно дуже схоже за будовою на ацетон, від якого відрізняється тільки тим, що замість гидроксогрупп там стоїть кетогруппу (тобто атом кисню, з'єднаний подвійним зв'язком з атомом азоту). Як відомо, сам ацетон знаходить застосування в розчинниках і лаках, але, крім цього, він застосовується в якості реагенту для подальшого синтезу більш складних речовин, таких як поліуретани, епоксидні смоли, оцтовий ангідрид і так далі.
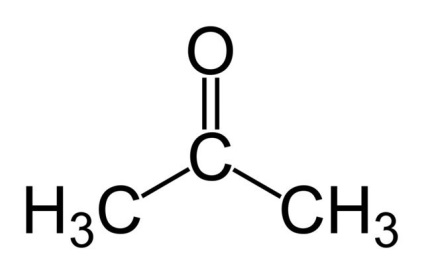
Реакція отримання ацетону
Думаємо, не зайвим буде описати перетворення ізопропілового спирту в ацетон, тим більше що реакція ця не така складна. Для початку пропанол випаровують і при 400-600 градусах за Цельсієм оксіляют киснем на спеціальному каталізаторі. Дуже чистий продукт виходить при проведенні реакції на срібній сітці.

рівняння реакції
Не будемо вдаватися в подробиці механізму реакції окислення пропанолу в ацетон, так як він дуже складний. Обмежимося звичайним рівнянням хімічного перетворення: CH3 - CH (OH) - CH3 + O2 = CH3 - C (O) - CH3 + H2 O. Як видно, на схемі все досить просто, але варто заглибитися в процес, і ми зіткнемося з рядом труднощів .
висновок
Ось ми і розібрали процес гідратації пропілену і вивчили рівняння реакції і механізм її протікання. Розглянуті технологічні принципи лежать в основі реальних процесів, що відбуваються у виробництві. Як виявилося, вони не дуже складні, проте мають реальну користь для нашого повсякденного життя.
