Всі зустрічаються в природі амінокислоти володіють загальною властивістю - амфотерні (від грец. Amphoteros - двосторонній), тобто кожна амінокислота містить як мінімум одну кислотну і одну основну групи. Загальний тип будови # 945; -амінокислот може бути представлений в наступному вигляді:
Як видно із загальної формули, амінокислоти будуть відрізнятися один від одного хімічною природою радикала R, що представляє групу атомів в молекулі амінокислоти. пов'язану з # 945; -вуглецевим атомом і не бере участь в утворенні пептидного зв'язку при синтезі білка. Майже все # 945; -амино- і # 945; -карбоксільние групи беруть участь в утворенні пептидних зв'язків білкової молекули. втрачаючи при цьому свої специфічні для вільних амінокислот кислотно-основні властивості. Тому все розмаїття особливостей структури і функції білкових молекул пов'язано з хімічною природою і фізико-хімічними властивостями радикалів амінокислот. Саме завдяки їм білки наділені рядом унікальних функцій, не властивих іншим биополимерам. і володіють хімічною індивідуальністю.
Класифікація амінокислот розроблена на основі хімічної будови радикалів, хоча були запропоновані й інші принципи. Розрізняють ароматичні і аліфатичні амінокислоти. а також амінокислоти. містять сірку або гідроксильні групи. Часто класифікація заснована на природі заряду амінокислоти. Якщо радикал нейтральний (такі амінокислоти містять тільки одну амино- і одну карбоксильну групи), то вони називаються нейтральними амінокислотами. Якщо амінокислота містить надлишок амино- або карбоксильних груп. то вона називається відповідно основній або кислій амінокислотою.
Сучасна раціональна класифікація амінокислот заснована на полярності радикалів (R-груп), тобто здатності їх до взаємодії з водою при фізіологічних значеннях рН (близьких до рН 7,0). Розрізняють 5 класів амінокислот. містять такі радикали: 1) неполярні (гідрофобні); 2) полярні (гідрофільні); 3) ароматичні (здебільшого неполярні); 4) негативно заряджені і 5) позитивно заряджені. У представленій класифікації амінокислот (табл. 1.3) наведено найменування, скорочені англійські і російські позначення і однобуквені символи амінокислот. прийняті у вітчизняній і зарубіжній літературі, а також значення ізоелектричної точки (РІ) і молекулярної маси (М). Окремо даються структурні формули всіх 20 амінокислот білкової молекули.
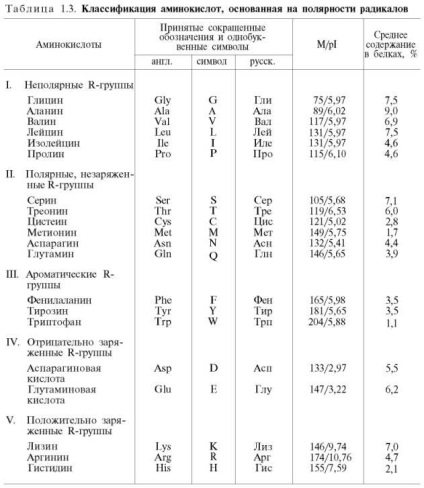
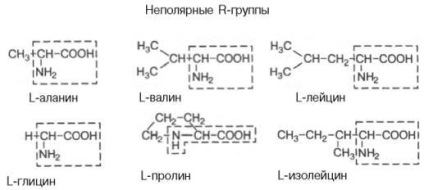
Полярні, незаряджені R-групи
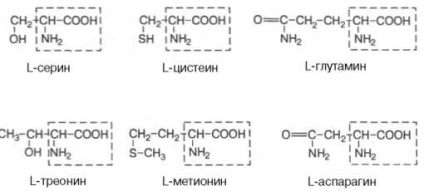
Негативно заряджені R-групи
Позитивно заряджені R-групи
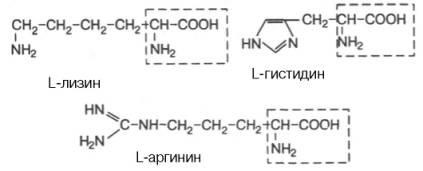
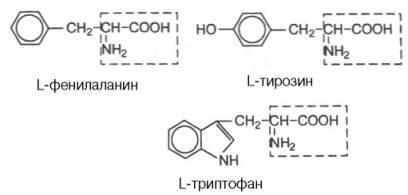
Перераховані амінокислоти присутні в різних кількісних співвідношеннях і послідовності в тисячах білків. хоча окремі індивідуальні білки не містять повного набору всіх цих амінокислот. Окрім наявності в більшості природних білків 20 амінокислот. в деяких білках виявлені похідні амінокислот. оксипроліну. оксілізін, дийодтирозин, фосфосерин і фосфотреонин (останні дві амінокислоти представлені в розділі 2):
Крім зазначених, ряд # 945; -амінокислот виконує важливі функції в обміні речовин. хоча і не входить до складу білків. зокрема орнітин. цитрулін, гомосерін, гомоцистеїн, цістеінсульфіновая кислота. диоксифенилаланин і ін.
