Механізми розвитку (патогенез) ускладнень інфаркту міокарда
Лікування пацієнтів з гострим інфарктом міокарда (ІМ) до теперішнього часу стало надзвичайно успішним. Одночасно зі зменшенням загальної летальності від ІХС починаючи з 1960-х рр. частота випадків внутрішньолікарняної летальності знизилася приблизно з 30 до 7% при своєчасному лікуванні ІМ. 50% випадків смерті від гострого ІМ відбувається в межах 1 годину з його початку - більшість цих пацієнтів не встигають потрапити в лікарню.
Рутинна терапія при гострому інфаркті міокарда (ІМ) полягає в застосуванні ацетилсаліцилової кислоти і гепарину (запобігають подальший тромбоз), кисню (зменшує ішемію), нітратів (індукують розширення судин і усувають їх спазм), b-адренергічних інгібіторів (b-блокатори знижують потребу серця в кисні і ризик аритмії), інгібіторів ангіотензинперетворюючого ферменту (обмежують розширення шлуночків).
Крім того, проводять втручання для усунення обструкції, включаючи введення фібринолітичних агентів, коронарну ангіопластику з установкою стента або без нього і коронарне шунтування. Вибір терапії залежить від клінічної картини і можливостей лікувального закладу. Ангіопластика є високоефективним методом в досвідчених руках, але майже такий же ефект може дати фибринолитическая терапія. До факторів, асоційованим з поганим прогнозом, відносять похилий вік, жіноча стать, цукровий діабет і інфаркти в анамнезі (кумулятивна втрата функціонуючого міокарда).
У багатьох пацієнтів, які перенесли гострий інфаркт міокарда (ІМ), незважаючи на терапевтичні заходи, розвиваються одне або кілька ускладнень, в т.ч.
- порушення скорочувальної функції серця. ІМ викликає порушення функції лівого шлуночка, приблизно пропорційне величині ураженої області. Зазвичай присутній лівошлуночкова недостатність деякій мірі з гіпотензією, венозним застоєм в легенях і інтерстиціальним легеневим транссудатом з можливим розвитком вираженого набряку легенів і порушеннями дихання. Тяжке порушення систолічної функції серця (кардіогенний шок) після ІМ виникає у 10-15% пацієнтів, частіше у перенесли раніше обширний інфаркт (ураження> 40% лівого шлуночка). Летальність від кардіогенного шоку становить 70% і обумовлює 75% випадків внутрішньолікарняної летальності;
- аритмії. У багатьох пацієнтів після перенесеного ІМ відзначаються підвищена збудливість міокарда та / або порушення проведення, які можуть привести до розвитку фатальних аритмій. Асоційовані з ІМ аритмії включають синусовую брадикардію, блокаду проведення (асистолию), тахікардію, передчасне скорочення шлуночків або шлуночкову тахікардію і фібриляцію шлуночків. Оскільки частина атріовентрикулярної провідної системи (пучок Гіса) локалізована в міокарді нижнього відділу міжшлуночкової перегородки, інфаркт в цій області також може асоціюватися з блокадою проведення;
- розрив серця. Синдроми розриву серця виникають в результаті розм'якшення і ослаблення некротизированного, а слідом за тим і запаленого міокарда. Ці синдроми включають розрив вільної стінки шлуночка (найчастіше) з гемоперикардом і тампонадой серця; розрив міжшлуночкової перегородки (менш часто), що призводить до гострого ДМШП і артеріовенозне шунтування; відрив папілярних м'язів, що призводить до важкої гострої мітральної регургітації. Розрив вільної стінки шлуночка найбільш часто відбувається на 3-7-му добу після ІМ (в середньому на 5-ту добу з коливаннями від 1 до 10 діб), коли коагуляційний некроз, нейтрофильная інфільтрація і лізис сполучної тканини міокарда відчутно послаблюють вражений інфарктом міокарда.

(A-В) Синдроми розриву серця: розрив передньої стінки лівого шлуночка при гострому інфаркті (стрілка) (А);
розрив міжшлуночкової перегородки (стрілка) (Б);
повний відрив некротизированной папілярного м'язу (В).
Найбільш часто місцем постинфарктного розриву лівого шлуночка є його переднелатеральная стінка на рівні середини шлуночка. Фактори ризику такого типу розривів: вік старше 60 років, жіноча стать, предсуществующей артеріальна гіпертензія. Це ускладнення у пацієнтів без попереднього ІМ зустрічається рідше. Гострі розриви вільної стінки лівого шлуночка швидко призводять до летального результату. Іноді адгезія перикарда в області інфаркту частково блокує розрив і може стати причиною утворення помилкової аневризми (локалізована гематома, сполучена з шлуночком). Стінка помилкової аневризми складається тільки з епікарда і прилеглого до нього париетального перикарда, тому не виключений її подальший розрив;
- перикардит. Фібринозний або фібринозно-геморагічний перикардит (синдром Дресслера) розвивається на 2-3-у добу після трансмурального інфаркту як результат запалення міокарда;
- інфаркт правого шлуночка. Ізольований інфаркт правого шлуночка спостерігається рідко, проте інфаркт деякої частини міокарда правого шлуночка часто супроводжує ішемічне ураження прилеглої задньої області лівого шлуночка і міжшлуночкової перегородки. Будь-які інфаркти правого шлуночка викликають гостру правожелудочковую недостатність, яка призводить до застою крові в венозної системі і гіпотензії;
- розширення зони інфаркту. У ділянках, прилеглих до існуючого інфаркту, можуть виникати нові вогнища некрозу;
- поширення інфаркту. Результатом ослаблення некротизированной м'язи може бути непропорційний розтягнення, витончення і розширення зони інфаркту (особливо в разі антеросептальних інфарктів), часто в поєднанні з пристінковим тромбозом;
- пристінковий тромбоз. При будь-якому інфаркті поєднання порушення скоротливості (що викликає стаз) і пошкодження ендокарда (що створює тромбогенного поверхню) підсилює ризик розвитку пристінкового тромбозу і потенційної тромбоемболії;
- аневризма шлуночка. На відміну від помилкової аневризми в освіті істинної аневризми шлуночка бере участь тільки міокард, що піддався рубцевих змін. Аневризма шлуночка являє собою пізніше ускладнення великих трансмуральних інфарктів, що зазнали раннє поширення. Тонка рубцева тканина стінки аневризми парадоксальним чином випинається під час систоли. Ускладнення: внутрістеночних тромбоз, аритмія і серцева недостатність. Загроза розриву еластичною фіброзної стінки зазвичай відсутня;
- дисфункція папілярних м'язів. Як було зазначено раніше, після ІМ може статися відрив папілярних м'язів. Найчастіше постинфарктная митральная регургітація виникає в результаті ішемічної дисфункції папілярних м'язів і підлягає міокарда, а пізніше - як наслідок фіброзу і укорочення папілярних м'язів або розширення шлуночка;
- прогресуюча пізня серцева недостатність.

б - раннє поширення передневерхушечного інфаркту з тонкою стінки (стрілка) і пристінковим тромбом.
в - велика верхівкова левожелудочковая аневризма
Ризик специфічних постінфарктних ускладнень і прогноз залежать головним чином від величини інфаркту, його локалізації та глибини (субендокардіальний або трансмуральний інфаркт). Великі трансмуральний інфаркти зумовлюють високу ймовірність кардіогенного шоку, аритмій і ХСН.
Пацієнти з передніми трансмуральний інфаркт мають найбільш високий ризик розриву вільної стінки шлуночка, розширення зони інфаркту, внутрістеночних тромбозу і аневризми. На відміну від цього задні трансмуральний інфаркти ризиковані таких ускладнень, як блокада проведення та / або залучення правого шлуночка. Якщо розрив міжшлуночкової перегородки відбувається в її задньому відділі, лікування більш складне. В цілому у пацієнтів з переднім інфарктом прогноз гірше, ніж з нижнім (заднім) інфарктом. При субендокардіальних інфарктах перикардит, розрив і аневризми спостерігаються лише в рідкісних випадках.
На додаток до наслідків репарації уражених при інфаркті тканин неушкоджені сегменти шлуночка гіпертрофуються і розширюються. Такі зміни отримали назву ремоделювання шлуночків. Компенсаторна гіпертрофія неураженої міокарда спочатку гемодинамически сприятлива. Адаптивний ефект може бути нейтралізований розширенням шлуночка (в присутності або за відсутності аневризми) і підвищеною потребою міокарда в кисні, що може посилити ішемію і викликати пригнічення функції серця.
Також можуть змінитися форма і еластичність серця через утворення рубця і гіпертрофії, що ще більше знижує серцевий викид. Деякі з цих несприятливих ефектів вдається послабити інгібіторами ангіотензинперетворюючого ферменту (зменшують розширення шлуночка після ІМ).
Довготривалий прогноз після ІМ залежить від багатьох факторів. Найбільш важливі з них - якість залишкової функції лівого шлуночка і ступінь обструкції судин, перфузируются життєздатний міокард. Загальна смертність протягом першого року становить 30%. Протягом кожного наступного року з тих, що вижили вмирають 3-4%.
Профілактика інфаркту шляхом контролю факторів ризику у осіб, які не мали ІМ (первинна профілактика), і запобігання повторного інфаркту у осіб, які перенесли гострий ІМ (вторинна профілактика), - це важливі стратегії, яким приділяють велику увагу. У цьому напрямку досягнуті значні успіхи.
Співвідношення причин, патофізіології і наслідків інфаркту міокарда (ІМ) представлено на малюнку нижче, включаючи можливий результат хронічної ІХС і раптову смерть.
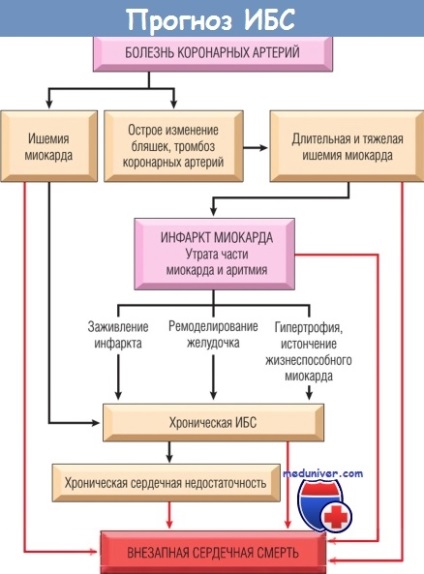
Показано взаємозв'язок хвороби коронарних артерій, гострого зміни бляшок, ішемії міокарда,
інфаркту міокарда, хронічної ІХС, хронічної серцевої недостатності і раптової серцевої смерті.