Чистота розчинів має важливе значення для всього гідрометалургійного процесу. При роботі заводу на чистих розчинах зменшується витрата електроенергії на тонну цинку, збільшується продуктивність обладнання, поліпшуються процеси відстоювання і фільтрації, знижується собівартість продукції.
Присутні в розчинах домішки в залежності від способу очищення від них можна розділити на наступні групи:
1) залізо, алюміній, мідь, миш'як, сурма, германій, індій, галій, кремнезем;
2) мідь, кадмій, кобальт, талій;
3) кобальт, хлор, фтор;
4) калій, натрій, магній, марганець.
Домішки першої групи видаляються з розчину за допомогою гідролізу, соосаждения, адсорбції і коагуляції. Очищення від домішок другої групи заснована на процесі електрохімічного витіснення більш негативними металами. Для третьої групи домішок використовуються методи хімічного очищення з утворенням сполук, що не розчинних у водних розчинах. Домішки четвертої групи накопичуються в розчинах і від них звільняються тільки шляхом виведення частини розчину з виробничого циклу.
З викладеного видно, що мідь і кобальт можна видалити з розчину різними способами.
У поняття -гідролітіческая »очищення входять методи очищення, засновані на гідролізі і осадженні домішок при підвищенні pH пульпи.
Гідролітична очищення зазвичай поєднується з вилуговуванням недогарка і протікає в процесі нейтралізації кислоти. Цим методом видаляються домішки, які осідають з розчину при менших значеннях pH, ніж для гідроксиду цинку.
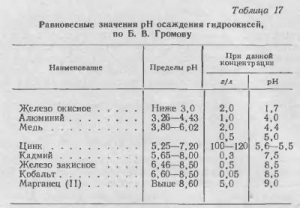
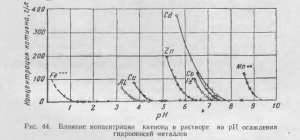
Осадження гідроксидів відбувається при певному pH, яке в свою чергу залежить від концентрації катіона в розчині, від температури і іонної сили розчину. Найбільш повні дослідження гідролізу солей важких металів проведені Б. В. Громовим, У своїй роботі він наводить ряд осадження гідроксидів (табл. 17) Вплив концентрації металу на pH осадження його гідроксиду показано на рис. 44.
Як видно з наведених даних, нейтральні пульпи при вмісті цинку 100-120 г / л мають pH = 5,6 / 5,5, при якій залізо, алюміній, мідь і інші метали, що мають pH осадження менше 5,6, випадають з розчину .
Залізо знаходиться в кислому розчині в формі сульфату закису FeSO4 і сульфату окису Fe2 (SO4) 3. Концентрація тривалентного заліза зважаючи на присутність відновників в кислому пульпи завжди менше, ніж двовалентного. З'єднання заліза гідралізуют по реакціях
Гідрат закису заліза швидко окислюється, при вмісті в розчині вільного кисню до гідрату окису
4Fe (OH) 2 + O2 + 2Н2О = 4Fe (OH) 3.
Насправді в умовах вилуговування недогарка відбувається осадження основних сульфатів заліза, так як гідроксиду в чистому вигляді осідають лише з дуже розбавлених розчинів. Двовалентне залізо в умовах нейтрального вилуговування гидролизует в незначній мірі. Для повноти осадження заліза необхідно перевести його в окисну форму.
Окислення заліза проводиться трьома методами, марганцевої рудою, киснем повітря та сполуками міді.
Пиролюзит, що міститься в марганцевої руди, окисляє залізо в кислому середовищі за реакцією
2FeSО4 + MnO2 + 2H2SО4 = Fe2 (SO4) 3 + MnSO4 + 2Н2О.
Деякі заводи для окислення невеликих кількостей заліза користуються перманганатом калію Окислення протікає по рівнянню
10FeSO4 + 2КМnO4 + 8H2SO4 = 5Fe2 (SO4) 3 + K2SO4 + 2MnSO4 + 8Н2O.