Визначте склад реакційної суміші до і після реакції з урахуванням виходу продуктів реакції.
Складіть таблицю матеріального балансу.
1. Хімічна реакція для розрахунку матеріального балансу
NH4Cl + NaOH = NaCl + NH3

2. Характеристики вихідних розчинів
СМ (NH4 Cl) = 4 моль / л; mр-ра (NH4 Cl) = 2,3 кг; (NH4 Cl) = 1,065 г / мл;
Сп (NaOH) = 2 моль / л; mр-ра (NaOH) = 2,5 кг; (NaOH) = 1,250 г / мл;
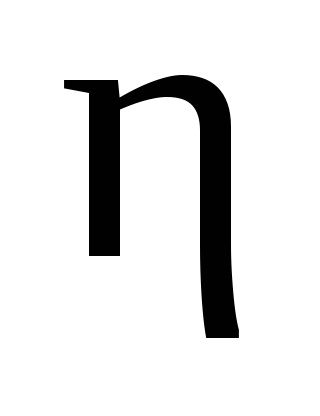
Проведемо розрахунок речовин приходять в реакцію
Проведемо розрахунок речовин утворилися в реакції (Продукти реакції) Витрата:
Обсяг приходить розчину NH4 Cl:
Кількість NH4 Cl в приходить розчині:
Маса NH4 Cl в приходить розчині:
Маса води в приходить розчині хлориду амонію NH4 Cl:
Обсяг приходить розчину лугу (NaOH):
Маса речовини NaOH в приходить розчині:
Кількість NaOH в приходить розчині:
Маса води в розчині лугу:
Кількість прореагировавшего NaOH з урахуванням виходу продуктів реакції:
Завдання 4. Визначте рН середовища після реакції.
Після завершення реакції в розчині присутні речовини: NH4 Cl, NaOH, NaCl, частково розчинений аміак. На реакцію середовища можуть впливати NaOH і гідролізіруемий NH4 Cl.
моль / л, так як, то
Концентрацію іонів водню, що утворюються при гідролізі NH4 Cl, обчислимо через константу і ступінь гідролізу:
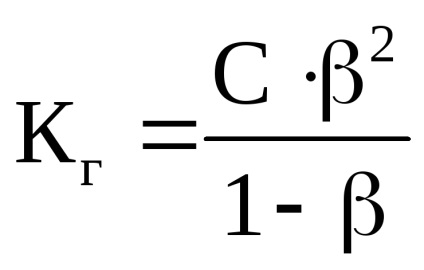
де С - концентрація солі, моль / л;

Так як ступінь гідролізу значно менше одиниці, то вираз набуває вигляду:
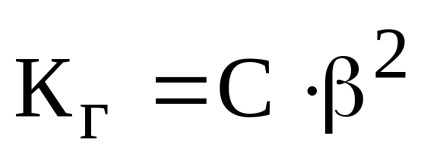
Константа гідролізу солі слабкої основи і сильної кислоти розраховуються за формулою:
,
.
Так як C (HCl) = C (NH4 Cl), то
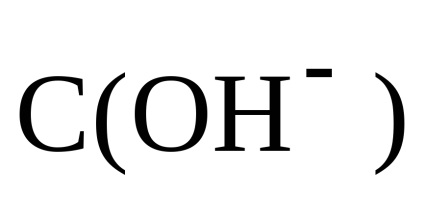
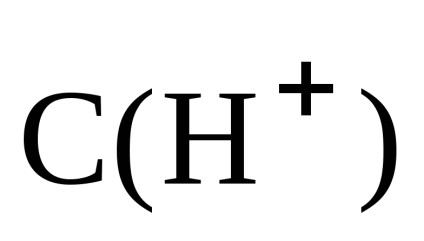
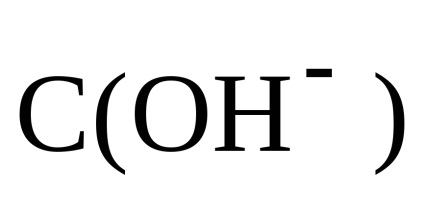
Отже, рН розчину вважаємо за концентрацією лугу:
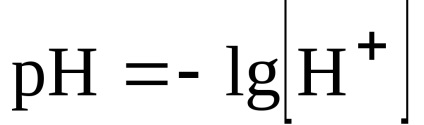
.
ВАРІАНТИ семестрових завдань ДЛЯIIСЕМЕСТРА