Технологічні властивості аміаку.
Аміак (NH3) - безбарвний газ з різким запахом і температурою кипіння -33,4 # 730; С і температурою плавлення -77,8 # 730; С аміак добре розчинний у воді (750 літрів в літрі води), обмежено розчинний в органічних розчинниках .
При взаємодії з водою аміак утворює гідрати наступного складу:
Незначна кількість розчинених у воді молекул аміаку іонізує в результаті реакції:
Ступінь дисоціації 0.004.
Рідкий аміак розчиняє лужні і лужноземельні метали, фосфор, сірку, йод і багато інших неорганічні і органічні сполуки.
При температурі 1300 ° С аміак дисоціює на азот і водень:
Сухий аміак утворює з повітрям вибухові суміші, межі вибуховості яких залежать від температури.
Світове виробництво аміаку становило в 1980 році більше 90 млн. Тонн.
Перший завод по проізводствуамміака був пущений в 1913 році з продуктивністю 25 т на добу.
Сировиною у виробництві аміаку є азотоводородная суміш (АВС) складу N2: H2 = 1: 3. Ресурси атмосферного азоту практично невичерпні, тому виробництво аміаку визначається в основному способом виробництва водню.
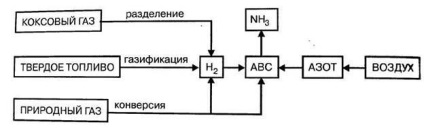
Малюнок 4.3. - Сировинні ресурси виробництва аміаку.
Азот одержують ректифікацією (перегонкою) зрідженого атмосферного повітря.
Водень для синтезу аміаку може бути отриманий:
1. поділом зворотного коксового газу,
2. газифікацією твердого палива,
3. конверсією природного газу (метану або його газоподібних гомологів),
4. конверсією оксиду вуглецю з водяною парою,
5. крекингом метану
6. електролізом або термічним розкладанням води
Основне значення мають методи конверсії метану і оксиду вуглецю, а також поділ коксового газу.
Для перспективних планів широкого застосування водню в промислових і енергетичних цілях планується його великомасштабне виробництво з води - найдешевшого сировини, запаси якого необмежені. Існуючі і розробляються методи виробництва водню з води діляться на три групи:
1. електроліз води
2. термохимические методи
3. комбіновані термо-і електрохімічні методи.
ЕЛЕКТРОЛІЗ - найбільш освоєний метод виробництва водню з води, в даний час він використовується в невеликих масштабах при наявності дешевої електроенергії. Електрохімічні процеси засновані на взаємних перетвореннях електричної енергії в хімічну і навпаки. Переваги електрохімічних процесів - їх простота в аппаратурном оформленні, малостадійность технологічного процесу, висока чистота одержуваних продуктів, надостіжімая для хімічних способів і ін. Основний недолік електролізу - висока витрата електроенергії, вартість якої становить основну частку в собівартості продуктів - більше 90%. Більш того, при промисловому електролізі водних розчинів коефіцієнт використання енергії - не більше 50 - 60%, що ще більше підвищує вартість продуктів електролізу. При отриманні водню електролізом води застосовують в якості електроліту водні розчини кислот, лугів або солей, так як електропровідність чистої води мізерно мала - при 18 ° С питома електропровідність води становить (2-6) × 10 -10 См × м -1. Найчастіше застосовують лужні електроліти, найменш агресивні для конструкційних матеріалів електролізерів. Виділення водню відбувається на катоді по реакції:
Сумарний ККД виробництва водню електролізом води з використанням електроенергії, вироблюваної атомною станцією, становить не більше 20 - 30%, і це негативно позначається на собівартості водню. Зниження собівартості електролітичного водню може бути досягнуто удосконаленням конструкції електролізерів, їх здешевленням, і, що амое головне, застосуванням дешевої електроенергії. Як основна перспектива, розглядається можливість харчування водневих електролізерів «провальною» енергією атомних станцій, тобто використанням електроенергії в ті періоди, коли станції недовантажені, наприклад, в нічні години.
Термохимический метод отримання водню заснований на розкладанні води за допомогою теплової енергії, яку передбачається отримувати від атомних реакторів з гелієвим охолодженням, використовуючи теплоту газового теплоносія на виході з реактора. Безпосереднє розкладання води по реакції
нездійсненно, так як при необхідній для цього високій температурі (близько 1000 ° С) константа рівноваги реакції мізерно мала (10 -6). Реалізація процесу можлива заміною реакції прямого розкладу води термохимическим циклом, що складається з декількох стадій, для кожного з яких значення константи рівноваги були б прийнятні для практики. Розроблено та запропоновано безліч термохімічних циклів для розкладання води при температурах, доступних з точки зору використання теплоти охолоджуючих газів ядерних реакторів. У більшості із запропонованих циклів проміжні речовини мають високу спорідненість до водню, або до кисню - це галогени, елементи IV групи (сірка), метали II групи (Mg, Ca. Ba) і перехідні елементи зі змінним ступенем окислення (V, Fe). Нижче наведено один з прикладів термохімічного циклу реакцій, що ведуть до розкладання води на H2 і O2:
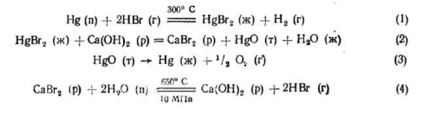
Весь термохимический цикл розкладання води являє собою замкнутий цикл, так як всі вихідні реагенти відокремлюються від продуктів реакції і повертаються в цикл, за винятком води, що витрачається на утворення водню і кисню. Максимальна температура реакцій не перевищує 700 ° С і може бути забезпечена теплоносієм на виході їх атомного реактора на рівні 800 - 900 ° С.
В даний час жоден із запропонованих термохімічних циклів ще не реалізований в промисловості і значення ККД циклів, а так само розрахунки витрат на отримання водню цим методом поки не визначені.
Комбінований метод виробництва водню полягає в комбінуванні термо- і електрохімічних стадій процесу. Очікувані переваги комбінованого методу полягають у тому, що можуть бути використані гідності кожного з розглянутих способів: електрохімічний добре освоєний, має просте апаратурнеоформлення, а термохимический економічніший, але мало освоєний і включає стадії, важкі для промислового здійснення.
Прикладом може служити сірчанокислотний комбінований цикл отримання водню і кисню з води. Це двоступеневий процес, що включає 2 стадії
1. термохімічна - ендотермічна реакція, що здійснюється при 900 ° С
2. низькотемпературний електрохімічний процес:
Остання реакція може бути реалізована тільки шляхом електролізу, так як її константа рівноваги і теоретичним вихід водню надзвичайно малі. Джерелом енергії для комбінованої установки може служити атомний газовий реактор, що постачає отбросной теплотою термохімічну стадію і електроенергією електрохімічний стадію. Розрахункові витрати для комбінованої установки менше, ніж для прямого електролізу води. Сумарний ККД процесу повинен скласти 35 - 37%. На думку фахівців комбінування термохімічних і електрохімічних стадій - найбільш перспективний напрямок великомасштабного виробництва водню з води.
Основним методом отримання водню для синтезу аміаку є каталітична конверсія метану. Сировиною для цього методу служить природний і попутний газ. що містить до 90-98% метану.