В основі захворювання лежить прогресуюча дегенерація альфа-мотонейронів передніх рогів спинного мозку, що приводить до формування симетричного млявого парезу поперечно-смугастих м'язів c їх переродженням. Встановлено, що генетичною основою хвороби є мутація гена, картірован в області довгого плеча хромосоми 5 в сегменті 5q11.2-13.3, який отримав назву НСА-локусу. У цьому локусі локалізована «ген життєздатності моторного нейрона» (survival motor neuron - SMN). Встановлено характер мутації у вигляді мікроделеції в 7-м і / або 8-м (теломерной) екзонах SMN-гена. СМА I типу - найбільш важко протікає захворювання, що пов'язано не тільки з гомозиготною делецией SMN-гена, але і з дефектами «сусіднього» NAIP-гена (neuronal apoptosis inhibitor protein, ген білка-інгібітора загибелі нейрона).
Залежно від часу початку і типу клінічного перебігу захворювання СМА підрозділяють на 4 типи. Спинальная м'язова атрофія I типу, або хвороба Верднига-Гоффмана (В-Г), виникає у віці до 6 міс. і характеризується м'язовою слабкістю. Клінічна маніфестація відзначається в дитячому віці: початок хвороби в 5 - 6 місяців. Частота хвороби В-Г оцінюється як 1:13 000 новонароджених, гетерозиготное носійство зустрічається з частотою 1. Більшість дітей зі СМА I типу гине у віці до двох років. Типовий клінічнийсимптомокомплекс при СМА I типу формується до 6-місячного віку, коли спостерігаються рухові порушення у вигляді периферичного паралічу скелетної мускулатури. Дуже рано згасають сухожильні і періостальних рефлекси, виявляється дифузна м'язова гіпотонія. У хворих з СМА I типу до 6 місяців від народження виявляється «синдром млявого дитини». Батьки відзначають у дітей недостатню рухову активність, в ряді випадків надлишкову масу тіла, характерну пасивну позу дитини з відведенням і зовнішньої ротацією стегон ( «поза жаби»). М'язові атрофії носять виражений характер, але виявлення їх утруднено на першому році життя внаслідок добре розвиненою жирової клітковини. Захворювання має характерну форму залучення скелетної мускулатури в патологічний процес - спочатку уражаються проксимальні відділи ніг, потім патологічний процес поширюється на м'язи тулуба, рук, шиї. Паралельно з м'язовою атрофією наростають і периферичні парези. Діти не можуть вставати, перестають брати в руки іграшки, не можуть сидіти і тримати голову. Визначається характерний дрібний тремор пальців витягнутих рук. Швидко формуються кісткові деформації грудної клітки у вигляді кіфозу. Бульбарні симптоми представлені атрофією м'язів мови з фібрилярні посмикуваннями, парезом м'якого піднебіння зі зниженням глоткового рефлексу і утрудненням ковтання. Внаслідок ураження ядер лицьового нерва розвивається гипомимия. Атрофії і слабкість міжреберних м'язів призводить до недостатньої екскурсії легких і сприяє розвитку бронхіту, пневмонії та ателектазів легенів. Будь-яка интеркуррентная інфекція різко послаблює організм хворої дитини і погіршує перебіг основного захворювання. Порушення чутливості, координації, а також затримки психічного розвитку у дітей з СМА I типу не відзначається. Часто виявляються вегетативні порушення у вигляді помірного дистального гіпергідрозу.
CMA II і III типів. Спинальная м'язова атрофія II типу має більш пізній початок у віці 6 - 18 міс. і менш тяжкий перебіг. Діти зберігають здатність сидіти самостійно. Тривалість життя таких пацієнтів в середньому становить 10-14 років. Початок СМА III типу (юнацька форма), або хвороба Кугельберга - Веландер, варіює в віці між 18 міс. і першим-другим десятиліттям життя. Хворі з CMA III типу зберігають здатність пересуватися самостійно, але можуть часто падати або зазнавати труднощів при підйомі і спуску по сходах, бігу, нахилі, підйомі з положення сидячи. Нижні кінцівки при даному типі захворювання вражені сильніше, ніж верхні.
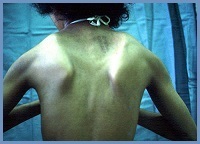
У дітей з СМА II і III типу клінічна картина представлена млявими паралічами рук і ніг, з переважанням процесу в проксимальних відділах, активні рухи зберігаються лише в дистальних відділах рук, м'язах шиї, мімічної і дихальної мускулатури. Спостерігаються генералізовані фібриляції і фасцікуляціі м'язів, виражена дифузна м'язова гіпотонія. У 85% дітей мають місце виражені атрофії міжреберних м'язів з дихальною недостатністю і негрубими бульбарними розладами. Зміни в кістково-суглобової системи представлені вираженими контрактурами великих суглобів кінцівок і кифосколиозом. Функції тазових органів збережені. Виявляються порушення вегетативної нервової системи: дистальний гіпергідроз, червоний дермографізм. Порушень чутливості та інтелекту не відзначено. Внаслідок прогресуючої дегенеративного процесу в альфа-мотонейронах спинного мозку на шийно-грудному рівні наростає атрофія в м'язах тулуба, що призводить до формування патологічного викривлення хребетного стовпа. Виражений кифосколиоз стає причиною зміни нормального біомеханізма дихального акту, зниження екскурсії легких на 25 - 30% від фізіологічної норми, виникнення больового корінцевого синдрому у дитини, ускладнює стан хворого і ускладнює догляд за ним.
СМА IV типу. Також виділяють СМА IV типу. Дане захворювання виникає в третій декаді життя і характеризується прихованим початком і повільно прогресуючим перебігом.
Диференціальний діагноз СМА I і II типів у дітей проводиться з різними варіантами вроджених міопатій, мітохондріальними енцефаломіопатія, вродженими невропатиями, артрогрипоз, атонічний-астатичними формою дитячого церебрального паралічу. Діагностика в цих випадках базується не тільки на клінічних критеріях, але і на результатах електронейроміографіческіх досліджень (ЕНМГ), ДНК-аналізі і вивченні м'язових біоптатів.
Істотну допомогу в оцінці ступеня прогресування СМА надає ЕНМГ-дослідження. У м'язах хворих СМА реєструються множинні потенціали фібриляції (ПФ), позитивні гострі хвилі (ПОВ). Ступінь вираженості ПФ і ПОВ залежить від форми і тривалості перебігу захворювання. Зниження рекрутування рухових одиниць і збільшення частоти їх імпульсації вказує на втрату мотонейронів передніх рогів спинного мозку. У хворих на пізніх стадіях СМА збереглися рухові одиниці при максимальному м'язовому напрузі працюють з частотою імпульсації в десятки герц (до 40 - 50 Гц). Як відомо, паралельно з процесом втрати мотонейронів запускаються процеси реиннервации, які призводять до зміни параметрів потенціалів рухових одиниць (ПДЕ), колатеральний спрутінг від підлягаючих зберіганню аксонів призводить до формування потенціалів збільшеною тривалістю і амплітуди, в той же час як результатом аксональной регенерації є виникнення низько- амплітудних нестабільних поліфазних ПДЕ зниженою тривалості. При грубому ураженні в м'язувідсутні нормальні ПДЕ, а реєструються тільки потенціали збільшеною або зниженою амплітуди і тривалості.
При стимуляционной ЕНМГ швидкості проведення по моторних волокнах нервів знаходяться в межах норми або незначно знижені внаслідок втрати найбільш високошвидкісних аксонів. Зниження амплітуд М-відповідей у хворих СМА від помірного до грубого відображає ступінь зниження кількості функціонуючих рухових одиниць. Результати дослідження сенсорного проведення - амплітуди ПД нервів і швидкості проведення не порушені.
Оскільки в патогенезі спінальних м'язових атрофії досі не визначені первинні біохімічні продукти патологічних генів, які беруть участь в активації механізмів дегенерації альфа-мотонейронів, ця обставина, як і раніше перешкоджає розробці шляхів ефективної терапії дітей із захворюваннями цієї групи. Під корригирующей терапією можна розуміти велику групу заходів, спрямованих на відновлення втрачених або знижених функцій окремих органів або частини органу, а також заходи, що сприяють зменшенню сили впливає патологічного фактора.
Стаціонарне коригуючий лікування складається з трьох блоків: педагогічно-психологічний супровід, медикаментозна терапія і нефармакологічне вплив на організм дитини. Медикаментозна терапія має два напрямки: по-перше, постійна терапія препаратами вальпроєвої кислоти, дозування якої розраховується індивідуально з урахуванням маси тіла дитини і коригуюча медикаментозна терапія метою, якої є підтримка оптимальних умов для функціонування нейронів ЦНС (вітаміни, вазоактивні препарати, ноотропні та антиоксидантні засоби ).
При стаціонарному лікуванні хворих також застосовується елькарнітін у вигляді ін'єкцій (в / м), а при виписці призначається рідка форма препарату (перорально) протягом 2 місяців. Поліпшити психоемоційний стан хворої дитини можна, використовуючи методи корекційної педагогіки та психотерапії. Ці методи в стаціонарних умовах реалізуються через програму педагогічно-психологічного супроводу хворої дитини, до них відносяться: арттерапія - метод психотерапії, іспользующійдля лікування і психокорекції художні прийоми і творчість (малювання, ліплення, музика, ігрова арттерапія), юінгіанская пісочна терапія і казкотерапія . У процесі творчості зменшується дія механізмів психологічного самозахисту, і у дитини з'являється можливість зміцнити свої позиції в навколишньому світі. Сеанси в сенсорній кімнаті призводять до релаксації, знімається емоційне напруження дитини, активізується сенсорна - аферентна - система, відбувається стимулювання психічної активності дитини за рахунок виникнення позитивних емоційних реакцій.
Нефармакологічне вплив на організм дитини включає в себе: масаж, ЛФК, дихальну гімнастику і процедури фізіотерапевтичної спрямованості. Масаж при СМА повинен виконуватися з мінімальною силою впливу, спрямований на поліпшення трофіки шкірних покривів і зберіганню м'язів, використовується щадне розтягування укорочених сухожиль, погладжування суглобів і паравертебрально-точковий гармонізує масаж. Тривалість сеансу - до 10 хв. Курс № 10 через день. При наявності симптоматики слабкості дихальної мускулатури виконується масаж грудної клітини для полегшення дихальних рухів. Дозована лікувальна фізкультура з елементами stretch-гімнастики, спрямована на підтримку і максимальне збереження функціональної здатності не залучених в патологічний процес м'язів. В комплекс лікування пневмопатій включена інгаляція з мінеральною водою для активації клітинного метаболізму, зменшення гіпоксії тканин, відновлення слизової бронхів, нормалізації функції зовнішнього дихання, поліпшення дренажної функції бронхів. Діти і батьки навчаються дихальної гімнастики, вокалотерапіі, в основі якої лежить вимова звуків під час активного видиху з акцентом на голосні звуки. У домашніх умовах рекомендується надування гумових куль. Процедури ФТО включають в себе наступні методики: світлолікування, ультразвук, магнітотерапію, проводяться вони через день. Коригуючі ортопедичні операції проводитимуться для корекції вторинного грудо-поперекового кіфосколіозу у дітей з діагнозом спінальна м'язова атрофія II і III типу.
Дітям з встановленим діагнозом СМА I типу рекомендовано курсове щоденну підтримку дихальної функції легень із застосуванням портативних пристроїв штучної вентиляції легенів. На початковій стадії захворювання рекомендовано використовувати неінвазивну вентиляцію, дитині подається кімнатне повітря під тиском через маску або мундштук. Для дітей з тяжким ураженням дихальної мускулатури рекомендується штучна вентиляції легенів через трахеостому сумішшю збагаченої киснем.