3. Ізотермічний процес.
Ізотермічним процесом називається процес, що протікає при постійній температурі. В цьому випадку і. тобто внутрішня енергія газу залишається постійною і все підводиться тепло витрачається на роботу.
4. Адіабатичний процес.
Процес, що протікає без теплообміну з навколишнім середовищем, називається адіабатичним. В цьому випадку . Перший початок термодинаміки для такого процесу буде мати вигляд:
тобто при адіабатичному процесі розширення або стиснення, робота відбувається газом тільки за рахунок зміни запасу внутрішньої енергії.
Виведемо рівняння адіабатичного процесу. При адіабатичному розширенні робота здійснюється за рахунок убутку внутрішньої енергії. Так як і. то
Розділивши рівняння (6) на і з огляду на останній рівняння і (8), отримаємо
де - показник адіабати.
Інтегруючи і потенціюючи останнє рівняння, одержимо рівняння Пуассона
Згідно кінетичної теорії газів з (4) і (7), отримаємо
Ця формула справедлива як для молярних, так і для питомі теплоємності газів.
Опис і теорія методу
Пропонований метод визначення показника адіабати заснований на застосуванні адіабатичного і изохорический процесів.
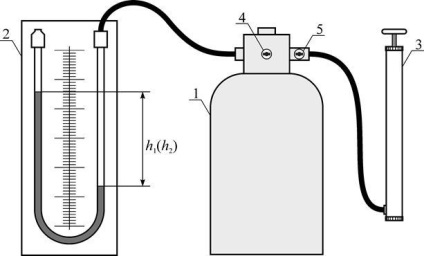
Мал. 17. Експериментальна установка
Установка складається з балона 1, з'єднаного з манометром 2 і насосом 3 (рис. 17). За допомогою крана 4 балон може бути з'єднаний з атмосферою, і відповідно, початкове тиск в ньому дорівнює атмосферному. Кран 5 служить для закриття подачі повітря з насоса. Якщо за допомогою насоса швидко накачати в балон деяку кількість повітря і закрити кран, то тиск в балоні підвищиться, але якщо це підвищення було вироблено досить швидко, то манометрический стовпчик не відразу займе остаточне положення, так як стиснення повітря було адиабатическим і, отже, його температура підвищиться. Остаточна різницю рівнів в манометрі встановиться тільки тоді, коли температура повітря всередині балона зрівняється, завдяки теплопровідності стінок, з температурою навколишнього повітря.
Позначимо через термодинамічну температуру навколишнього повітря і через - тиск газу всередині судини, відповідне показання манометра. Очевидно, тиск, що встановився в посудині, дорівнюватиме
де - приріст тиску, що сталося фактично за рахунок збільшення маси повітря в посудині в порівнянні з масою повітря в початковому стані.
Ці два параметри і характеризують стан газу, яке ми назвемо першим станом газу.
При швидкому відкриванні крана повітря з посудини почне виходити в атмосферу, тобто розширюватися до тих пір, поки тиск в посудині не міг зрівняється з атмосферним. Це розширення відбувається досить швидко і система не встигає обмінятися теплом з навколишнім середовищем. Отже, повітря розширюється адіабатично, в результаті чого його температура знизиться до деякого значення. Частина, що залишилася в посудині маса повітря буде в змозі, яке характеризується тиском. температурою і об'ємом. яке назвемо другим станом.
Якщо після цього знову закрити кран, то знаходиться в посудині повітря масою при тиску і температурі почне ізохорно нагріватися за рахунок теплообміну з навколишнім середовищем до тих пір, поки температура всередині і поза судини не стане однаковою. При цьому тиск зазначеної маси повітря збільшиться на деяку величину і стане рівним
У підсумку ми маємо третій стан повітря з параметрами. . і.
Адіабатичний перехід повітря з першого стану в друге описується законом Пуассона (9), яке, використовуючи рівняння стану (2), можна записати у вигляді
7.5. Контрольні питання
1. Що називають питомою (молярної) теплоємністю речовини?
2. Отримайте взаємозв'язок між питомою і молярної теплоємності ідеального газу, користуючись першим початком термодинаміки.
3. Що називають числом ступенів свободи молекули? Чому дорівнює число ступенів свободи для одноатомного, двухатомного, трехатомного газу?
5. Що таке коефіцієнт Пуассона? Як пояснити, що його значення для будь-якого газу більше одиниці? Чому дорівнює коефіцієнт Пуассона для повітря?
6. Які процеси відбуваються з повітрям в даній роботі? Яким законам вони підпорядковуються?
7. Який процес називають адіабатичним? Отримайте рівняння цього процесу для ідеального газу, користуючись першим законом термодинаміки і рівнянням стану.
8. Зобразіть в координатах адіабатичний і ізотермічний процеси.
9. Що стверджує закон равнораспределенія енергії за ступенями свободи молекул? Які межі його застосовності?