Сторінка 51 з 80
Як правило, пухлинні віруси можуть не тільки «проїдати» дірки в шарі відповідних клітин, але і порушити строгий порядок в культурі тканини.
Багато клітини, вирощувані в культурі тканини, підкоряються загальним порядком: вони діляться тільки до тих пір, поки є місце. Якщо утворюється товстий шар клітин, поділу припиняються: тісні контакти між клітинами запобігають нові мітози (феномен «контактного гальмування»).
Клітини, інфіковані пухлинними вірусами, іноді відмовляються підкорятися цим правилам: вони продовжують рости, навіть «наповзаючи» на сусідів і утворюючи нерівномірні шари. Такі морфологічні ознаки вже самі по собі в якійсь мірі нагадують невеликі пухлини. Більш того, по суті доведено, що проблеми, що накопичуються один на одного клітини суть не що інше, як справжні пухлинні клітини. Якщо їх імплантувати невластивому реципієнту (тварині того ж інбредних штаму, від якого спочатку були взяті клітини для даної культури), то у тварини утворюються справжні пухлини.
Іншими словами, «безладно зростаючі клітини» під впливом пухлинного вірусу перетворюються в пухлинні клітини (фіг. 40).
Ознаки трансформованої клітини
- Посилений темп зростання.
- Можливість необмеженого пассірованія в культурі тканини ( «постійна лінія»).
- Втрата контактного гальмування ( «нагромадження клітин» і «безладний зростання»).
- Освіта вирусспецифических антигенів.
- Освіта пухлин з імунологічної сумісністю.
Трансформація і загибель клітини
Трансформація і загибель клітин можуть супроводжувати один одного: якщо клітини ембріона миші інфікувати вірусом поліоми, то, крім просвітлінь в клітинному шарі, можна спостерігати і характерні безладні нагромадження клітин.
Але загибель клітин і трансформація - процеси настільки різні, що напрошується припущення про наявність двох різних типів вірусів. В такому випадку віруси, виділені з ділянок окремих просвітлінь, здавалося б, повинні були викликати тільки просвітлення, але не трансформацію.
Однак досвід показав зворотне: трансформація і руйнування клітин супроводжували один одного навіть у тих випадках, коли віріони були виділені з одного просвітлення. Отже, один і той же вірус може викликати як продуктивну інфекцію, так і трансформацію.
Клітини можуть робити вибір між продукуванням вірусу і трансформацією
Рішення про те, чи прийме клітина участь в продукуванні вірусів з подальшим своїм розпадом або піддасться трансформації і стане пухлинної, в значній мірі залежить від клітини-мішені. Відомі лінії клітин, які переважно лизируются вірусом SV- 40, і такі, які переважно піддаються трансформації (див. Фіг. 40).
Відіграють роль не тільки спадкові властивості клітини, але і її фізіологічний стан. Вірусної трансформації набагато легше піддаються зростаючі, діляться клітини, ніж клітини покояться (так звані стаціонарні клітини). Вірусна ДНК, ймовірно, легше вбудовується в ДНК клітини в процесі її реплікації. Це означає, що важлива не тільки лінія клітин, але і фаза клітинного циклу.
Зрозуміло, клітини не цілком вільні у «ухваленні рішення»: якщо обробити клітини надмірною кількістю SV-40, який зазвичай викликає лише трансформацію (множинна інфекція), то може статися «заборонене» продукування вірусу.
В одній клітці може бути вироблено кілька тисяч вірусних частинок, а трансформовані клітини, навпаки, як би зовсім не містять вірусу.
«Масковані» віруси
Власне кажучи, в тому, що трансформовані клітини більше не містять вірусу, немає нічого дивного. Цей факт узгоджується з колишніми даними про те, що в пухлинах, індукованих вірусами, вірус часто не вдається спостерігати. (Так, швидко зростаюча папілома Шоупа у домашніх кроликів більш не містить вірусу Шоупа.)
Тут можливі два пояснення:
- Віруси дійсно викликають трансформацію, але сформувалася пухлинної клітці вони більше не потрібні. Отже, віруси можуть не тільки ховатися, а й справді зникати.
- Але, як з'ясувалося, хоча віруси і можуть, очевидно, ховатися, вони все ж не втрачаються: вони впроваджуються в клітину і живуть в ній в «замаскованій» формі.
Класичною моделлю таких «маскованих» вірусів є бактеріофаги. Фаги - це віруси, які розмножуються в бактеріях і лизируют клітини бактерій. Однак розмноження і лізис настають не завжди. Іноді спостерігається так звана «німа інфекція» 1. при якій фаг проникає в клітину, але не руйнує її. Потомство таких інфікованих бактеріальних клітин здається здоровим, проте вони можуть раптово почати бурхливе продукування фагових частинок і руйнуються.
* У вітчизняній медичній літературі прийнято термін «дрімаючі інфекція». - Прим. ред.
Різні чинники визначають такий відстрочений вибух: ультрафіолетове опромінення, рентгенівське опромінення, перекису, різні барвники і канцерогени.
В латентно-інфікованих бактеріальних клітинах вірус не виявляється, однак після лізису він раптово знову з'являється в достатку. У таких клітинах він як би впадав в сплячку, але тим не менш брав участь у всіх клітинних діленнях і, таким чином, поводився подібно гену.
«Союз» бактерії і фага можна уподібнити «шлюбу», який в один прекрасний момент розпадається під впливом зовнішніх впливів: вірусний геном «приймає управління» і починає займатися виключно розмноженням фага. Господар поставляє все складальні конвеєрні лінії і енергію на службу фагу і врешті-решт гине.
ДНК пухлинних вірусів віддалено нагадує такі латентні фаги. Вірус поліоми і SV-40 також не зникають повністю з трансформованих клітин. Навіть в видно вільних від вірусу пухлинних клітинах є «свіжі сліди», які свідчать про присутність вірусу.
Слідами «маскованих» вірусів: вірусснеціфіческіе антигени
Перші сліди вдалося виявити завдяки імунологічних методів: в клітинах, трансформованих вірусом, містяться антигени, відсутні в нормальних клітинах. Вони різняться в залежності від вірусу, що викликав трансформацію. Так були виявлені антигени, специфічні по відношенню до вірусу поліоми або до SV-40
Вірусснеціфіческіе антигени були відкриті в ядрі трансформованих клітин і названі Т-антигенами (пухлинними антигенами). У хом'яків з пухлинами, індукованими вірусом поліоми, виробляються антитіла проти специфічних по відношенню до поліоми ядерних антигенів. Якщо їх помітити флуоресцирующим барвником, то антигени можна буде спостерігати під мікроскопом: клітини з Т-антигеном після інкубації з міченими антитілами характеризуються яскравим флуоресцирующим ядром, тоді як клітини без антигенів залишаються темними.
Т-антиген не є компонентом вірусу, таким, як, наприклад, білок його оболонки. Функції його досі не з'ясовані. Недавні дослідження показали, що клітини пухлин, індукованих вірусами, не завжди містять Т-антигени. Отже, вони не обов'язкові для трансформації.
Вірусспеціфіческой антигени можуть також локалізуватися на клітинній мембрані трансформованих клітин (антигени реакції відторгнення при трансплантації - АРОТ). Вони відповідальні за відторгнення пересаджених вірусних пухлин. Як ми бачили в попередньому розділі, можливе вироблення, правда обмеженого, імунітету проти пересаджених вірусних пухлин. Якщо спробувати вдруге ввести ту ж вірусну пухлина резистентності тварини, то клітини пересаджують пухлини не щепитимуться (за умови, - що вводиться не дуже багато клітин).
Локалізація таких трансплантаційних антигенів на клітинній мембрані добре вивчена.
- Загальноприйнято, що Трансплантаційні антигени розташовуються на поверхні клітини. Лише в цьому випадку можлива пряма реакція між пересадженими клітинами і клітинами імунної захисту.
- Імунні реакції можуть бути викликані не тільки інтактними трансформованими клітинами, але і їх «тінями». «Тінями» клітин називають їх оболонки з досить хорошою сохранностио поверхневих структур, одержувані при набуханні клітин і їх розриві в гипотоническом сольовому розчині.
Антигенні речовини самих вірусних частинок (білкові субодиниці) не ідентичні АРОТ-антигенів. АРОТ-антигени виробляються трансформованої клітиною відповідно до вказівок, що виходять від вірусного генома. Різні типи клітин виробляють одні й ті ж антигени при трансформації одним і тим же вірусом (див. Стор. 167).
Крім поверхневих антигенів, які виявляються при трансплантації, є також антигени, які вдається виявити безпосередньо in vitro (проба на аглютинацію, антитіла, мічені флуоресцеїном). Такі антигени часто називають S-антигенами.
Розглянемо тепер біологічне значення трансплантаційних антигенів. Трансплантація і відторгнення трансплантата є штучно створеною ситуацією, так би мовити, біологічно винятковим випадком, можливим лише в умовах експерименту. І все ж є достовірні свідчення про те, що вірус-специфічних речовини типу трансплантаційних антигенів відіграють певну роль і в «нормальному» розвитку вірусної пухлини.
Змінені антигенні структури пухлинної клітини попереджають систему імунного захисту господаря. Трансформовані клітини розглядаються як «нові», «чужі», і механізми захисту приводяться в дію. Під впливом вірусу частину власних клітин організму стає «чужий», що знаходить відображення в наступному:
- Клітини, що стали чужими, випадають з системи цілісного організму: переставши підкорятися правилам «суспільства», вони стають пухлинними.
- Але саме через те, що клітини стали чужими, господар отримує можливість здобути їх як чужорідний матеріал.
Відповідно до цієї теорії, S-антигени знаходяться в центрі вірусного онкогенезу: чим більше клітини стають чужими завдяки цим антигенів, тим легше їм ухилятися від нормальних регуляторних сигналів. Однак це ж обставина послаблює їхні позиції по відношенню до системи імунного захисту організму. Взаємозв'язок очевидна, хоча і не має поки строгого експериментального підтвердження.
Вірусспеціфіческой антигени не є єдиними «відбитками пальців» пухлинних вірусів в трансформованих клітинах. Особливо видають присутність вірусу вірусспеціфіческой РНК.
Слідами «маскованих» пухлинних ДНК-вірусів: вірусспеціфіческой РНК
Трансформовані пухлинні клітини виробляють вірусспеціфіческой інформаційну РНК. Виявлення цієї РНК здійснюється шляхом так званої гібридизації ДНК з РНК. Тут слід зробити невеличкий екскурс в теорію, щоб зрозуміти суть цього методу.
Інформаційна РНК отримує генетичну інформацію від ДНК, і послідовність нуклеотидів в ній визначається нуклеотидної послідовністю ДНК.
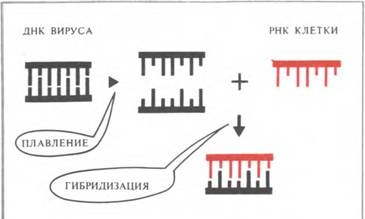
МОЛЕКУЛЯРНИЙ ПРИНЦИП гібридизації
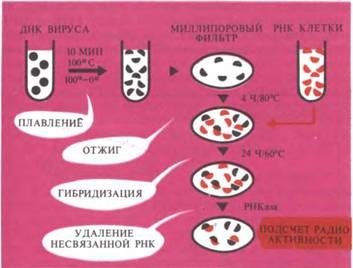
ТЕХНІКА гібридизації
Отже, інформаційна РНК і ДНК комплементарні один до одного. Правда, окрема молекула інформаційної РНК являє собою «зліпок» лише з короткого відрізка нуклеотидной ланцюжка ДНК. Якщо ДНК і інформаційну РНК від однієї і тієї ж клітини змішати один з одним, то відповідні нуклеотидні ланцюжки двох нуклеїнових кислот знову об'єднаються попарно. Такі ДНК - РНК-комплекси можуть бути розділені і кількісно охарактеризовані. Якщо ж ДНК змішати з інформаційної РНК з різних джерел, то, як правило, буде спостерігатися лише слабка асоціація (фіг. 41).
Точно так же інформація, укладена в вірусної ДНК, перш за все переписується на молекулу РНК, і ця вірусспеціфіческой інформаційна РНК також може бути гібридизувати з вірусною ДНК. Отже, вірусспеціфіческой інформаційна РНК - це РНК, гібридизувати з вірусною ДНК.
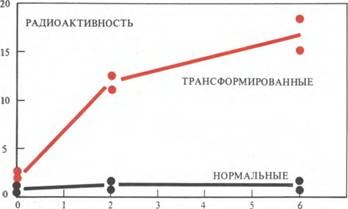
У дослідах по гібридизації вірусної ДНК з РНК з незаражених нормальних клітин спаровування не спостерігається. І навпаки, якщо виділити РНК з трансформованих клітин і гібридизувати її з вірусною ДНК, то станеться часткова гібридизація між РНК і ДНК. І хоча спаровування підлягає лише дуже невелика частина загальної РНК трансформованої клітини, її зв'язування з вірусною ДНК визначається з високим ступенем надійності (фіг. 42). Це означає, що вірус-специфічних РНК присутня навіть в трансформованих клітинах, хоча самі віріони в них і не виявляються.
Отримані нові відомості є прямою вказівкою на присутність вірусної ДНК, інакше звідки б клітці взяти інформацію для синтезу цієї РНК?
Вірусна ДНК зберігається в трансформованих клітинах
Про наявність в трансформованих клітинах вірусної ДНК свідчить не тільки виявлення вирусспецифической інформаційної РНК; вірусна ДНК була виявлена і прямими методами.
Докази знову грунтуються на методі з'єднання комплементарних ДНК і РНК. Для цього перш за все необхідно отримати вірусну інформаційну РНК, яка використовується як індикатор вірусної ДНК. Цю РНК можна виділити з суміші інформаційних РНК клітини і вірусу, екстрагованих з інформаційних клітин.
Вестфаль вибрав більш витончений шлях: він синтезував інформаційну РНК SV-40. З цією метою він використовував фермент, Полімеризується рибонуклеотиди до полинуклеотидов (РНК) в точній відповідності з так званої «затравочной» ДНК (ДНК-залежна РНК-полімераза). Послідовність нуклеотидів в такий синтетичної РНК виявляється комплементарної послідовності нуклеотидів, використовуваної затравочной ДНК. Якщо ж в якості «затравки» взяти вірусну ДНК, то можна отримати вірусснеціфіческую РНК.
Така синтетична вірусна інформаційна РНК може бути пов'язана з ДНК клітини, трансформованої пухлинними вірусами; з ДНК нормальних клітин зв'язування не відбувається. З цього випливає, що вірусна ДНК постійно присутня в трансформованому клітці. Таким чином, «маскуватися» вірус не що інше, як «гола вірусна ДНК», або «ядро» вірусної частинки. За попередніми підрахунками є 10-50 вірусних копій на клітину. Всі копії локалізуються в ядрі клітини. Якщо згадати про те, що трансформація відбувається успішніше в ті фази клітинного циклу, коли здійснюється синтез
ДНК, то легко погодитися з припущенням про те, що вірусна ДНК вбудовується в ДНК клітини-господаря. При кожному діленні клітини вірусна ДНК ділиться разом з усією ДНК клітини. В іншому випадку вона повинна була б поступово зникнути і її не можна було б виявити.
В повному розумінні слова метод гібридизації нуклеїнових кислот доводить лише те, що принаймні частина вірусної ДНК зберігається в трансформованому клітці. Нові методи дозволяють зробити ширші узагальнення: доведено, що в трансформованому клітці зберігається весь геном вірусу SV-40.
Демаскування пухлинного вірусу: злиття клітин викликає продукування вірусу
В останні роки вдалося добитися злиття клітин ссавців (Ефруссі, Харріс). При цьому утворюються клітини, що мають спочатку два або більше ядра; через деякий час формується одне ядро, яке містить хромосоми обох батьківських клітин.
У природі таке злиття клітин вищих організмів є рідкістю. Його можливо спостерігати лише в особливих випадках, коли «суперклетка», що виникла в результаті злиття, має в порівнянні зі звичайними батьківськими клітинами перевага у відборі. Однак такого злиття можна домогтися штучним шляхом, обробивши клітини вірусом Сендай. Цей вірус, названий на честь міста в Японії і зазвичай викликає захворювання типу грипу, здатний викликати також злиття клітин в культурах: мабуть, він містить «фактор злиття», який специфічно впливає на клітинні стінки. Злиття клітин може бути викликано і «мертвим» (інактивованих ультрафіолетовим опроміненням) вірусом Сендай. В останньому випадку усувається необхідність в «зупинці» продукування вірусу після злиття клітин.
Використовуючи описаний метод, Копровскі зумів здійснити злиття цілої серії трансформованих клітин (очевидно, без вірусу) з нормальними клітинами, в яких можливо продукування вірусу. Продукування вірусу починалося в освічених таким чином багатоядерних гібридах клітин. Нормальна «продуктивна» клітина перетворює «маскувати» вірус трансформованої клітини в продуктивний вірус (див. Фіг. 40).
В ході проведених експериментів з'ясувалося, що:
1) в трансформованих клітинах може зберігатися весь геном вірусу, оскільки злиття клітин викликає утворення повних вірусних частинок;
2) по-видимому, в трансформованому клітці не відбувається якихось реакцій, необхідних для продукування повних вірусних частинок. У трансформованому клітці немає синтезу білкової оболонки і відповідно масового виробництва вірусної ДНК. Тому, як можна вважати, трансформована клітина (принаймні в цьому відношенні) тримає вірус під контролем.