Сировина, напівфабрикати і готову продукцію бродильних виробництв мають кислу реакцію; тільки меляса зазвичай має слаболужну реакцію. Кислотність прийнято виражати в кубічних сантиметрах нормального розчину лугу, що йде на нейтралізацію кислот в 100 см 3 або 100 г продукту.
У спиртовому виробництві кислотність виражають в градусах кислотності, тобто числом кубічних сантиметрів нормального розчину лугу, необхідне для нейтралізації 20 см 3 розчину; при цьому 1 см 3 нормального розчину лугу, витрачений для нейтралізації 20 см 3 розчину, відповідає 1 градусу кислотності. Кислотність пива висловлюють в кубічних сантиметрах нормального розчину лугу, що йдуть для нейтралізації 100 см3 пива. Загальну кислотність визначають титруванням в присутності індикатора. У технохимічеському контролі бродильних виробництв в якості індикаторів застосовують метилоранж, метілкрасний, бромтимоловий синій, фенолфталеїн, лакмус. Характеристика цих індикаторів наведена нижче.
Таблиця 6 - Характеристика індикаторів
Зона переходу забарвлення (рН)
При визначенні кислотності світлих і прозорих продуктів беруть певну кількість досліджуваного розчину, додають кілька крапель індикатора і титрують нормальним або 0,1 н розчином лугу до зміни забарвлення. Для визначення кислотності темних продуктів (Осахаренний маса, зріла бражка і інші) певний обсяг досліджуваного розчину титрують лугом, в процесі титрування час від часу беруть краплю досліджуваного розчину на порцелянову платівку, додають індикатор, перемішують скляною паличкою і спостерігають за забарвленням. За кількістю витраченого на титрування лугу знаходять загальну кислотність.
Апаратура і реактиви. Лабораторна млин; сито № 08; конічні колби на 100-150 см 3; скляні пластинки розміром 20х20; 0,1 н розчин NаОН; 1% розчин фенолфталеїну; червоний фенолфталеин (до 20 см 3 дистильованої води додають 10 крапель 1% фенолфталеїну і 4 краплі 0,1 н NаОН, розчин готується щодня).
Визначення кислотності по бовтанці (ГОСТ 10844) / 8 /
Метод заснований на титруванні суспензії розмеленого зерна 0,1 н розчином лугу в присутності фенолфталеїну. При титруванні луг пов'язується не тільки перейшли в розчин кислими речовинами, а й речовинами частинок борошна, внаслідок чого кислотність по бовтанці виходить дещо завищеною. Результати в великій мірі залежать від тонкості помелу, тому його обов'язково перевіряють.
Хід визначення. З середнього зразка зерна відбирають 50 г ячменю, очищають від смітної домішки (зіпсовані зерна залишають) і розмелюють на млині так, щоб все размолотое зерно проходило при просіюванні через металлотканое сито № 08. Борошно поміщають на скляну пластинку, перемішують, розподіляють рівним шаром так, щоб після прідавліванія другою платівкою шар борошна вийшов не товщі 3-4 мм. Видаливши верхнє скло, відбирають не менше ніж з 10 місць 5 г борошна і зважують з точністю до ± 0,01 г. Наважку переносять в суху конічну колбу на 100-150 см 3. додають 50 см 3 дистильованої води (спочатку невеликими порціями до повного змочування), добре перемішують до зникнення грудочок, після чого змивають зі стінок частки борошна водою. У бовтанку додають 5 крапель 1% розчину фенолфталеїну і титрують при збовтуванні 0,1 н розчином лугу до появи виразного рожевого забарвлення, не зникає при стоянні протягом 1 хвилини.
Якщо бовтанка має інтенсивне забарвлення, то готують ще одну бовтанку з цієї проби ячменю і при титруванні порівнюють зміна кольору з початковим кольором бовтанки.
Кислотність (в градусах) розраховують за формулою
де а - обсяг 0,1 н. розчину лугу, що пішов на титрування, см3;
К - поправочний коефіцієнт до титру 0,1 н розчину лугу;
н - навішування борошна, г;
100 - коефіцієнт перерахунку на 100 г ячменю;
10 - коефіцієнт перерахунку 0,1 н розчину лугу в 1 н розчин.
За фактичну кислотність приймають середнє арифметичне з двох паралельних визначень, розбіжність між якими не повинно перевищувати (0,20.
Визначення титруемой кислотності в суслі та пиві
Пиво перед визначенням звільняють від діоксиду вуглецю, збовтуванням або нагріванням протягом 30 хвилин при 400С, потім охолоджують до температури 200 ° С.
Хід визначення. У конічну колбу на 150-200 мл піпеткою відмірюють 50 мл сусла або пива і титрують 0,1 н розчином лугу до тих пір, поки 4 краплі сусла (пива), поміщені на порцелянову платівку, при змішуванні з 2 краплями червоного фенолфталеїну не перестануть його знебарвлювати .
Кислотність х (в мл 1 н розчину лугу на 100 мл рідини) розраховують за формулою
# 19; EMBED Equation.3 # 20; # 21 ;, (14)
де а - обсяг 0,1 н розчину лугу, що пішов на титрування, см3;
б - обсяг сусла (пива), взятий на титрування, мл;
10 - коефіцієнт перерахунку 0,1 н. розчину лугу в 1 н розчин.
Приклад. На титрування 50 мл сусла витрачено 10,2 мл 0,1 н розчину лугу. Кислотність сусла х = (10,2 (100). (50 (10) = 2,04 мл 1 н розчину лугу на 100 мл сусла.
Електрометричне або потенціометричні титрування засноване на різкій зміні потенціалу індикаторного електрода поблизу точки еквівалентності (точки кінця титрування (ТКТ) при додаванні до розчину невеликої кількості титрів реагенту. При реакціях нейтралізації індикаторними можуть служити різні електроди (сурм'яний, скляний і ін.), Потенціали яких залежать від рН. як електроди порівняння найбільш часто використовують каломельний і хлорсрібний електроди. Потенціометричне титрування виконують, использ уя спеціальні прилади (рН-метри, тітратори, потенціометри та ін.). ТКТ можна визначати, титруючи розчин або до заданого значення рН, або до моменту, коли стрілка гальванометра перестає відхилятися або змінює напрямок відхилення. Зазвичай застосовують перший спосіб, використовуючи рН метри.
Значення рН, прийнятого за ТКТ, вибирають в залежності від рН переходу забарвлення індикатора, що використовується при звичайному титруванні. Якщо при звичайному титруванні застосовується фенолфталеин, то титрування закінчують при рН 8,5, бромтимоловий синій - при рН 7,3, лакмус - при 7,0, метиловий червоний - при рН 6,3 і т.д.
При електрометричного титрування з однаковою точністю можна визначати кислотність як безбарвних, так і Темна розчинів.
Хід визначення. У хімічний стаканчик відмірюють піпеткою 25 мл пива або сусла, після чого його титрують при безперервно працюючій мішалці 0,1 н розчином лугу, спостерігаючи за переміщенням стрілки гальванометра. На початку титрування розчин лугу додають невеликими порціями, а в міру наближення до значення рН 8,5 - по краплях. Після закінчення титрування знімають відлік по шкалі бюретки. Кислотність розраховують за попередньою формулою.
Визначення активної кислотності (рН) в суслі та пиві
Електрометричний метод визначення рН
Метод заснований на тому, що при зануренні електроду в розчин відбувається обмін іонів між електродом і розчином, внаслідок чого на електроді виникає потенціал, величина якого залежить від концентрації водневих іонів в розчині. Його можна виміряти, якщо скласти гальванічний елемент з електрода, потенціал якого хочуть виміряти (індикаторний електрод), і допоміжного електрода з відомим потенціалом (електрод порівняння).
В даний час в якості індикаторного застосовують скляний і сурм'яний електроди, а в якості електродів порівняння - хлорсеребряного і каломельний.
Визначення рН за допомогою рН-метра ЛПУ-0,1
Принцип роботи приладу заснований на вимірюванні ЕРС гальванічного елемента, складеного зі скляного (індикаторного) і хлорсрібного (допоміжного) електродів. Шкала приладу градуйована в одиницях рН і мілівольтах. Межі вимірювання рН від 2 до 14. Для підвищення точності вимірювання прилад має чотири діапазони з вузькими інтервалами значень рН. У цих інтервалах похибка приладу не перевищує (1%; в інтервалі рН 2-14 - не вище (2,5% від діапазону вимірювань.
Прилад (рисунок 11) складається з гальванічного елемента (датчика) і вимірювача. Всі частини датчика зібрані на штативі. На верхньому кінці штатива укріплений проточний допоміжний електрод, поміщений в поліетиленовий посудину. У нижній частині штатива є рухливий столик для установки склянки з досліджуваним розчином і електродами. Електричний контакт між двома електродами здійснюється через стовпчик насиченого розчину хлориду калію, що випливає з поліетиленового судини по гумовій трубці і скляному наконечника в досліджуваний розчин. Розчин хлориду калію повільно (20 мл на добу) випливає через пористу перегородку наконечника, запобігаючи таким чином проникнення сторонніх іонів з досліджуваного розчину в посудину з допоміжним електродом. Необхідно стежити, щоб в трубці електрода не було бульбашок повітря, що порушують контакт. Скляний електрод і наконечник кріпляться до кронштейну зажимами. У комплекті датчика є електролітичний контакт для вимірювань рН в розчинах об'ємом до 1 мл.
На панелі вимірювача (рисунок 12) знаходиться шкала, що показує 5 значень рН: від 2 до 4, від 2 до 6, від 6 до 10, від 10 до 14 і від 2 до 14, а також шкала для вимірювання ЕРС. На панель виведені також всі ручки управління приладом.
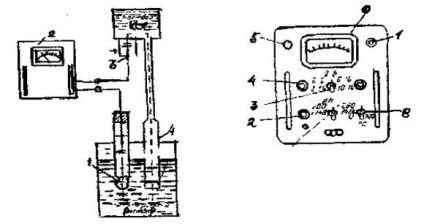
Малюнок 11 - Схема РН-метри ЛПУ-01
2-панель вимірювального приладу;
3-проточний допоміжний електрод;
4-наконечник з пористої перегородкою
Малюнок 12 - Панель рН-метра ЛПУ-01 1-рукоятка перемикання «Види робіт»; 2-гніздо підключення датчика; 3-перемикач меж вимірювань; 4-ручка настройки по буферного розчину; 5 - контрольна лампочка; 6-шкала; 7 - тумблер включення; 8-рукоятка компенсатора температури
Після прогріву приладу приступають до його налаштуванні за стандартними буферним розчинам з відомим значенням рН.
Буферні розчини готують із спеціальних фіксоналов. Для настройки беруть буферний розчин, рН якого близький до передбачуваного рН досліджуваного розчину. Буферний розчин наливають в стакан на 200 мл, столик на штативі відводять вліво, стакан підставляють під електроди, повертають столик і опускають на нього склянку. Столик встановлюють на такій висоті, щоб електроди були занурені в розчин на глибину 2-4 см, перемикач меж вимірювань ставлять проти потрібного діапазону вимірювань і через 0,5-1 хвилину ручкою настройки по буферного розчину стрілку на шкалі підводять до поділу, відповідного значенням рН буферного розчину.
Вимірювання рН досліджуваного розчину проводиться в послідовності, прийнятої під час налаштування приладу. Якщо рН розчину абсолютно невідомий, то спочатку роблять орієнтовний визначення, ставлячи перемикач меж вимірювань в положення «2-14» і знімаючи відлік за шкалою, градуйованою в одиницях рН від 2 до 14. Потім, не змінюючи розчину, перемикач встановлюють на позначку знайденого діапазону рН і відлік знімають за відповідною шкалою.
У перервах роботи електроди тримають в дистильованої воді, так як при висиханні змінюється їх характеристика. При появі плівок на електродах їх промивають органічними розчинниками, розчинами кислот і лугів, а потім дистильованою водою.
Похибка приладу за стандартними буферним розчину не вище 0,02 рН, а чутливість не нижче 0,01 рН.
Перевірку нового приладу або нового скляного електрода проводять по буферним розчинам в перші кілька днів щодня, а в подальшому - раз в тиждень.
У виробничому контролі прилади використовують для визначення не тільки рН, а й титруемой кислотності методом електрометричного титрування.
Перед початком роботи електроди ретельно промивають дистильованою водою і висушують фільтрувальним папером. До гнізда 2 за допомогою штекера підключають датчик, прилад включають в мережу, тумблер 7 ставлять в положення «Включено» (при цьому загоряється контрольна лампочка) і прилад прогрівають 30 хвилин. Рукоятку перемикання «Види робіт» встановлюють в положення «рН», а рукоятку компенсатора температури - на потрібне значення температури. Вимірювання проводять при температурі 20-30 0 С, так як при цій температурі відхилення в значеннях рН лежать в межах похибки приладу.
Активна кислотність в солоді дуже впливає на ферментативні процеси при затирання і рН в заторі зазвичай становить 5,5-5,6.
рН сусла так само, як і затору, обумовлюється іонами водню, що переходить із сировини, а також хімічним взаємодією катіонів та аніонів води і сусла.
У охмеленого сусла активна кислотність знаходиться в межах 5,3-5,5.