Стійкість комплексів залежить від природи металу і ліганду. Відносно іона металу важливими є наступні фактори: розмір і заряд, іонний потенціал, енергія стабілізації кристалічним полем, освіту датівная я-зв'язку.
Слід привести таблицю, яка ілюструє вплив заряду центрального іона на стійкість комплексів (табл. IX-4). Для зіставлення обрані центральні іони з приблизно однаковими радіусами (г *) і однієї і тієї ж електронної структурою [11].
Таблиця IX-4. Логарифм константи стійкості комплексних іонів в залежності від заряду центрального іона
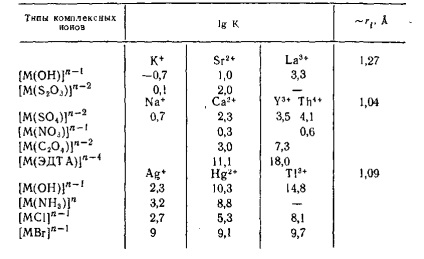
Якщо визначити іонний потенціал як відношення заряду катіона до його радіусу в кристалі, то стійкість комплексів з невеликими або високозарядних лигандами і полідентатними лигандами збільшується в міру зростання іонного потенціалу [6, 12]:
для іонів з одним і тим же зарядом Li> Na> До >> Rb> Cs; Mg> Са> Sr> Ва> Ra; Al> Sc> Y >> La;
для іонів з різними зарядами, але приблизно однакового розміру Th> Y> Са> Na; La> Sr> К.
Однак, як видно з табл. IX-5, вплив заряду іона металу на стійкість істотніше, ніж вплив іонного радіуса [6].
Таблиця IX-S. Вплив відносини заряд / радіус на стійкість гідроксокомплексів | М (ОН)] (п-
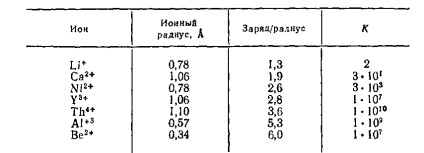
Стійкість комплексів, утворених іонами перехідних металів, залежить не тільки від іонного потенціалу, а й від таких факторів, як енергія стабілізації кристалічним полем [6] (рис. IX-3), наявність ва-
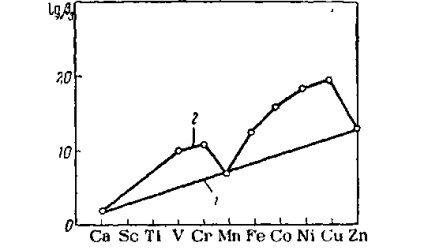
Мал. IX-3. Залежність логарифма константи стійкості комплексів двовалентних перехідних металів першого ряду з етилен-діамін від атомного номера металу
Стійкість комплексів для дво- і трехзарядних
Розглядаючи роль лігайда в збільшенні стійкості комплексів, важливо відзначити наступні фактори (див. Гл. X): основність, дентатність лиганда, хелатний ефект, стерические чинники.