Всі речовини складаються з рухомих і взаємодіючих між собою атомів і молекул.
Прості речовини складаються з однакових атомів, складні - з атомів різних хімічних елементів. Атом - найменша частина хімічного елемента, що є носієм його властивостей.
У центрі атома знаходиться позитивно заряджене ядро, навколо якого рухаються негативно заряджені електрони, що притягуються до позитивно зарядженого ядра силами електромагнітної взаємодії.
Головною характеристикою хімічного елемента є заряд ядра атома.
Z - Зарядове число ядра, яка дорівнює кількості протонів в ядрі, збігається з порядковим номером хімічного елемента в періодичній системі хімічних елементів Д. І. Менделєєва.
Атом електронейтрален. позитивний заряд (+ Ze) ядра компенсується негативним зарядом (-Ze) електронів.
Крім протонів, в ядрі атомів містяться нейтрони, пов'язані з протонами сильним взаємодією. Загальна назва протонів і нейтронів, що входять до складу ядра, - нуклони.
Масове число А дорівнює числу нуклонів в ядрі (сумарне число протонів Z і нейтронів N):
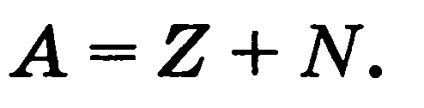
Ізотоп - різновид одного і того ж хімічного елемента, атом якого містить однакове число протонів в ядрі і різну кількість нейтронів.
В умовному позначенні ізотопу хімічного елемента вказуються масове число А і Зарядове число Z:
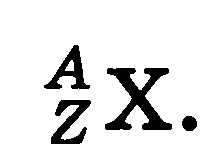
Маса атома менше сумарної маси частинок, що входять до його складу.
Дефект маси - різниця сумарної маси окремих частинок, які входять до складу атома (ядра), і повної маси атома (ядра):
Дефект маси обумовлюється виділенням енергії ДЕ при утворенні атома:
Атомна одиниця маси (а.е.м.) - середня маса нуклона в атомі вуглецю 12С 6 С.
Атомна одиниця маси дорівнює 1/12 маси атома вуглецю 12С 6 С.
Відносна маса атома Мr - число атомних одиниць маси, що містяться в масі атома:
Моль - кількість речовини, маса якого, виражена в грамах, чисельно дорівнює відносній масі атома.
Молярна маса - маса одного моля.
Одиниця молярної маси - кілограм на моль (кг / моль). Постійна Авогадро - число атомів (або молекул) в одному молі будь-якої речовини:
Молярна маса речовини
Існує чотири агрегатних стани (або фази) речовини: тверде, рідке, газоподібне, полум'яне.
Фазовий перехід - перехід системи з одного агрегатного стану в інше. При фазовому пере
Під час стрибкоподібно змінюється якась фізична величина (наприклад, щільність, внутрішня енергія) або симетрія системи. Речовина знаходиться в твердому стані, якщо середня потенційна енергія тяжіння молекул багато більше їх середньої кінетичної енергії.
Молекули в твердому тілі розташовуються впорядковано.
Рідкий стан утворюється, якщо середня потенційна енергія тяжіння молекул порівнянна з їх середньої кінетичної енергією. Впорядковане розташування молекул спостерігається в рідини лише в межах декількох сусідніх молекулярних шарів.
Речовина знаходиться в газоподібному стані, якщо середня кінетична енергія молекул перевищує середню потенційну енергію їх взаємодії. Молекули газу рухаються хаотично. Умови ідеальності газу:
1) діаметр молекул багато менше середньої відстані між ними;
2) середня кінетична енергія молекул багато більше середньої потенційної енергії їх взаємодії;
3) молекули взаємодіють між собою і зі стінками пружно. Плазма - електронейтральна сукупність нейтральних і заряджених частинок.
Іонізація - процес утворення іонів з атомів.