Сторінка 7 з 18
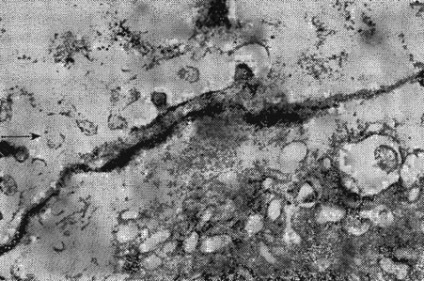
Мал. 8. Ділянка головною клітини, на якому видно формування внутрішньоклітинного канальця (стрілка).
«Змішані» (мікст) клітини зустрічаються в МОР тварин, що знаходяться на більш низьких Рівнях філогенетичного розвитку. Х32 500
Для електронно-мікроскопічного дослідження шматочки тканини МОР фіксували в 2,5% розчині глутаральдегида, приготованому на 0,1 М какоділатном буфері (рН 7,4), який містив 7% полівінілпіролідону. Дофіксаціей проводили 2% розчином 0s04, приготованому на веронал-ацетатному буфері (рН 7,4). Після фіксації тканину укладали в ЕП0Н-812; ультратонкі зрізи, отримані на ультрамікротоме УМЛТП-3, доконтрастіровалі уранілацетатом і свинцем і переглядали в електронному мікроскопі ЕОМ-100 JI. Ультратонкі зрізи готували за методикою, запропонованою І. А. Морозовим (1976, 1977), на рівні генеративної зони, зони росту (150 мкм), тіла залоз (400-500 мкм) найбільш активних в функціональному відношенні клітин і дна залоз. Ультратонкі зрізи готували після того, як залози орієнтувалися в поперечному напрямку.
Для виявлення кислих гликозамингликанов з використанням рутенієвого червоного була застосована гістохімічна методика електронної мікроскопії, запропонована J. Zuft (1965, 1966).
Окислювальні ферменти визначали за допомогою діамінобензідіна за методом К. Hirai (1971).
Для вивчення патогенезу виразкової хвороби (порушення нейротрофических, обмінних процесів, мікроциркуляції в МОР), що обумовлюють зниження клітинної резистентності і характеризують виразкову хворобу, а також для підтвердження єдності захворювання при різної локалізації (дуоденальної і шлункової) виразкового дефекту (досліджували в основному «низькі »виразки або медіогастральние із збереженою кислотоутворюючою функцією) і вираженості процесу (виразкова хвороба з наявністю виразки і передвиразковий стану ка прояви початкової стадії захворювання) у хворих на виразкову хворобу обох локалізацій і передвиразковий станом нами проведено електронно-мікроскопічне дослідження всіх елементів МОР; клітин головних залоз шлунка (мукоїдному, головних, парієтальних, ендокринних), клітин сполучної тканини (лаброцитов, фібробластів, плазмоцитів) і неклітинних елементів, розташованих в сполучнотканинних прошарках (капіляри, нервові закінчення і колагенові волокна). В результаті виявлено наступне: на тлі гіперфункціонального стану клітин головних залоз шлунка, одноклітинних сполучнотканинних залоз розвиваються глибокі порушення в структурах, відповідальних за енергоутворення (мітохондрії) і білковий обмін (рис. 7). Порушення останнього можна характеризувати як дегенеративні зміни в уже синтезованому білковому матеріалі і пригнічення синтезу білка в результаті порушень в белоксінтезірующіх системах на тлі різкої активації навіть в молодих, ще не закінчили свою диференціацію, клітинах лізосомальної системи, що відображають глибину катаболічних процесів.
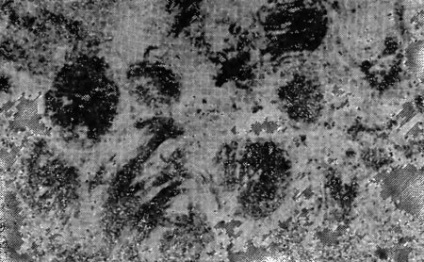
Мал. 9. Ділянка парієтальної клітини після проведення гистохимической реакції для виявлення активності окислювальних ферментів. Цитохром G і цитохромоксидаза розташовуються лише на окремих ділянках мітохондріальних крист. Х34 000

Мал. 10. Формування мукоїдному мас в додаткової клітці внаслідок злиття секреторних гранул. Х20 000
У клітинах МОР, особливо при шлункової локалізації виразки, часто спостерігали порушення диференціації клітин, що приводило до появи клітин змішаного типу: оксінтопептіческіх, несучих риси головних і парієтальних (рис. 8), «мукоідізірованних» головних, що мають гранули змішаного типу - пепсіногенов і мукоїдні, що особливо демонстративно при проведенні гистохимической реакції в електронній мікроскопії з рутенієвого червоним, що виявляє кислі глікозамінглікани, в даному випадку білків слизу додаткових клітин.
Порушення енергообразующую апарату мітохондрій навіть молодих клітин МОР, як головних залоз, так і сполучнотканинних і ендотеліальних, полягали в набуханні, просвітління матриксу, вираженої редукції крист, мієлінової перебудові вмісту мітохондрій, зменшення кількості депозитів, які свідчать про зниження активності окисно-відновних ферментів - ЦХО і цитохрому С (рис. 9). Слід зазначити, що найменш зміненими були мітохондрії, парієтальних клітин при дуоденальної виразці і передвиразковий стан, а в частині парієтальних клітин енергообразующую апарат був не тільки не порушений, а, судячи з ультраструктурі мітохондрій, можна було думати про гіперфункціонального статус клітин. У синтезованому білковому матеріалі спостерігали дегенеративні зміни, які характеризуються появою паракрісталліческіх, ламеллярной і мієлінових фігур всередині секреторних гранул головних і мукоїдному клітин і в місцях скупчення колагенових волокон. Останні були різко змінені: у них губилася поперечнасмугастість і з'являлися зміни, характерні для мукоїдного набухання. У головних і мукоїдному клітинах замість окремих гранул спостерігали суцільні секреторні поля (рис. 10), що, мабуть, перешкоджає виведенню секреторних білків в порожнину шлунка. Про порушення протеїнового обміну свідчить також патологічне випадання волокон колагену в цитоплазмі фібробластів, що знаходяться, як правило, у хворих на виразкову хворобу та з передвиразковий станом в гіперфункціонального стані.
Зміни в белоксінтезірующіх системах клітин СОШ полягали в порушенні освіти мембран гранулярного ретикулума загальновідомим шляхом (А. Полікар, М. Бессі, 1970) з базальної клітинної мембрани: часто на бульбашках, попередників майбутнього гранулярного ретикулума, рибосоми розташовувалися не тільки на зовнішній, а й на внутрішньої поверхні, а самі бульбашки були двошаровими. Усередині таких бульбашок утворювалися шаруваті структури. Ці освіти з елементами навколишнього цитоплазми обмежувалися мембраною, і в результаті виникали аутофагосоми.
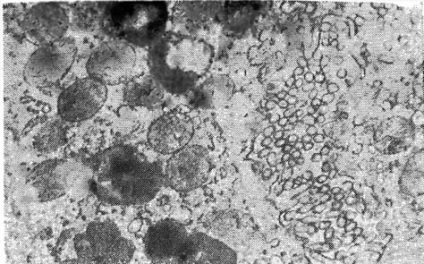
Мал. 11. Вторинні лізосоми і мієлінові фігури в молодої парієтальної клітці при передвиразковий стан. X27 500
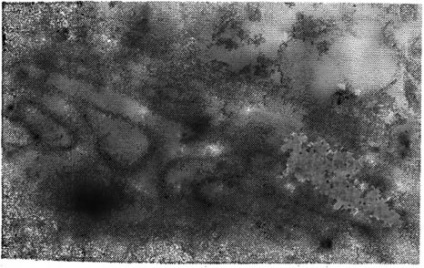
Мал. 12. Зменшення вмісту рутенійположітельного компонента і розпушення рутенійположітельіого шару базальної мембрани і десмосоми. Х82 50б
На деяких ділянках прімембранной шари капілярів відділялися від мембран, місцями спостерігалося скупчення рутенійположітельного речовини в кавеол, розташованих на люмінальной поверхні капілярів. Збільшувалася кількість фібрилярних структур, які не мають рутенійположітельного компонента. Описані порушення можуть зумовити зміни фізико-хімічних властивостей неклеточного речовини, що ведуть до порушення проникності капілярів - Лізор. Існувала пряма залежність між ступенем ураження капілярів і змінами, що розвиваються в клітинах прилеглих залоз. Порушення субклітинному, клітинної та судинної проникності є відображенням порушеною резистентності СО гастродуоденальної зони, що має патогенетичне значення та відповідальної на кінцевому етапі, поряд з кіслотопептіческой агресією, за язвообразование.
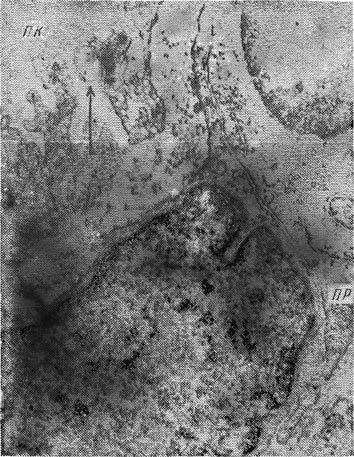
Мал. 14. Ділянка стінки артеріального відділу капіляра.
Видно розпушення прімембранной шару (стрілка). У кавеол (дві стрілки) відбувається накопичення рутенійположітельного речовини.
Багато фібрили базального шару демаскувати. Х85 000
Порушення, виявлені в ультраструктурі нервових закінчень, особливо змішаного типу, дозволили зробити висновок про різку активації холінергічних, на тлі зниження адренергічних процесів в СОШ. Нервові закінчення змішаного типу містили світлі везикули холинергического типу і щільні гранули адренергического типу, причому при виразковій хворобі як шлункової, так і особливо дуоденальної локалізації і передвиразковий стан, на фоні різко збільшеної кількості світлих пухирців зменшувалася кількість щільних гранул в нервових закінченнях (рис. 15, 16). У претерміналях часто спостерігалося розпушення нейрофибрилл. У перицитами - клітинах-посередниках передачі медіатора на ендотелій було помітно ущільнення матриксу цитоплазми, з'являлися мієлінові фігури і осередки сегрегації.
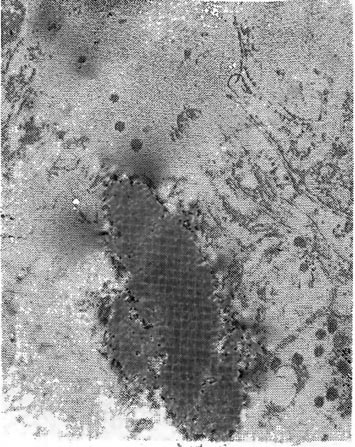
Мал. 15. Нервові закінчення в МОР хворого дуоденальної виразкою, розташовані в прошарку сполучної тканини, що містять в основному світлі пухирці. X 30 000
Дослідження клітин головних залоз шлунка і сполучнотканинних (лаброцитов, фібробластів і плазмоцитів), неклітинних утворень (колагенових волокон), структур, розташованих в сполучної тканини (нервових закінчень, капілярів), дозволили нам зробити загальні висновки, що стосуються патогенезу виразкової хвороби. Незважаючи на те що огрядні (рис. 17), секреторні і ендокринні клітини знаходяться в стані гіперфункції, захворювання протікає на тлі різкої активації катаболічних і гноблення белковосінтетіческой процесів в клітинах, що виникають при порушенні в МОР нервово-трофічної регуляції, мікроциркуляції, гіпоксії, що призводить до різкого зниження її резистентності.
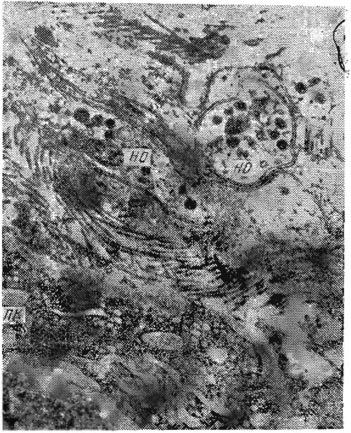
Мал. 16. Нервові закінчення змішаного типу у хворого на хронічний гастрит типу В (передвиразковий стан), в яких превалюють світлі холинергические бульбашки над адренергічними темними гранулами. Х24 000
Ультраструктурномудослідження МОР при дуоденальної, шлункової локалізації виразки і при передвиразковий стан дозволило встановити, незважаючи на істотні відмінності, загальні риси (гіперфункціонального стан секреторних і сполучнотканинних клітин, порушення в белоксінтезйрующіх і енергообразующіх структурах клітин, катаболічних спрямованість процесів в них, порушення в ультраструктурі базальних клітинних мембран, капілярів і нервових закінчень) і зробити висновок про односпрямованість порушень, але різного ступеня їх висловлю нности. Все сказане дає підставу вважати, що існує патогенетичне єдність виразкової хвороби з різною локалізацією виразкового процесу і передвиразковий стану як початкової. пред'язвенное, стадії хвороби.
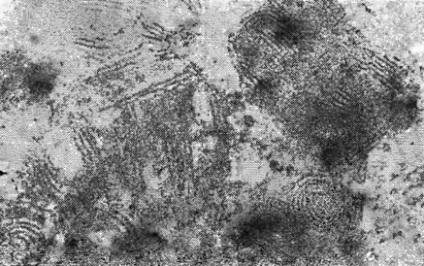
Мал. 17. Ділянка гладкої клітини, на якому розташовані зрілі гранули, котрі піддаються дезагрегації. X 48 000
У той же час активність ферментів, що відображають процеси окисного фосфорилювання, - СДГ, АТФ-аза (магній-залежна аденозинтрифосфатаза) і, в меншій мірі, ЦХО була знижена (рис. 22). Причому, якщо при шлункової локалізації виразки спостерігалося рівномірне зниження в МОР активності цих ферментів, то при дуоденальної виразці спостерігалися вогнищеві зміни активності СДГ і особливо ЦХО. Поряд з різким зниженням їх активності відзначали осередки підвищеної активності, що, мабуть, за даними Л. І. Аруін (1969) та І. А. Морозова (1977), відповідає місцезнаходженню парієтальних клітин, при дуоденальної виразці мало пошкоджений.
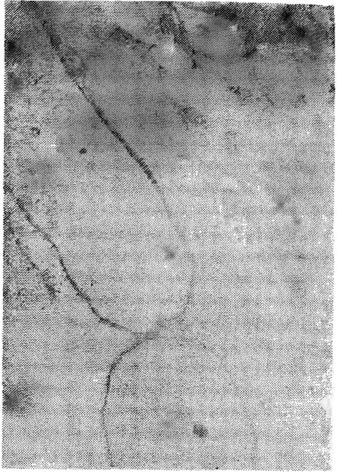
Мал. 19. Helicobacter pylori з CO антрального відділу шлунка в стані активного ділення.
Хворий з хронічним гастритом типу В (невиразкова диспепсія - пред'язвеіное стан). Х48 000
При гістохімічному дослідженні МОР на кислу фосфатазу (КФ) і арилсульфатазу (АРС) нами виявлено виражене підвищення активності цих ферментів як при шлункової, так і при дуоденальної локалізації виразки, на підставі чого можна говорити про підвищений вихід лізосомальних гідролаз, що обумовлюють катаболическую спрямованість, процесів в МОР. Отримані нами дані підтверджують результати досліджень, виконаних на ультраструктурному рівні, які свідчать про те, що виразкова хвороба супроводжується різким переважанням катаболічних процесів над белковосінтетіческой в сож-.
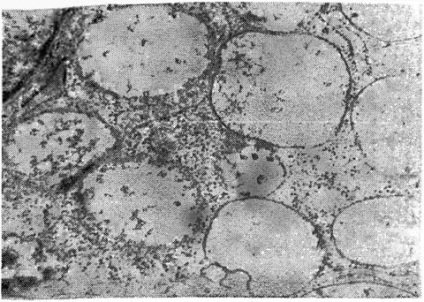
Мал. 20. Порушення енергоутворення (лізис крист мітохондрії) в мукоїдного клітці хворого з передвиразковий станом, х 48 000
Останнє може бути пов'язано як з активацією лізосомальної системи - великої кількості всіх її елементів, так і з підвищеним виходом в цитоплазму лізосомальних гідролаз.
В результаті проведених нами гістоензімологіческіх досліджень МОР на лужну фосфатазу (ЛФ) і АТФ-азу при виразковій хворобі обох локалізацій ми змогли встановити зниження активності цих ферментів. Оскільки ЛФ і АТФ-аза в МОР розташовуються в основному в стінці капілярів і в молодої грануляційної тканини, слід вважати, що зниження їх активності в МОР при виразковій хворобі свідчить про знижених репаративні можливості сполучної тканини і порушення мікроциркуляції.
В результаті проведених досліджень зроблено висновок, що в розвитку порушень в МОР у хворих на виразкову хворобу-основне патогенетичне значення мають порушення нервової трофіки, мікроциркуляції, що ведуть до гіпоксії та пригнічення пластичних процесів (зниження синтезу і посилення катаболізму білка), що в сукупності є основою порушення резистентності - одного з факторів, відповідальних за язвообразование.
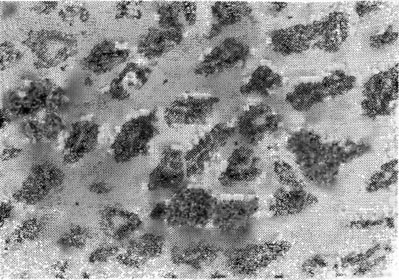
Мал. 21. Різке посилення реакції на кислу фосфатазу в МОР у хворого на виразкову хворобу дуоденальної локалізації. Х180

Мал. 22. Осередкове ослаблення реакції на цитохромоксидазу в МОР хворого на виразкову хворобу шлунковоїлокалізації (по Нокласу і співавт.). Х180