Процес розчині-ня ВМС протікає мимовільно, але протягом длитель-ного часу, і йому часто передує набухання полімеру в розчиннику.
Полімери, макромолекули яких мають симетричну форму, можуть переходити в розчин, попередньо-тельно НЕ набухаючи. Наприклад, гемоглобін, печінковий глікоген при розчиненні майже не набухають, а розчини цих речовин не володіють високою в'язкістю навіть при срав-ково великих концентраціях, в той час як речовини з більш асиметричними витягнутими молекулами при розчиненні дуже сильно набухають (желатин, целюлоза, нату-ральний і синтетичні каучуки).
Набухання - збільшення маси і об'єму полімеру за рахунок проникнення молекул розчинника в просторову структуру ВМС.
Причина набухання - велика раз-ка в розмірах молекул речовини, що розчиняється і розчини-теля і, як наслідок, велика різниця в швидкостях їх диф-фузії. При набуханні спочатку відбувається практичні скі одностороння дифузія молекул розчинника в про-просторову сітку полімеру, що має ту ж природу, що і осмос розчинника в осмотичну осередок через пори напівпроникною мембрани.
Механізм набухання зводиться до проникнення молекул розчинника в найближчі шари полімеру і сольватації со-відповідних ділянок полімерного ланцюга. В результаті мак-ромолекули «розрихлюються», що полегшує подальше про- нення молекул розчинника і збільшення маси і об'єк-ема полімеру.
Розрізняють два види набухання: необмежену, заканчи-вающий повним розчиненням ВМС (наприклад, набухання желатини в воді, каучуку в бензолі, нітроцелюлози в ацето-ні) і обмежене, що приводить до утворення набряклого полімеру - холодцю (наприклад, набухання целюлози в воді, желатин в холодній воді, вулканізованого каучуку в бен-золі). Холодець є просторовою сітку, що складається з пов'язаних між собою макромолекул полімерних-ра і заповнену молекулами розчинника.
Ступінь обмеженості процесу набухання і можли-ність мимовільного розчинення визначаються соотно-ням енергії зв'язку в решітці полімеру і енергії сольва-тації полімерного ланцюга з урахуванням ентропійного фактора.
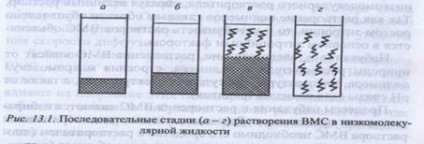
Весь процес набухання і розчинення ВМС можна умовах а-а розділити на ряд стадій: (рис. 1).
1. На початковій стадії (рис. 1, а) система складається з двох компонентів: полімеру і низкомолекулярной рідини.
2. Пе-реход а -> б характеризується інтенсивним проникненням молекул низькомолекулярної рідини в структуру полімеру і сольватацией полімерного ланцюга, що супроводжується виокрем-ленням теплоти (# 916; Н <0). Изменение энтропии по сравнению с энтальпийным фактором незначительно. При этом объем полимера возрастает, но общий объем системы «полимер-растворитель» уменьшается. Это явление называется кон-тракцией, а выделение теплоты говорит о физико-химической природе процесса.
3. Перехід б -> в являє собою початковий етап розбраті-ділення макромолекул полімеру по всьому об'єму розчиніть-ля і характеризується зростанням ентропії системи внаслідок зростання числа можливих конформацій. Ентальпія сис-теми якщо і змінюється, то незначно.
На даному етапі зазвичай відбувається основне збільшення обсягу і маси по-Лімер, що є результатом подальшого пронікнове-ня молекул розчинника в полімерну сітку, її розпушити-ня і пов'язане з цим часткове звільнення макромоле-кул. Окремі макромолекули починають відриватися один від одного і переходити в шар низкомолекулярной рідини. Обмежене набухання закінчується на стадії б або в утворенням холодцю. Подальший розвиток процесу - Ні-обмежене набухання - призводить до розчинення полімеру, тобто до утворення розчину ВМС.
4. Перехід в -> г відбувається в результаті сил дифузії і характеризується зна-ве збільшенням ентропії системи. При цьому макро-молекули ВМС рівномірно розподіляються по всьому об'єму низькомолекулярного розчинника, утворюючи справжній розчин.
Так як розчинення полімерів головним чином обумовлено зростанням ентропії, то і стійкість розчинів ВМС пояснив-ється в основному ентропійних фактором.
Набухання і розчинення ВМС залежать від:
1. природи розчинника і полімеру,
2. будови макромолекул полімеру,
4. присутності електролітів,
5. від рН середовища (для поліелектролітів).
Процеси набухання і розчинення, ВМС є виборчі-них процесами. Для утворення розчину ВМС необхідно його спорідненість з розчинником (ліофільность). Неполярні полімери добре набухають (раство-ряют) в неполярних розчинниках (каучук в бензолі або бензині) і не набухають в полярних. Полярні полімери краще набухають (розчиняються) в полярних рідинах (білок у воді) і не набухають в неполярних.
Через спорідненості полімеру з розчинником при набуханні і розчиненні велика частина розчинника «зв'язується» в сольватні (гідратів) оболонки. Особливо це характерно для полярних макромолекул у водному середовищі. І оскільки макромолекули мають великий поверхнею, то для не-обмеженого набухання (розчинення) навіть в ліофільної системі потрібна достатня кількість рідини. Інакше процес набухання може зупинитися на стадії обмежений-ного набрякання, тобто освіти холодцю.
Істотну роль в набуханні грає будова макро-молекул полімеру. Наприклад, полімери з довгими жорсткі-ми ланцюгами і великою кількістю полярних груп добре набухають, але не розчиняються навіть у відповідному рас-творитель (целюлоза у воді). Якщо полімер розчиняється в рідині не досить добре, то також утворюється холодець.
Температура на ці процеси впливає відповідно до принципу Ле Шательє. Оскільки набухання супроводжує-ся виділенням теплоти на першому етапі, то з підвищенням температури ступінь набухання, а також розчинність по-Лімер, зменшуються. На другій стадії набухання може стати ендотермічним процесом. Отже, в цьому випадку набухання зі зростанням температури збільшується.
Наприклад, якщо в холодній воді желатину набухає ограни-ченно, то з підвищенням температури - необмежено, тобто розчиняється. При охолодженні отриманого розчину знову утворюється холодець. Однак швидкість набухання (розчинення) полімерів зі збільшенням температури зростає з огляду на збільшен-ня швидкості дифузії.
Дія іонів електролітів на набухання полярного ВМС пов'язано з їх здатністю до гідратації. Оскільки аніони гидратируются більше, ніж катіони, то катіони впливають на набухання цих полімерів незначно.
За спо-можності зменшувати набухання аніони розташовуються в так званий ліотропний ряд або ряд Гофмейстера (при одному і тому ж катіоні): СNS -
Іони СNS - підсилюють набухання внаслідок того, що, слабо гидратируясь, вони добре адсорбуються на макроме-лекул ВМС. А іони SO4 2- процес набухання гальмують, так як сульфат-іони сильніше всіх аніонів цього ряду гідратів-ються, зменшуючи цим кількість «вільної» (не пов'язаний-ний в гідратів оболонки) води.
Вплив рН середовища особливо значно для високомол-кулярной електролітів (білків, нуклеїнових кислот, вироб-водних целюлози і крохмалю). Мінімум набухання відзначатимуть-ється в ВЕТ, оскільки в ній сумарний електричний заряд макромолекул білків і, відповідно, ступінь їх гідрату-ції мінімальні. При більш низьких або більш високих значеннях рН збільшується іонізація функціональних груп, що призводить до розштовхування однойменно заряджених ділянок полімерного ланцюга і її розпушення. Внаслідок цього молі-кули води легше проникають в простір між ланцюгами, що відбивається на величині набухання в бік її збільшення.
Кількісною характеристикою обмеженого набухання полімерів є ступінь набухання # 945 ;. визначається відношенням приросту маси (т - т0) або обсягу (V- V0) полімеру до його первісної масі то (обсягом V0):
де т - маса (V- обсяг) набряклого полімеру.
Набухання полімерів супроводжується виникненням тиску, яке назвали тиском набухання (≈ 5 # 8729; 10 5 -10 # 8729, 10 5 Па). Механізм його виникнення подібний до механізму виникнення осмотичного тиску. Це тиск легко виявляється, коли яка-небудь перешкода заважає увели-ню обсягу полімеру.