Загальні відомості про аміаку і ступеня окислення в NH3
У звичайних умовах аміак являє собою безбарвний газ з різким задушливим запахом.
Брутто-формула - NH3. Молярна маса - 17 г / моль. Молекула аміаку має форму тригональной піраміди (dNH = 0,10 нм, кут HNH дорівнює 107,3 o). Згідно з методом валентних зв'язків, це відповідає sp 3-гібридизації валентних орбіталей атома азоту (рис. 1).
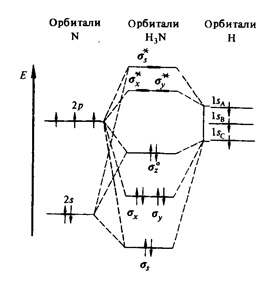
Мал. 1. Енергетична діаграма орбіталей молекули аміаку.
При охолодженні до (-33,4 o C) аміак під звичайним тиском перетворюється в прозору рідину, що твердіє при (-77,8 o C).
Аміак добре розчинний у воді: один об'єм води розчиняє при кімнатній температурі близько 700 обсягів аміаку. Концентрований розчин містить 25% (мас.) NH3 і має густину 0,91 г / см 3 .Раствор аміаку у воді називають нашатирним спиртом.
NH3, ступеня окислення елементів в ньому
Щоб визначити ступеня окислення елементів, що входять до складу аміаку, спочатку необхідно розібратися з тим, для яких елементів ця величина точно відома.
Аміак - це тривіальне назва гідриду азоту, а, як відомо, ступінь окислення водню в гидридах дорівнює (+1). Для знаходження ступеня окислення азоту приймемо її значення за «х» і визначимо його за допомогою рівняння електронейтральності:
Значить ступінь окислення азоту в аміаку дорівнює (-3):
Приклади розв'язання задач
Максимальну ступінь окислення центральний елемент має в гідроксосоедіненіі:
Для того, щоб знайти правильну відповідь на поставлене запитання будемо по черзі перевіряти кожен із запропонованих варіантів.
а) Центральним атомом є хлор. Приймемо значення ступеня окислення хлору за «х» і складемо рівняння електронейтральності. Ступені окислення кисню і водню рівні (-2) і (+1) відповідно.
1 + (-2) + х + 2 × (-2) = 0;
б) Центральним атомом є фосфор. Приймемо значення ступеня окислення фосфору за «у» і складемо рівняння електронейтральності. Ступені окислення кисню і водню рівні (-2) і (+1) відповідно.
3 × 1 + 3 × (-2) + у + (-2) = 0;
в) Центральним атомом є сірка. Приймемо значення ступеня окислення сірки за «z» і складемо рівняння електронейтральності. Ступені окислення кисню і водню рівні (-2) і (+1) відповідно.
2 × 1 + 2 × (-2) + z + 2 × (-2) = 0;
г) Центральним атомом є фосфор. Приймемо значення ступеня окислення фосфору за «а» і складемо рівняння електронейтральності. Ступені окислення кисню і водню рівні (-2) і (+1) відповідно.
3 × 1 + 3 × (-2) + а = 0;
Найменше значення ступеня окислення одно (+3), воно характерно для фосфору в з'єднанні складу (HO) 3 P.