Виробництво фосфорної кислоти. Фізико-хімічні основи процесу. Технологічна схема
Фосфорна кислота H3 PO4 є найважливішим проміжним продуктом у виробництві концентрованих фосфоровмісних добрив. Крім того, фосфорна кислота використовується у виробництві різних технічних солей, фосфорорганічних сполук, в тому числі інсектицидів, напівпровідників, іонообмінних смол, а також для створення захисних покриттів на металах. Очищена або так звана харчова фосфорна кислота використовується в харчовій промисловості, для приготування кормових концентратів і фармацевтичних препаратів.
Сировина для виробництва фосфорної кислоти - див. Сировинна основа хімічної промисловості (лекція 1).
Фосфор витягують з фосфатних руд їх розкладанням. В даний час найбільшого поширення набуло кислотне розкладання руд, що містять більше 25% Р2 О5. Фосфорна кислота утворюється безпосередньо при розчиненні руди, тобто прямим вилученням сполук фосфору екстракцією. Звідси назва продукту - екстракційна фосфорна кислота (ЕФК). З бідніших руд отримують термічну фосфорну кислоту. Контроль здійснюється шляхом відновлення фосфору з природних фосфатів коксом при високих температурах і подальшому отриманні Н3 РО4 з фосфору.
Функціональна схема виробництва ЕФК.
Складність складу вихідної сировини, яке не може бути уніфіковано, призводить до існування ряду варіантів технологічних схем його переробки. Одним з добре досліджених є сернокислотное розкладання апатитового концентрату, одержуваного збагаченням хибинских апатито-нефелінових руди і містить близько 39% Р2 О5. Його розкладання - гетерогенна реакція "рідина - тверде тіло".
Виділення домішок полегшується переходом їх в іншу фазу. Кальцієва складова випадає в осад у вигляді гіпсу (CaSO4), друга йде в газову фазу у вигляді фтороводорода HF. Функціональна схема виробництва ЕФК (рис. 1) включає розкладання подрібненої сировини в реакторі (екстракторі), фільтрацію твердого осаду, упаривание фосфорної кислоти до товарної концентрації та очищення газів, що відходять. Твердий відхід отримав назву "фосфогіпс". Утворений фтороводород взаємодіє з порожньою породою сировини
Тому при промиванні газів, що відходять водою обидва летючих продукту уловлюються у вигляді кремнефтористоводородной кислоти H2 SiF4.
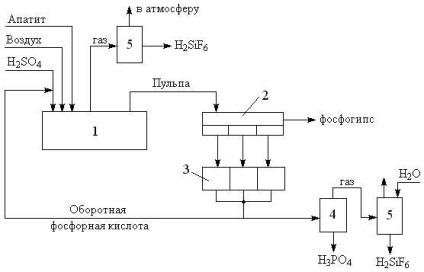
Малюнок. 1. Функціональна схема виробництва екстракційної фосфорної кислоти.
1 - реактор розкладання апатиту (екстрактор); 2 - вакуум фільтр; 3 - збірка фільтратів;
4 - колона випарювання фосфорної кислоти; 5 - система очищення газів.
Сірчанокислотне розкладання апатиту.
На швидкість перетворення апатиту по реакції (1) впливає відведення продуктів реакції - іонів Са 2+ і від поверхні частинок в розчин, і чим менше концентрація Са 2+ в розчині, тим швидкість розчинення буде більше.
Одночасно з розчиненням апатиту відбувається утворення твердого CaSO4. який погано розчинний. Зв'язування Са 2+ в CaSO4 має збільшувати швидкість розчинення апатиту. Здавалося б, збільшення концентрації сірчаної кислоти, тобто іонів - фактор сприятливий. Але викликають не тільки осадження Са 2+ у вигляді окремої фази в розчині, а й на поверхні частинок апатиту. Утвориться кірка CaSO4 спочатку уповільнює розчинення, а потім блокує поверхню, і розчинення практично припиняється. Тому є деяка оптимальна концентрація CaSO4. при якій ступінь вилучення фосфору з сировини буде максимальною. Таким чином, до концентрації Н2 SO4 в реакторі висуваються жорсткі вимоги: суворе підтримання цієї концентрації на оптимальному рівні в усьому обсязі реакційної зони.
Реакційний вузол являє собою послідовність секцій з інтенсивним перемішуванням реагентів в кожній з них і перетіканням між ними для організації руху реакційної маси по каскаду. Перемішування має запобігти розшарування на тверду і рідку фази. У перших секціях відбувається в основному розчинення апатиту. Решта секції працюють як дозреватель, в них формуються кристали CaSO4. Між останньою і першою секціями організований інтенсивний рецикл (при кратності циркуляції 20 і більше).
Щоб створити сприятливі умови спочатку для розчинення, коли необхідно мати балансову концентрацію, а потім для формування кристалів при невеликому надлишку організовують розподілену подачу сірчаної кислоти в одну з перших і в одну з останніх секцій каскаду. Ступінь розкладання апатиту досягає 97% і вище, утворюються великі кристали, що полегшують їх відділення фільтрацією.
Освіта продукционной фосфорної кислоти включає в себе відділення осаду CaSO4 (фосфогіпсу) і концентрування кислоти. Залежно від умов розкладання утворюються кристали CaSO4 × 2Н2 О (дигідрат) або CaSO4 × 0,5Н2 О (напівгідрат). У дігідратном процесі температура 343-353 К і концентрація фосфорної кислоти 25-35%. У полугідратном процесі ці показники становлять 358-378 К і 35 мас. %. Фосфогіпс відокремлюють на вакуум-фільтрі. Фільтрат направляють на випарювання, де концентрація кислоти збільшується до 52-54%. Це і є продукційна кислота. При випаровуванні з кислоти видаляється 80-90% фтору у вигляді HF. Відходять з реактора і з вузла випарювання фторвмісні гази в системах очищення поглинаються з утворенням кремнефтористоводородной кислоти.
На одну тонну продукту утворюється понад 2,5 т важко переробляється CaSO4. C ним втрачається сірчана кислота, її ефективна промислова регенерація із фосфогіпсу до сих пір не розроблена. Фосфогіпс використовується для виробництва гіпсових в'яжучих добавок до цементу, будівельних виробів, в сільському господарстві для гіпсування солонцюватих ґрунтів. Велика частина фосфогіпсу складується у відвали.
Екстракційна кислота використовується для отримання фосфорних добрив. Для інших цілей використовується концентрована фосфорна кислота, яку отримують електротермічним методом. Він заснований на відновленні фосфору з фосфатів в електродугових печах з подальшим окисленням елементарного пароподібного фосфору (Р4) до його оксиду
7.3.3. Фосфорні добрива. Фізико-хімічні основи процесів їх виробництва. Типи реакційних вузлів.
Існує ряд методів переробки природних фосфатів в добрива: механічні, термічні і методи кислотного розкладання.
Одним з методів механічної обробки є подрібнення фосфатів. Отримана фосфористая борошно при використанні в кислих грунтах повільно розчиняється в грунтових водах і таким чином стає довготривало діючим добривом.
Фосфорні добрива можуть бути отримані термічним розкладанням фосфатів при температурах 1200 - 1800 ° С. Так отримують термофосфати, обесфторенниє фосфати, плавлені магнієві і термощелочние фосфати.
Основним методом отримання фосфорних добрив є хімічне розкладання фосфатної сировини. Так, в результаті кислотною обробки отримують простий суперфосфат і фосфорну кислоту, яку в свою чергу, переробляють в подвійний суперфосфат, преципітат і складні добрива.
Сутність виробництва простого суперфосфату складається в перетворенні природного фторапатита, нерозчинного у воді і ґрунтових розчинах, в розчинні сполуки, переважно в монокальцийфосфат (Ca (H2 PO4) 2)
У цьому процесі розкладання протікає в дві стадії. На першій стадії близько 70% апатиту реагує із сірчаною кислотою. При цьому утворюється фосфорна кислота і напівгідрат сульфату кальцію (рівняння (1)). Ця стадія характеризується утворенням поверхневих плівок CaSO4 на зернах фосфату. Структура утворюється кірки обумовлена швидкістю кристалізації твердої фази, що залежить головним чином від пересичення розчину сульфатом кальцію, яке визначається в свою чергу концентрацією сірчаної кислоти, температурою та іншими факторами. Тому необхідна оптимальна концентрація сірчаної кислоти, що поєднує достатню швидкість розчинення апатиту з утворенням пухкої плівки, більш проникною для дифузії сірчаної кислоти до поверхні фосфату. Перша стадія закінчується через 20 - 40 хвилин після змішування фосфату з сірчаною кислотою. Після повного зникнення сірчаної кислоти починається друга стадія розкладання, в якій залишився апатит (
30%) розкладається фосфорною кислотою
Утворений монокальцийфосфат на відміну від сульфату кальцію не відразу випадає в осад. Він поступово насичує розчин фосфорної кислоти, після чого починає викристалізовуватися у вигляді Ca (H2 PO4) 2 × H2 O і протікає значно повільніше, ніж реакція (1), що пояснюється низькою активністю фосфорної кислоти і кристалізацією твердих фаз. Вона починається в суперфосфатних камерах і триває протягом 5 - 20 діб зберігання суперфосфату на складі.
Для отримання твердого продукту більш високої якості суперфосфат перед дозріванням піддають нейтралізації твердими добавками (вапняком, фосфоритного борошном і т.п.) і гранулюють.